帕金森病
| A+醫學百科 >> 帕金森病 |
帕金森病(Parkinson's disease,簡稱PD)又稱"震顫麻痹",巴金森氏症或柏金遜症,是一種常見於中老年的神經系統變性疾病,多在60歲以後發病。主要表現為患者動作緩慢,手腳或身體的其它部分的震顫,身體失去了柔軟性,變得僵硬。最早系統描述該病的是英國的內科醫生詹母.帕金森,當時還不知道該病應該歸入哪一類疾病,稱該病為「震顫麻痹」。 帕金森病是老年人中第四位最常見的神經變性疾病,在≥65歲的人群中,1%患有此病;在>40歲的人群中則為0.4%.本病也可在兒童期或青春期發病。
目錄 |
發病原因
迄今為止,PD的病因仍不清楚。目前的研究傾向於與年齡老化、遺傳易感性和環境毒素的接觸等綜合因素有關。
1)年齡老化:帕金森主要發生於中老年人,40歲以前發病少見,提示老齡與發病有關。研究發現,自30歲以後,黑質多巴胺能神經元、酪氨酸氧化酶和多巴脫羧酶活力,紋狀體多巴胺遞質水平隨年齡增長逐漸減少。然而,僅少數老年人患此病,說明生理性多巴胺能神經元蛻變不足以致病,年齡老化只是本病發病的促發因素。
2)環境因素:流行病學調查結果發現,帕金森病的患病率存在地區差異,所以人們懷疑環境中可能存在一些有毒的物質,損傷了大腦的神經元。
3)遺傳易患性。近年在家族性帕金森病患者中曾發現a共同核素基因的Alα53THr突變。但以後多次未被證實。
4)家族遺傳性:醫學家們在長期的實踐中發現帕金森病似乎有家族聚集的傾向,有帕金森病患者的家族其親屬的發病率較正常人群高一些。
目前普遍認為,帕金森並非單一因素,多種因素可能參於其中。遺傳因素可使患病易感性增加,只有與環境因素及衰老的相互作用下,通過氧化應激、粒線體功能衰竭、鈣超載、興奮性胺基酸毒性作用、細胞凋亡、免疫異常等機制才導致黑質多巴胺能神經元大量變性丟失而發病。
發病機制
PD與紋狀體內的多巴胺(DA)含量顯著減少有關。目前較公認的學說為「多巴胺學說」和「氧化應激說」。
前者指出DA合成減少使紋狀體DA含量降低,黑質-紋狀體通路多巴胺能與膽鹼能神經功能平衡失調,膽鹼能神經元活性相對增高,使錐體外系功能亢進,發生震顫性麻痹。
後者解釋了黑質多巴胺能神經元變性的原因,即在氧化應激時,PD患者DA氧化代謝過程中產生大量H2O2和超氧陰離子,在黑質部位Fe2+催化下,進一步生成毒性更大的羥自由基,而此時黑質粒線體呼吸鏈的複合物I活性下降,抗氧化物(特別是谷胱甘肽)消失,無法清除自由基,因此,自由基通過氧化神經膜類脂、破壞DA神經元膜功能或直接破壞細胞DNA,最終導致神經元變性。
1997年,美國國家衛生研究院的波利摩羅普洛斯(Mihael H. Polymeropoulos)及同事,研究義大利與希臘家庭中,出現家族遺傳性帕金森氏症的患者,在α-synuclein這種蛋白質的基因中,找到一種基因突變。這種突變屬於自體顯性突變,意思就是說,只要從父親或母親遺傳到這種突變,就可以造成疾病。α-synuclein 基因的突變極罕見,而且對全球這麼多帕金森氏症患者來說也不顯著,在患者中所佔的比例遠低於1%。但是發現蛋白質與帕金森氏症之間的關聯,引發了許多研究。部份原因是不管α-synuclein蛋白是否正常,都是蛋白堆塊中的一種蛋白質。研究人員認為,進一步了解突變如何造成帕金森氏症,或許可以提供一些線索,了解偶發性疾病患者腦中,製造多巴胺的黑質細胞路易體的形成機制。
α-synuclein 基因製造的蛋白質很小,只含有144個胺基酸,據信與細胞間的訊號溝通有關。突變會造成蛋白質胺基酸序列的微小變化。事實上,目前已知有幾種這樣的突變,其中兩種會造成序列上某一個胺基酸改變。果蠅、線蟲與小鼠的研究顯示,如果突變α-synuclein的產量很高,就會造成多巴胺細胞退化與運動缺失。其他研究則顯示,突變的α-synuclein無法正常摺疊,而且會堆積在路易體。突變的α-synuclein也會抑制泛素–蛋白分解體系統,因而不會受蛋白分解體分解。此外,最近的證據也逐漸顯示,額外的正常α-synuclein 基因可以造成帕金森氏症。
1998年,也就是發現α-synuclein突變後的一年,日本順天堂大學的水野美邦與慶應大學的清水信義,在另一群家族遺傳性帕金森氏症患者身上,找到了第二個突變基因parkin 。這種突變大多在40歲以前診斷出帕金森氏症的患者身上發現;越早發病的人越有可能是因為parkin 突變的結果。這種突變屬於自體隱性突變,雖然從雙親身上各遺傳一個突變基因的人最終會發病,但只帶一個缺失基因的人,罹患帕金森氏症的風險也會比較高。parkin 突變似乎比α-synuclein 基因的突變更常見,但目前還沒有足夠的統計數字能夠證實。
parkin 基因所產生的蛋白質稱為帕金蛋白(parkin protein),它帶有許多蛋白質都有的一些胺基酸序列(稱為功能區)。最有趣的是兩個稱為RING的功能區,有RING功能區的蛋白質都參與了蛋白質分解的過程。現在的研究發現指出,在類帕金森氏症患者身上,神經元死亡的原因,有部份是因為蛋白質清除系統的泛素化過程出了問題,因為帕金蛋白會將泛素接到摺疊錯誤的蛋白質,沒有這個步驟,就不會有泛素的標示,蛋白質就無法清除。最近我們的研究指出,路易體中一種稱為BAG5的蛋白質,可以和帕金蛋白結合,並抑制帕金蛋白的功能,造成多巴胺神經元的死亡。
有趣的是,在某些parkin 突變的帕金森氏症患者身上,並沒有發現到黑質神經元有路易體。這項觀察顯示,除非泛素接到蛋白質的過程正常運作,蛋白質可能不會聚在一起。這項觀察也暗示,有害蛋白質沒有聚集在路易體時,可能會為細胞帶來災難。因為parkin 突變的患者很早就會出現帕金森氏症,可能是因為他們缺乏一開始時,將有毒的蛋白質堆積以隔離的保護作用。
其他新近的發現,則凸顯更多遺傳造成的細胞機具的混亂。2002年,荷蘭鹿特丹伊萊玆馬斯醫學研究中心的波尼法蒂(Vincenzo Bonifati)及同事,在荷蘭與義大利的家族中,找到了一種叫DJ-1 基因的突變。這種突變像parkin ,會造成自體隱性遺傳的帕金森氏症。研究人員也在家族遺傳性帕金森氏症患者身上,發現到另一種叫做UCHL1 基因的突變。《科學》有一篇文章指出,PINK1 基因的突變可能會造成黑質細胞的代謝缺失與死亡。另一項研究則找到一種叫LRRK2 的基因,這個基因會製造一種叫做震顫素(dardarin)的蛋白質(患者來自法國與西班牙交界的巴斯克區域,當地居民稱這種症状為dardarin,意指「震顫」)。這種蛋白質也與代謝有關,而且出現在家族遺傳性的帕金森氏症患者中。不過,研究人員只要再一些時間,就可以真正了解這些突變是怎麼造成問題的。
臨床表現
人們對該病進行了更為細緻的觀察,發現除了震顫外,尚有肌肉僵直、寫字越寫越小等其它症状,但是四肢的肌肉的力量並沒有受損,認為稱麻痹並不合適,所以建議將該病命名為「帕金森病」。
靜止性震顫
震顫往往是發病最早期的表現,通常從某一側上肢遠端開始,以拇指、食指及中指為主,表現為手指象在搓丸子或數鈔票一樣的運動。然後逐漸擴展到同側下肢和對側肢體,晚期可波及下頜、唇、舌和頭部。在發病早期,患者並不太在意震顫,往往是手指或肢體處於某一特殊體位的時候出現,當變換一下姿勢時消失。以後發展為僅於肢體靜止時出現,例如在看電視時或者和別人談話時,肢體突然出現不自主的顫抖,變換位置或運動時顫抖減輕或停止,所以稱為靜止性震顫,這是帕金森病震顫的最主要的特徵。 震顫在病人情緒激動或精神緊張時加劇,睡眠中可完全消失。震顫的另一個特點是其節律性,震動的頻率是每秒鐘 4-7 次。這個特徵也可以幫助我們區別其它的疾病,如因舞蹈病、小腦疾患、還有甲狀腺機能亢進等引起的疾病。
肌肉僵直
帕金森病患者的肢體和軀體通常都失去了柔軟性,變得很僵硬。病變的早期多自一側肢體開始。初期感到某一肢運動不靈活,有僵硬感,並逐漸加重,出現運動遲緩、甚至做一些日常生活的動作都有困難。如果拿起患者的骼膊或腿,幫助他活動關節,你會明顯感到他的肢體僵硬,活動其關節很困難,象在來回折一根鉛管一樣。如果患肢同時有震顫,則有斷續的停頓感,就象兩個咬合的齒輪轉動時的感覺。
運動遲緩
在早期,由於上臂肌肉和手指肌的強直,病人的上肢往往不能作精細的動作,如解系鞋帶、扣紐扣等動作變得比以前緩慢許多,或者根本不能順利完成。寫字也逐漸變得困難,筆跡彎曲,越寫越小,這在醫學上稱為「小寫症」。面部肌肉運動減少,病人很少眨眼睛,雙眼轉動也減少,表情呆板,好象戴了一副面具似的,醫學上稱為「面具臉」。行走時起步困難,一旦開步,身體前傾,重心前移,步伐小而越走越快,不能及時停步,即 「慌張步態」。行進中,患側上肢的協同擺動減少以至消失;轉身困難,要用連續數個小碎步才能轉身。因口、舌、鄂及咽部肌肉的運動障礙,病人不能自然咽下唾液,導致大量流涎。言語減少,語音也低沉、單調。嚴重時可導致進食飲水嗆咳。病情晚期,病人坐下後不能自行站立,臥床後不能自行翻身,日常生活不能自理。
特殊姿勢
儘管患者全身肌肉均可受累,肌張力增高,但靜止時屈肌張力較伸肌高,故病人出現特殊姿勢:頭前傾、軀幹略屈、上臂內收、肘關節彎曲、腕略伸、指掌關節彎曲而指間關節伸直,拇指對掌,髖及膝關節輕度彎曲。
疼痛
很多患者都會出現疼痛,雖然沒有嚴重到必須吃止痛藥的地步,但疼痛有時會非常令病人苦惱。疼痛的表現是多方面的,可以表現為肩頸部痛、頭痛、腰痛,出現最多的症状是手臂或腿的酸痛,局部的肌肉僵直是其主要原因。
治療帕金森病肌肉僵直引起的疼痛,補充左旋多巴有很好的療效,多數病人在藥物起效時隨著肌肉僵直的緩解而緩解。但在用藥的後期,少數患者在左旋多巴起效的高峰期反而會出現下肢,尤其是足趾的痙攣性疼痛。出現這種情況往往比較難處理,因為這顯然是左旋多巴的副作用,減少劑量往往可以減輕痛性痙攣的症状,但同時又使帕金森病的症状不能很好緩解。遇到這種情況,醫生往往是採用減少每次左旋多巴的用量,但增加給藥的次數,或者增加多巴胺受體激動劑的藥量。如果不能奏效,可以嘗試局部注射肉毒素方法,可以起到緩解的作用。
感覺異常
帕金森病患者還會有身體的某些部位出現異常的溫熱或是寒冷的症状,出現異常溫熱感覺的病人多一些。這種異常的溫度感多出現在手、腳。還有患者的異常感覺在身體的一側或是出現在體內,如感到胃部或是下腹部不適。病人中出現異常發熱感的情況比較多見,身體的某些部位甚至會出現一種燒灼感。一個得了帕金森病十多年的老年婦女有嚴重的腰部燒灼感。當藥物失效時,其燒灼的感覺會更加嚴重,但當調整病人的用藥有效地控制病情時,其症状也會得到改善。說明這種異常感覺還是帕金森病本身的症状。
對這種症状用麻醉藥物治療無效也缺乏特異性療法,通常對帕金森氏病的治療會對這種症状有所改善,有時加用一種叫卡馬西平的藥物會有一些效果。
吞咽困難
在帕金森病的晚期,會出現吞咽困難。
現在,除了帕金森病本身造成吞咽障礙以外,各地都有一些手術後造成的吞咽障礙,其結果比前者更加嚴重,而且抗帕金森病治療對它是無效的。其原因是雙側蒼白球切開術或其它術式造成的吞咽麻痹,是一種器質性的損害,很難恢復。這種情況除了功能鍛煉和慢慢恢復外,沒有什麼好的方法。
言語障礙
言語障礙是帕金森病患者的常見症状,表現為語言不清、說話音調平淡,沒有抑揚頓挫、節奏單調等等。
其 他
可有植物神經功能紊亂現象,如唾液和皮脂腺分泌增多,汗分泌增多或減少,大、小便排泄困難和直立性低血壓。少數病人可合併痴呆或抑鬱等精神症状。
除了上面介紹的症状之外,帕金森病患者還有以下一些特殊症状:
油脂面 帕金森病病人的前額總是油光發亮。
流涎 有很多帕金森病的患者經常出現流口水的現象,嚴重者需要別人拿著手帕不停地為他擦拭。研究發現病人的唾液分泌並沒有增加,而是因帕金森病人吞咽反射困難,自動吞咽動作的減少使唾液在口腔內淤積的原因,淤積的量大了唾液就會自動流出。因此,患者要經常有意識的將唾液吞咽下去可減少流口水。對年輕的患者,應用抗膽鹼藥物如安坦可以抑制唾液的分泌。
膀胱刺激症状 部分帕金森病患者往往一天中要上洗手間數次,尤其是晚上夜尿的次數多,並因此導致失眠。尿意有時是不可遏制的,加上患者本身行動緩慢,很容易導致尿濕褲子。
下肢腫脹 帕金森病病人有時會出現下肢的腫脹現象,主要出現在腳部,嚴重時會波及小腿。通常在先出現障礙的那一側下肢。那些有顯著運動遲緩的病人,腳部腫脹更容易見到。它通常在晚間睡眠之後減輕或消失,但是白天又會逐漸變得嚴重起來。出現的原因是由於帕金森病患者缺乏活動,不能通過腿部的活動和肌肉的收縮來把靜脈血液擠壓到心臟,使靜脈血淤積在靜脈血管中,組織液外滲,引起腳部和踝關節的浮腫。
嚴重時,可以採取些對症的治療方法,如用一些利尿性藥物。晚上睡覺時,可將腳墊高一些,這樣有利於靜脈迴流,減輕水腫。
出現上述情況,往往與帕金森病的症状控制不好有關,抗帕金森病的治療在減輕帕金森病症狀的同時,膀胱的症状也隨之得到改善。值得一提的是多巴胺受體激動劑協良行對改善帕金森病患者的膀胱症状有較好的作用。
如果通過抗帕金森病的治療,症状不見好轉,則應考慮是否合併有其它疾病,如是否有泌尿系的炎症、男性患者是否有前列腺肥大等,可以讓泌尿科的醫生檢查一下,採取對症治療。
臨床診斷
提示本病的早期體征有眨眼動作的減少,面部表情的缺乏,各種動作的減少,與姿勢反射的障礙.在疾病初期大約70%病例有震顫,但往往隨著疾病的進展震顫也會有所減弱.雖然偶爾僵直可能很輕微或甚至缺如,但如果只有震顫而不具備上述這些徵象,則應考慮其他的診斷,或有需要在以後再進行複查,因為如果病人的確患有帕金森病則陸續會出現新的體征.最常與帕金森病發生混淆的是原發性震顫(見上文震顫),但原發性震顫的病人面部表情正常,動作的速度也正常,而且無步態障礙.而且原發性震顫是動作性震顫,不是在帕金森病中最常見的靜止性震顫.自發性動作有所減少,伴有因風濕性關節炎引起的小步步態,輕度抑鬱或痴呆的老年人與帕金森病病人的區別可能比較困難.繼發性帕金森症候群的病因可從病史中了解到。
輔助檢查
1.血清腎素活力降低、酪氨酸含量減少;黑質和紋狀體內NE、5-HT含量減少,谷氨酸脫羧酶(GAD)活性較對照組降低50%。
2.CSF中GABA下降,CSF中DA和5-HT的代謝產物HVA含量明顯減少。
3.生化檢測 放免法檢測CSF生長抑素含量降低。尿中DA及其代謝產物3-甲氧酪胺、5-HT和腎上腺素、NE也減少。
4.CT、MRI影像表現 由於帕金森病是一種中樞神經系統退性變疾病,病理變化主要在黑質、紋狀體、蒼白球、尾狀核以及大腦皮質等處,所以,CT影像表現,除具有普遍性腦萎縮外,有時可見基底節鈣化。MRI除能顯示腦室擴大等腦萎縮表現外,T2加權像在基底節區和腦白質內常有多發高信號斑點存在。
5.SPECT影像表現
鑒別診斷
1. 腦炎後帕金森症候群:
通常所說的昏睡性腦炎所致帕金森症候群,已近70年未見報導,因此該腦炎所致腦炎後帕金森症候群也隨之消失。近年報導病毒性腦炎患者可有帕金森樣症状,但本病有明顯感染症状,可伴有顱神經麻痹、肢體癱瘓、抽搐、昏迷等神經系統損害的症征,腦脊液可有細胞數輕~中度增高、蛋白增高、糖減低等。病情緩解後其帕金森樣症状隨之緩解,可與帕金森病鑒別。
2. 肝豆狀核變性:
隱性遺傳性疾病、約1/3有家族史,青少年發病、可有肢體肌張力增高、震顫、面具樣臉、扭轉痙攣等錐體外系症状。具有肝臟損害,角膜K-F環及血清銅藍蛋白降低等特徵性表現。可與帕金森病鑒別。
3. 特發性震顫:
屬顯性遺傳病,表現為頭、下頜、 肢體不自主震顫,震顫頻率可高可低,高頻率者甚似甲狀腺功能亢進;低頻者甚似帕金森震顫。本病無運動減少、肌張力增高,及姿勢反射障礙,並於飲酒後消失、心得安治療有效等可與原發性帕金森病鑒別。
4. 進行性核上性麻痹:
本病也多發於中老年,臨床症状可有肌強直、震顫等錐體外系症状。但本病有突出的眼球凝視障礙、肌強直以軀幹為重、肢體肌肉受累輕而較好的保持了肢體的靈活性、頸部伸肌張力增高致頸項過伸與帕金森病頸項屈曲顯然不同,均可與帕金森病鑒別。
5. Shy_Drager症候群:
臨床常有錐體外系症状,但因有突出的植物神經症状,如:暈厥、直立性低血壓、性功能及膀胱功能障礙,左旋多巴製劑治療無效等,可與帕金森病鑒別。
6. 藥物性帕金森症候群:
過量服用利血平、氯丙嗪、氟哌啶醇及其他抗抑鬱藥物均可引起錐體外系症状,因有明顯的服藥史、並於停藥後減輕可資鑒別。
帕金森的併發症
1、損傷是帕金森病不可忽視的併發症。隨著病情的發展,震顫、僵直、協調功能障礙,會逐漸累及運動功能,腳下遇到障礙物時容易跌跤甚至可發生骨折等損傷。冬天結冰及雨天濕滑的路面,廁所及浴室潮濕光滑的瓷磚地板,對於動作遲鈍、步履不穩的帕金森病病人都是危險的場所,要格外小心,避免摔跌。
2、常並發心理障礙和智能減損,尤多見於晚期病人。帕金森病表現的肢體震顫、僵直、動作笨拙以及缺乏面部表情而呈現的面具臉,兼之說話含混不清,語調單一,音量降低,流口水等,使病人感到有失大雅,心理上常有自卑感,不願參加社會活動,不去公共場所,疏於人際交往。在治療中及疾病發展過程中,還可見到失眠、焦慮、抑鬱、痴呆等。
3、由於植物神經功能障礙,導致消化系統併發症的發生。表現為:①營養障礙和水電解質 紊亂,與吞咽困難、飲食減少、液體補充不足有關。吞咽困難是因為咽部肌肉的協調動作發生障礙,咀嚼的速度減慢,其結果是進食緩慢而更長時間地咀嚼,使食物在口腔和咽喉部堆積;如進食過快則可導致噎塞和嗆咳。②食管擴張,假憩室形成,食管擴約肌功能不良,胸骨後有燒灼感。放射學證明有胃、食管返流。③胃排空延遲,有人統計約佔55%,表現為餐後飽脹、噁心、嘔吐。④小腸運動功能不良,由此產生腹脹感。放射學檢查提示小腸擴張。⑤結腸功能不良,主要表現為便秘,其高發生率(50%~67%)和頑固性給病人帶來痛苦,使醫生治療棘手。消化系統的各種併發症有其相同的病理生理基礎,都是由於胃腸平滑肌過度緊張,運動緩慢,相互協調不良所致。
4、感染是對帕金森病構成威脅的併發症。一般的呼吸道感染、發熱都會使本病症狀加重。病人由於免疫功能低下,感冒經常發生,也容易罹患支氣管炎、肺炎、胃腸炎等,晚期臥床的病人,完全喪失生活自理能力,不能獨立起坐,甚則不能自行翻身,兼之營養不良,皮膚受壓,常致褥瘡。墜積性肺炎、吸入性肺炎、心功能衰竭是晚期病人常見的併發症,最終可以導致死亡。尿頻也常成為帕金森病人求醫的原因,尤其夜間尿頻給病人帶來不少麻煩。男性病人常合併前列腺肥大,可導致排尿困難。女性病人因護理不周,尿便浸漬等,可造成泌尿系統反覆感染直至腎功能損害。感染、敗血症是導致本病晚期死亡的重要原因。
5、肢體攣縮、畸形、關節僵硬等主要見於本病的晚期。故對早、中期病人應鼓勵其多運動,為晚期病人多做被動活動,以延緩肢體併發症。
治療
治療方法的差異
多年臨床觀察結果表明,採取不同的治療行為,帕金森病患者病情的變化差異十分顯著:
1.在發病早期就開始接受合理治療的患者,絕大多數能夠延緩病情的發展,病情相對穩定,生活基本能夠自理。
2.雖然治療,但時常中斷的患者,大多不能很好地控制病情,病情會出現反覆及不同程度加重。
3.發展到晚期才開始治療的患者,病情往往已很嚴重,現有的治療手段對改善病症也很有限,患者通常會出現明顯的殘障。
帕金森的西醫治療
早期治療
PD早期黑質-紋狀體系統存留的DA神經元可代償地增加DA合成,推薦採用理療(按摩、水療)和體育療法(關節活動、步行、平衡及語言鍛煉、面部表情肌操練)等,爭取患者家屬配合,鼓勵患者多主動運動,盡量推遲藥物治療時間。若疾病影響患者日常生活和工作,需藥物治療。
藥物治療
PD目前仍以藥物治療為主,恢復紋狀體DA與Ach遞質系統平衡,應用抗膽鹼能和改善DA遞質功能藥物,改善症状,不能阻止病情發展。
用藥原則:①從小劑量開始,緩慢遞增,盡量用較小劑量取得滿意療效;②治療方案個體化,根據患者年齡、症状類型和程度、就業情況、藥物價格和經濟承受能力等選擇藥物;③不應盲目加用藥物,不宜突然停藥,需終生服用;④PD藥物治療複雜,近年來推出的輔助藥物DR激動藥、MAO-B抑制劑、兒茶酚-氧位-甲基轉移酶(COMT)等,與復方多巴合用可增強療效、減輕症状波動、降低復方多巴劑量,單獨使用療效不理想,應權衡利弊,適當選擇聯合用藥。
(1)抗膽鹼能藥:對震顫和強直有效,對運動遲緩療效較差,適于震顫明顯年齡較輕患者。常用安坦(artane)1~2mg口服,3次/d;開馬君(kemadrin)2.5mg口服,3次/d,逐漸增至20~30mg/d。其他如苯甲托品(cogentin)、環戊丙醇(cycrimine)、安克痙(akineton)等,作用與安坦相似。副作用包括口乾、視物模糊、便秘和排尿困難,嚴重者有幻覺、妄想。青光眼及前列腺肥大患者禁用,可影響記憶功能,老年患者慎用。
(2)金剛烷胺(amantadine):促進DA在神經末梢釋放,阻止再攝取,並有抗膽鹼能作用,是谷氨酸拮抗藥,可能有神經保護作用,可輕度改善少動、強直和震顫等,早期可單獨或與安坦合用。起始劑量50mg,2~3次/d,1周後增至100mg,2~3次/d,一般不超過300mg/d,老年人不超過200mg/d。藥效可維持數月至1年。副作用較少,如不安、意識模糊、下肢網狀青斑、踝部水腫和心律失常等,腎功能不全、癲癇、嚴重胃潰瘍和肝病患者慎用,哺乳期婦女禁用。也可用其衍生物鹽酸美金剛烷(memantine hydrochloride)。
(3)左旋多巴(L-dopa)及復方左旋多巴:L-dopa是治療PD有效藥物或金指標。作為DA前體可透過血腦屏障,被腦DA能神經元攝取後脫羧變為DA,改善症状,對運動減少有特殊療效。由於95%以上的L-dopa在外周脫羧成為DA,僅約1%通過BBB進入腦內,為減少外周副作用,增強療效,多用L-dopa與外周多巴脫羧酶抑制劑(DCI)按4∶1製成的復方製劑(復方L-dopa),用量較L-dopa減少3/4。
復方L-dopa劑型:包括標準片、控釋片、水溶片等。標準片如美多巴(madopar)和帕金寧(sinemet):①Madopar由L-dopa與苄絲肼按4∶1組成,美多巴250為L-dopa 200mg+苄絲肼50mg,美多巴125為L-dopa100mg+苄絲肼25mg;國產多巴絲肼膠囊成分與美多巴相同;②帕金寧(Sinemet 250和Sinemet 125)由L-dopa與卡別多巴按4∶1組成。
控釋劑包括兩種:①息寧控釋片(sinemet CR):L-dopa 200mg+卡別多巴50mg,製劑中加用單層分子基質結構,藥物不斷溶釋,達到緩釋效果,口服後120~150min達到血漿峰值濃度;片中間有刻痕,可分為半片服用,保持緩釋特性;②美多巴液體動力平衡系統(Madopar-HBS):L-dopa 100mg+苄絲肼25mg及特殊賦形劑組成,膠囊溶解時藥物基質表面形成水化層,通過彌散作用逐漸釋放。
水溶片有彌散型美多巴(madopar dispersible),劑量為125mg,由L-dopa 100mg+苄絲肼25mg組成。其特點易在水中溶解,便於口服,吸收迅速,很快達到治療閾值濃度,使處於「關閉」狀態的PD患者在短時間內(10min左右)迅速改善症状,且作用維持時間與標準片基本相同。該劑型適用於有吞咽障礙或置鼻飼管、清晨運動不能、「開」期延遲、下午「關」期延長、劑末肌張力障礙的PD患者。
用藥時機:何時開始復方L-dopa治療尚有爭議,長期用藥會產生療效減退、症状波動及運動障礙等併發症。一般應根據患者年齡、工作性質、疾病類型等決定用藥。年輕患者可適當推遲使用,早期盡量用其他抗PD藥,患者因職業要求不得不用L-dopa時應與其他藥物合用,減少復方L-dopa劑量。年老患者可早期選用L-dopa,因發生運動併發症機會相對較少,對合併用藥耐受性差。
用藥方法:從小劑量開始,根據病情逐漸增量,用最低有效量維持。①標準片:復方L-dopa開始用62.5mg(1/4片),2~3次/d,根據需要逐漸增至125mg,3~4次/d;最大劑量不超過250mg,3~4次/d;空腹(餐前1h或餐後2h)用藥療效好;②控釋片:優點是減少服藥次數,有效血藥濃度穩定,作用時間長,可控制症状波動;缺點是生物利用度較低,起效緩慢,標準片轉換成為控釋片時每天劑量應相應增加並提前服用;適於伴症状波動或早期輕症患者;③水溶片:易在水中溶解,吸收迅速,10min起效,作用維持時間與標準片相同,適於吞咽障礙、清晨運動不能、「開關」現象和劑末肌張力障礙患者。
副作用:周圍性副作用常見噁心、嘔吐、低血壓和心律失常(偶見)等,用藥後可逐漸適應,餐後服藥、加用嗎叮啉可減輕消化道症状。中樞性副作用包括症状波動、運動障礙和精神症状等,症状波動和運動障礙是常見的遠期併發症,多在用藥4~5年後出現。閉角型青光眼、精神病患者禁用。
(4)DA受體激動藥:DA包括五種類型受體,D1R和D2R亞型與PD治療關係密切。DR激動藥共同作用特點是:①直接刺激紋狀體突觸後DR,不依賴於DDC將L-dopa轉化為DA發揮效應;②血漿半衰期(較復方多巴)長;③可能對黑質DA能神經元有保護作用。早期DR激動藥與復方多巴合用,不僅能提高療效,減少復方多巴用量,且可減少或避免症状波動或運動障礙發生。
適應證:PD後期患者用復方多巴治療產生症状波動或運動障礙,加用DR激動藥可減輕或消除症状,減少復方多巴用量。疾病後期因黑質紋狀體DA能系統缺乏DDC,不能把外源性L-dopa脫羧轉化為DA,用復方多巴完全無效,用DR激動藥可能有效。單用DA受體激動藥療效不佳,一般主張與復方L-dopa合用,發病年齡輕的早期患者可單獨應用。應從小劑量開始,漸增量至獲得滿意療效而不出現副作用。副作用與復方L-dopa相似,症状波動和運動障礙發生率低,體位性低血壓和精神症状發生率較高。
常用製劑:主要是溴隱亭、培高利特。①溴隱亭(bromocriptine):激活D2受體,開始0.625mg/d,每隔3~5天增加0.625mg,通常治療劑量7.5~15mg/d,分3次服;副作用與左旋多巴類似,錯覺和幻覺常見,精神病史患者禁用,相對禁忌證包括近期心肌梗死、嚴重周圍血管病和活動性消化性潰瘍等;②培高利特(pergolide):激活D1和D2兩類受體,開始0.025mg/d,每隔5天增加0.025mg,一般有效劑量0.375~1.5mg/d,最大不超過2.0mg/d,1~3h達血漿峰值濃度,半衰期較長(平均30h),較溴隱亭抗PD作用稍強,作用時間亦長,溴隱亭治療無效時改用培高利特可能有效;③泰舒達緩釋片(trastal SR):化學成分為吡貝地爾,是選擇性D2/D3多巴胺受體激動藥,劑量為150~250mg/d,對中腦-皮質和邊緣葉通路D3R有激動效應,改善震顫作用明顯,對強直和少動也有作用;④麥角乙脲(lisuride):具有較強選擇性D2R激動作用,對D1R作用很弱,從小劑量開始,0.05~0.1mg/d,逐漸增量,平均有效劑量為2.4~4.8mg/d;按作用-劑量比,作用較溴隱亭強10~20倍,半衰期短(平均2.2h),作用時間短,為水溶性,可靜脈或皮下輸注泵應用,用於復方多巴治療出現明顯「開-關」現象;⑤阿朴嗎啡(apomorphine):D1和D2R激動藥,可顯著減少「關期」狀態,對症状波動,尤其「開-關」現象和肌張力障礙有明顯療效,採取筆式注射法給藥後5~15min起效,有效作用時間60min,每次給藥0.5~2mg,每天可用多次,攜帶型微泵皮下持續灌注法可使患者每天保持良好運動功能;也可經鼻腔給藥,但長期用藥可刺激鼻黏膜;⑥卡麥角林(cabaser):是所有DR激動藥中半衰期最長(70h),作用時間最長,適於PD後期長期應用復方多巴產生症状波動和運動障礙患者,有效劑量2~10mg/d,平均4mg/d,只需1次/d,較方便;⑦普拉克索(Pramipexole,0.125mg,3次/d,逐漸加量至0.5~1.0mg,3次/d)和羅吡尼洛(Ropinirole,0.25mg,3次/d,逐漸加量至2~4mg,3次/d),均非麥角衍生物,無麥角副作用,用於早期或進展期PD,症状波動和運動障礙發生率低,常見意識模糊、幻覺及直立性低血壓。
(5)單胺氧化酶B(MAO-B)抑制劑:抑制神經元內DA分解,增加腦內DA含量。合用復方L-dopa有協同作用,減少L-dopa約1/4用量,延緩開關現象,有神經保護作用。常用思吉寧(selegiline)即丙炔苯丙胺(deprenyl)2.5~5mg,2次/d,宜早、午服用,傍晚服用可引起失眠。副作用有口乾、胃納少和體位性低血壓等,胃潰瘍患者慎用。Lazabemide(Ro19-6327)亦系MAO-B抑制劑,目前臨床應用報導不多。
有學者主張此類藥與維生素E合用,稱DATA-TOP方案(deprenyl and tocopherol antioxidation therapy of Parkinsonism),作為神經保護劑用於早期輕症患者,可能延緩疾病進展。維生素E是天然自由基清除劑,有抗氧化作用,PD早期尤其未經治療患者用維生素E與丙炔苯丙胺可能減緩黑質細胞變性、延緩疾病進展。近年國外有人提倡丙炔苯丙胺2.5mg口服,1次/d,漸加至2.5mg,2次/d,再加至5mg,2次/d;同時服用維生素E 2000U,1次/d。但目前對此方案仍有爭議,須繼續觀察評價。
(6)兒茶酚-氧位-甲基轉移酶(COMT)抑制劑:抑制L-dopa外周代謝,維持L-dopa穩定血漿濃度,加速通過BBB,阻止腦膠質細胞內DA降解,增加腦內DA含量。與美多巴或息寧合用增強後者療效,減少症状波動反應,單獨使用無效。副作用可有腹瀉、頭痛、多汗、口乾、轉氨酶升高、腹痛、尿色變淺等,用藥期間須監測肝功能。
常用製劑:①托可朋(tolcapone):亦名答是美(tasmar),100~200mg口服,3次/d,副作用有腹瀉、意識模糊、運動障礙和轉氨酶升高等,應注意肝臟毒副作用;具有周圍和中樞COMT抑制作用,臨床試驗顯示,應用復方多巴療效減退的69例PD加用托可朋100~150mg,3次/d,療程6個月,有效率98.5%,無明顯毒副作用,可與復方多巴和MAO-B抑制劑合用;②恩他卡朋(entacapone):亦名珂丹(comtan),是周圍COMT抑制劑,100~200mg口服,5次/d為宜,與托可朋不同的是迄今無嚴重肝功能損害報導。
(7)興奮性胺基酸(EAA)受體拮抗藥及釋放抑制劑:EAA可損害黑質細胞,抑制劑有神經保護作用,可增強L-dopa作用。但目前尚無臨床有效治療的報導。
(8)鐵螯合劑:PD患者黑質Fe2 濃度明顯增加,鐵蛋白含量顯著減少。給予鐵螯合劑可降低Fe2 濃度,減少氧化反應。目前常用21-氨基類固醇(21-aminosteroide),可通過血腦屏障與Fe2 結合,抑制脂質過氧化,對黑質細胞有保護效應。
(9)神經營養因子(neurotrophic factors):對神經元發育、分化及存活起重要作用,選擇性作用於DA能神經元的神經營養因子有助於PD防治。神經營養因子包括酸性及鹼性成纖維細胞生長因子(aFGF、bFGF)、上皮生長因子(EGF)、睫狀神經營養因子(CNTF)、腦源性神經營養因子(BDNF)、膠質細胞源性神經營養因子(GDNF)及Neurturin等。GDNF和Neurturin對中腦DA能神經元特異性強。
(10)中藥或針灸對PD治療有一定的輔佐作用,需與西藥合用,單用療效不理想。
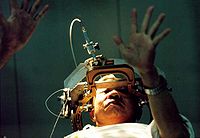
外科治療
立體定向手術治療PD始於20世紀40年代,近年來隨著微電極引導定向技術的發展,利用微電極記錄和分析細胞放電特徵,可精確定位引起震顫和肌強直的神經元,達到細胞功能定位,可顯著提高手術療效和安全性。手術可糾正基底節過高的抑制性輸出,適應證為藥物治療失效、不能耐受或出現運動障礙(異動症)的患者,年齡較輕,症状以震顫、強直為主且偏於一側者效果較好,術後仍需用藥物治療。
(1)蒼白球毀損術(pallidotomy):近年來隨著微電極引導定向技術的發展,使定位精確度達到0.1mm,進入到細胞水平,達到準確功能定位,確定電極與蒼白球各結構及相鄰視束和內囊的關係,有助於尋找引起震顫和肌張力增高的神經元。用此法確定靶點,手術效果較好,改善PD運動症状,尤其運動遲緩,很少產生視覺受損等併發症。
(2)丘腦毀損術:是用立體定向手術破壞一側丘腦腹外側核、豆狀襻及丘腦底核,對PD的震顫療效較好,最佳適應證是單側嚴重震顫。單側丘腦毀損術併發症較少,雙側毀損術可引起言語障礙、吞咽困難及精神障礙等併發症,不主張採用。
(3)深部腦刺激療法(deep brain stimulation,DBS):是將高頻微電極刺激裝置植入PD患者手術靶點,高頻電刺激產生的電壓和頻率高於病變神經元產生的電壓和頻率,從而起到抑制作用。DBS優點是定位準確、損傷範圍小、併發症少、安全性高和療效持久等,缺點是費用昂貴。美國FDA已批准臨床應用DBS治療PD。
(4)立體定向放射治療(γ-刀,X-刀):利用立體定向原理,用計算機精確計算靶點,一次大劑量窄束高能射線精確地聚焦破壞靶點,靶點外正常組織受劑量極小。射線包括60鈷(60CO)產生的γ-射線(γ-刀)及直線加速器產生的X射線(X-刀)。適應證與立體定向毀損術相同,但療效不如後者,副作用較多,目前不推薦使用。
4.細胞移植及基因治療 細胞移植是將自體腎上腺髓質或異體胚胎中腦黑質細胞移植到患者紋狀體,糾正DA遞質缺乏,改善PD運動症状。酪氨酸羥化酶(TH)和神經營養因子基因治療正在探索中,是有前景的新療法。將外源TH基因通過exvivo或invivo途徑導入動物或患者腦內,導入的基因經轉錄、翻譯合成TH,促使形成DA。目前存在供體來源困難、遠期療效不肯定及免疫排斥等問題。
5.康復治療 對患者進行語言、進食、行走及各種日常生活訓練和指導,對改善生活質量十分重要。晚期臥床者應加強護理,減少併發症發生。康復包括語音語調訓練,面肌鍛煉,手部、四肢及軀幹鍛煉,鬆弛呼吸肌鍛煉,步態及平衡鍛煉,姿勢恢復鍛煉等。
物理治療
重要的是要讓病人儘可能保持各項活動.在疾病早期,病人應儘力完成各項日常活動.隨著運動功能障礙的加重,正規的體療與理療有助於維持或重建軀體的調整能力,可使病人學會一些適應性的策略.由於疾病本身,治療用藥以及活動的減少都能造成便秘,病人應保持高纖維素的飲食與充分的進食.應用歐車前(子)(psyllium)與潤濕性瀉藥(如多庫酯鈉)有助.
中醫治療
本病的臨床表現與中醫學中「顫證」、「顫振」、「振掉」、「內風」、「痙病」等病證的描述相似。《素問.至真要大論》「諸風掉眩,皆屬於肝,」是對本病的早期認識。其中「掉」即含有「震顫」之意。《華氏中藏經.論筋痹第三十七》說:「行步奔急,淫邪傷肝,肝失其氣……則使人筋急而不能行步舒緩也。」所謂行走奔急,不能舒緩,恰如帕金森病的慌張步態。隋.巢元方撰《諸病源候論》,其在「風四肢拘攣不得屈伸候」、「五指筋攣不能屈伸候」中進一步解釋了強直和姿勢障礙的病機。唐.孫思邈《備急千金要方》中記載有「金牙酒」治療「積年八風五痙,舉身蟬曳,不得轉側,行步跛蹙,不能收攝」等病,這些特徵很像帕金森病所出現的動作遲緩和步態障礙。金元.《儒門事親》記載一病案:「新寨馬叟,年五十九。……病大發,則手足顫掉,不能持物,食則令人代哺……。」根據病案所載,老年男性,病因不明,如以精神創傷為誘因,慢性進行性震顫伴隨意運動障礙和憂鬱色彩者,考慮為帕金森病的可能性最大。至明代,對顫證的認識進一步深化,這一時期的許多醫家對顫證的病名、病因病機、辨證論治等方面均有較系統的論述。張景岳《類經.疾病類(一)》註:「掉,搖也。……,風主動搖,木之化也,故屬於肝。」樓英《醫學綱目》提出邪實為患,風、火、痰致病觀點。孫一奎尤為傑出,他在《赤水玄珠》中首次把震顫為主要臨床表現的疾病統一命名為顫振證,強調顫振不能隨意控制,指出:「顫振者,人病手足搖動,如抖擻之狀,筋脈約束不住,而莫能任持,風之象也。」還對顫振的發病年齡和預後,也有科學論斷,說:「此病壯年鮮有,中年以後乃有之,老年尤多,夫年老陰血不足,少水不能制腎火,極為難治。」王肯堂《證治準繩》中總結出一套因人施治的治療顫振的方劑,代表方是治老人虛顫的定振丸(天麻、秦艽、全蠍、細辛、熟地黃、生地黃、當歸、川芎、芍藥、防風、荊芥、白朮、黃芪、威靈仙)。迨至清代,張璐《張氏醫通》系統總結前人的經驗,結合個人臨床實踐,指出本證主要是風、火、痰、虛為患,同時還對顫證的相應脈象做了詳細論述。高鼓峰《醫宗己任編.顫振》說:「大抵氣血俱虛,不能榮養筋骨,故為之振搖,而不能主持也。」強調氣血虧虛是顫證的重要原因,並創造大補氣血法治療顫證,指出:「須大補氣血,人蔘養榮湯或加味人蔘養榮湯主之。」此法沿用至今,仍為治療顫證的有效方法之一。
從近20餘年的文獻報導中可以看出,中醫學者對本病的認識尚未統一,1991年11月經第三屆中華全國中醫學會老年腦病學術研討會上討論、論證並通過了「中醫老年顫證診斷和療效評定標準」試行草案,確定統一病名為老年顫證,將本病的研究向客觀化推進了一步。
預後
PD是慢性進展性疾病,目前無根治方法,多數患者發病數年仍能繼續工作,也可迅速發展致殘。疾病晚期可因嚴重肌強直和全身僵硬,終至臥床不起。死因常為肺炎、骨折等併發症。
帕金森病的預防
迄今,帕金森病確切病因尚不十分清楚,因此,預防措施缺乏精確的針對性。但許多研究已證實,本文上述諸多危險因素與中腦黑質多巴胺神經元變性、壞死存在著一定的因果關係,若能針對危險因素採取相應的預防措施,對預防帕金森病的發病和延緩病程進展肯定是有益的。
一級預防
(無病防病) 1、對有帕金森病家族史及有關基因攜帶者,有毒化學物品接觸者,均應視為高危人群,須密切監護隨訪,定期體檢,並加強健康教育,重視自我防護。
2、加大工農業生產環境保護的力度,減少有害氣體、污水、污物的排放,對有害作業人員應加強勞動防護。
3、改善廣大農村及城鎮的飲水設施,保護水資源,減少河水、庫水、塘水及井水的污染,保證廣大人民群眾能喝上安全衛生的飲用水。
5、重視老年病(高血壓、高血脂、高血糖、腦動脈硬化等)的防治,增強體質,延緩衰老,防止動脈粥樣硬化,對預防帕金森病均能起到一定的積極作用。
二級預防
(早發現、早診斷、早治療) 1、早期診斷。帕金森病的亞臨床期長,若能即早開展臨床前期診斷技術,如嗅覺機能障礙、PET掃描、粒線體DNA、多巴胺抗體、腦脊液化學、電生理等檢查,將亞臨床期帕金森病儘早發現,採用神經保護劑(如維生素E、SOD、谷胱甘肽及谷胱甘肽過氧化物酶、神經營養因子、塞利吉林)治療,可能會延緩整個臨床期的過程。
2、帕金森病早期,雖然黑質和紋狀體神經細胞減少,但多巴胺分泌卻代償性增加,此時腦內多巴胺含量並未明顯減少,稱代償期,一般不主張用藥物治療,可採用理療、醫療體育、太極拳、水療、按摩、氣功、針灸等治療,以維持日常一般工作和生活,盡量推遲抗震顫麻痹藥物應用的時間。但也有人主張早期應用小劑量左旋多巴以減少併發症,這要因人而異,擇優選用。 3、帕金森病失代償期應使用藥物治療。
三級預防
(延緩病情發展、防止病殘、改善生活質量) 1、積極進行非藥物如理療、體療、針灸、按摩等及中西醫藥物或手術等綜合治療,以延緩病情發展。
2、重視心理疏導安撫和精神關愛,保證充足睡眠,避免情緒緊張激動,以減少肌震顫加重的誘發因素。
3、積極鼓勵患者主動運動,如吃飯、穿衣、洗漱等。有語言障礙者,可對著鏡子努力大聲地練習發音。加強關節、肌力活動及勞作訓練,儘可能保持肢體運動功能,注意防止摔跤及肢體畸形殘廢。
4、長期臥床者,應加強生活護理,注意清潔衛生,勤翻身拍背,防止墜積性肺炎及褥瘡感染等併發症,帕金森病大部分死於肺部或其他系統如泌尿系統等的感染。注意飲食營養,必要時給予鼻飼,保持大小便通暢。以不斷增強體質,提高免疫功能,降低死亡率。
研究歷史
《震顫麻痹論文》1817年,英國一般科開業醫師詹姆士.帕金森在一篇名為《震顫麻痹論文》的論文(Essay on the Shaking Palsy)中描述了這些症状:行動遲緩、肌肉僵直、四肢顫抖、步伐拖曳、憂鬱及痴獃等。
1917年,維也納醫生馮伊考諾摩首次描述了流行性嗜眠性腦炎。
1918年-1926年間,大約1千500萬人流行性嗜眠性腦炎,也通稱睡病。這是一個重要的發現,因為生存的人當中,有約5百萬人最終患上了帕金森氏症。
1960年,Enhringer及Horniewicz從帕金森氏症患者的腦部解剖發現,在基底核的多巴胺濃度有減少的現象。
1982年,繼美國加州流行吸食海洛英成癮之後,爆發出帕金森氏症的流行。
1984年Langston, Ballard及Burns發現合成出來的假海洛英(MPTP)有毒,會選擇性的危害黑質腦細胞,使得多巴胺神經元的粒線體中毒死亡,並因此產生帕金森氏症。這類的患者情況接近最嚴重的帕金森氏症(手腳僵硬)。他們亦發現不論用吸食或注射海洛英,都形成MPTP毒素,甚至海洛英製造工廠或實驗室所產生大量漂浮在空氣中的物質,能透過呼吸系統進入人體而危害人體健康。另外一氧化碳中毒及重金屬如鎂中毒,亦可以破壞黑質腦細胞而產生帕金森氏症患者,亦有多發性大腦栓塞的病症,可能跟他們的基因遺傳體質有關(Gary,Poirier,1991)。
1990年,Lindvall和他的工作隊員將3~4個約8至9個星期大的胚胎中取出黑質體腦細胞並植入一個患有帕金森氏症的病人中。由於腦組織和免疫系統被腦血管障壁隔離,因此捐贈細胞者不需和接受者有任何血源關係。5個月後,病人的黑核細胞生產了足夠的多巴胺,這含量的多巴胺足夠讓病人自由行動。
患上帕金森氏症的名人
鄧小平
張光直
李堯棠(巴金)
弗朗西斯科.佛郎哥
阿道夫.希特勒
若望.保祿二世
穆罕默德.阿里
皮埃爾.特魯多
薩爾瓦多.達利
凱瑟琳.赫本
比利.葛理翰
哈利.S.杜魯門
道格拉斯.麥克阿瑟
米高.霍士(Michael J. Fox,好萊塢影星)
參看
- 治療帕金森的藥品列表
- 神經內科疾病
- 《神經病學》- 震顫麻痹
- 《常見中老年疾病防治》- 震顫麻痹
- 《自我調養巧治病》- 震顫麻痹
- 《老年百病防治》- 震顫麻痹
- 《家庭醫學百科·醫療康復篇》- 震顫麻痹
- 《默克家庭診療手冊》- 帕金森病
健康問答網關於帕金森病的相關提問
| Error: It's not possible to get http://www.wenda120.com/tags/1562/rss... |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 關於「帕金森病」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |