急性早幼粒細胞白血病
| A+醫學百科 >> 腫瘤 >> 急性早幼粒細胞白血病 |
急性早幼粒細胞白血病(acute promyelocytic leukemiaAPL)是急性髓細胞白血病(AML)的一種特殊類型,被FAB協作組定為急性髓細胞白血病M3型。
目錄 |
概述
急性早幼粒細胞白血病(acute promyelocytic leukemiaAPL)是急性髓細胞白血病(AML)的一種特殊類型,被FAB協作組定為急性髓細胞白血病M3型。
造血組織的惡性疾病。其特點是骨髓及其他造血組織中有大量白血病細胞無限制地增生,並進入外周血液,而正常血細胞的製造被明顯抑制,該病居年輕人惡性疾病中的首位,病因至今仍不完全清楚,病毒可能是主要的致病因子,但還有許多因素如放射、化學毒物(苯等)或藥物、遺傳素質等可能是致病的輔因子。根據白血病細胞不成熟的程度和白血病的自然病程,分為急性和慢性兩大類。
分型
發病急,骨髓和外周血中主要是原始細胞,若不治療病人常於半年內死亡。根據白血病細胞的類型,臨床上又分為急性淋巴細胞性白血病(ALL) 和急性非淋巴細胞性白血病(ANLL)兩大類,每類又有幾型。目前國內外通用的分型如下:
ANLL分為7型
即粒細胞白血病未分化型(M1) 、 粒細胞白血病部分分化型 (M2)、 早幼粒細胞型(M3)、粒-單核細胞型(M4)、單核細胞型(M5)、紅白血病(M6)、巨核細胞型(M7);
ALL分為L1 、L2和L3型
近年來又根據細胞的免疫學特點分為T、 B、前B、普通型和未分化型。病人常突然發生貧血、感染和出血及肝脾、淋巴結腫大和胸骨壓痛,血常規和骨髓檢查可確定診斷。近年來療效有較大提高,有些病人已治癒,除輸血和抗感染等對症支持治療外,聯合化療是當前主要的治療方法,由於新的有效化療藥物的不斷湧現和聯合用藥方法的改進,完全緩解率已達80%以上;另外分化誘導劑維甲酸等可使早幼粒白血病細胞分化誘導成熟,療效顯著,是近年來的重要發現;骨髓移植可獲痊癒,但仍有一些問題尚待解決。
流行病學
急性早幼粒細胞白血病在臨床上並不少見,病人常較年青年齡中位數30~38歲10歲以下者罕見據中國完全統計M3的發病率高於西方國家的10%左右,占同期AML的18.7%有的地區如東北油田M3的發病率在AML中可能高達20%~30%,甚至更高,國外資料顯示,歐洲中南美洲的拉丁裔民族發病率較高APL約佔成人原發性AML的10%~15%,不過也可存在年齡和種族的差異。
病因
原發性APL的病因目前尚未完全清楚繼發者常見於應用化療和(或)放療的腫瘤患者,也有應用烷化劑和拓撲異構酶Ⅱ抑制劑引起APL的報導繼發性APL的預後較好,其對治療的反應和長期生存率與原發者相近,但與化療相關的AML明顯不同。
特點
① 早幼粒細胞漿內充滿異常顆粒;
② 常伴有出血傾向發生率達72%~94%,嚴重者出現DIC;
③ 90%的患者出現特異性染色體t(15;17)(q22;q21)改變;
④ 對化療敏感,但早期死亡率高,尤其在甲細胞毒細胞藥物化療時,約有10%~20%患者死於時期出血;
⑥ 持續緩解時間較長。以往APL的治療效果很差預後兇險,多因並發性彌散性血管內凝血(DIC)或原發性纖維蛋白溶解導致嚴重出血,而早期死亡近年來隨著對APL細胞生物學的特性認識的不斷提高和治療方法改進,使治療結果和預後得到了很大的改善早期死亡率明顯下降
發病機制
APL是白血病中對誘導分化治療反應較好的一種類型,這與APL細胞中表達的維A酸受體(RARα)融合蛋白誘導的染色質的改變有關。已報導的APL的5種染色體易位均累及17號染色體上的RARα基因。該基因全長39398bp包含9個外顯子和8個內含子。t(15;17)易位見於絕大多數APL患者,維A酸受體α基因與15號染色體的早幼粒細胞白血病(PML)基因形成PML-RARα融合基因該融合基因編碼的蛋白具有不同於正常RARα等位基因編碼的野生型維A酸受體的功能RARα基因位於染色體17長臂2l區帶其功能是核激素受體。維A酸結合在RAR受體元件上轉錄調節許多基因。PML是一核蛋白從氨基端到羧基端包括脯氨酸豐富區、核小體定位所需的胱氨酸豐富區形成同/異二聚體所需的螺旋環螺旋結構核定位信號NLS以及絲氨酸、脯氨酸豐富區。PML正常位於一個稱為POD(PML oncogenic domain)的結構(又稱核小體多蛋白核器)中。POD在核中呈斑點狀數目15~20個PML的功能尚未完全闡明。近來的研究認為PML通過轉錄共激活作用,具有抑制腫瘤生長的活性,在多種凋亡途徑中PML也可能起重要作用。在M3型AML(急性早幼粒細胞白血病)中,17號染色體上的RARα與15號染色體上的PML相互易位即發生t(15;17)(q22;q21)PML和RARα的相互易位造成以下後果:
① PML-RARα融合蛋白通過顯性負抑制作用抑制早幼粒細胞分化成熟;
② PML去定位形成上百個細小顆粒分布在核及胞質中使POD的結構破壞,PML的正常抑制增殖和促凋亡功能發生障礙導致細胞增殖,凋亡減少;
③ RARα正常時能與轉錄共抑制複合物(N-CoR/Sin3a/HDAC-1)(N-CoR=核受體共抑制物,HDAC=組蛋白去乙醯化酶)結合在生理劑量的維A酸作用下RARα可以與共抑制複合物解離,起轉錄激活作用,即激活所調節的靶基因PML-RARα可促進RARα與共抑制複合物的結合抑制RARα所調節的靶基因抑制了早幼粒細胞的分化成熟並使其增殖引起M3型AML在治療劑量下ATRA可降解PML-RARα此外ATRA還可使共抑制複合物與RARα分離進而募集共激活(coactivators)複合物,包括CBP/P300、P/CAF、NcoA-1/SRC-1P/CIF等蛋白其中CBF/P300和P/CAF有強烈的組蛋白乙醯化酶活性,使組蛋白乙醯化組蛋白乙醯化後,轉錄激活靶基因的功能恢復早幼粒細胞乃分化成熟。
1%~2%的APL有變異型t(11;17)(q23;q21)使11號染色體上的早幼粒細胞白血病鋅指基因(PLZF)與位於17號染色體上的RARα基因融合。迄今報導的所有患者體內同時表達PLZF-RARα和RARα-PLZF兩種融合蛋白提示t(11;17)(q23;q21)APL發病可能需要RARot-PLZF融合蛋白髮揮相應的作用t(11;17)(q23;q21)APL對ATRA不敏感更少見的變異性染色體易位有t(5;17)(q35;q21)導致NPM(nucleophosmin)與RARα基因融合;t(11;17)(q13;q21)產生NuMA-RARα融合基因;dup(17)(q21.3-q23)產生STATSb-RARα融合基因。前2種易位的患者對ATRA敏感,但ATRA對STAT5b-RARα融合基因陽性患者無效。
APL融合基因的致白血病作用已在轉基因動物模型得到證實。hMRP8或人組織蛋白酶G(human cathepsin G)微基因調控下表達PML-RARα的hCG-PML-RARα轉基因小鼠在出生後約1年發生APL樣白血病,而hCG-PLZF-RARα轉基因小鼠在出生後3~12個月發生慢性粒細胞白血病樣病變,伴骨髓內早幼粒細胞增多;而同時表達PLZF-RARα和RARα-PLZF的轉基因小鼠才發生類似人類的APL;NPM-RARα轉基因小鼠在出生後1年出現典型APL或慢性粒細胞白血病樣病變。
臨床表現
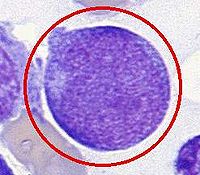
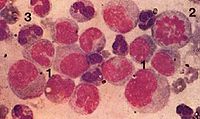
早幼粒細胞白血病(M3)骨髓片
急性早幼粒細胞白血病的臨床表現正常骨髓造血功能衰竭相關的表現如貧血、出血感染;白血病細胞的浸潤有關的表現如肝脾和淋巴結腫大骨痛等除了這些白血病具有的一般白血病表現外出血傾向是其主要的臨床特點,有10%~20%的患者死於早期出血,瀰漫性血管內凝血(DIC)的發生率高大約60%的患者發生DIC。
併發症
感染
是最常見的併發症 包括細菌病毒真菌感染主要表現為發熱,感染的部位常見於口腔肺部皮膚嚴重者可出現敗血症、感染中毒性休克。
DIC是APL
最重要的併發症 發生率高大約60%的患者發生。近年隨著應用甲酸和砷劑,DIC的發生已明顯減低。
高白細胞症
在應用維A酸治療過程中會合併高白細胞症,維A酸症候群,可同時給予羥基脲小劑量Ara-C或減量的AADA方案治療。
診斷
根據FAB的形態學診斷標準確立診斷。按FAB分型急性早幼粒細胞白血病(acute promyelocytic leukemia,APL)又稱AML-M3型。其典型特徵有:
① 骨髓形態為胞質含粗大顆粒和Auer小體(也有微顆粒變異型)的異常早幼粒細胞增生;
② 臨床常有嚴重出血且易合併DIC和纖維蛋白溶解;
③ 90%的患者顯示特異性染色體異位t(15;17);
④ 化療敏感(化療耐藥發生率<5%),緩解生存期長但早期死亡率高。
鑒別診斷: 主要與其他類型的白血病鑒別其鑒別要點根據細胞形態學、細胞免疫學檢查細胞遺傳學檢查,一般不難鑒別。
檢查
基本檢查
1、外周血 典型的血象顯示貧血,白細胞數量的變化,並可見幼稚細胞,血小板減少。
2、骨髓像 以異常的顆粒增多的早幼粒細胞增生為主>30%,多數>50%,且細胞形態較一致,原始細胞以下
各階段細胞較少,細胞核形態多不規則有內外漿,外漿中無顆粒,內漿中有大小不均的顆粒根據顆粒的大小可分為:
M3a(粗顆粒型):胞質中充滿粗大的嗜苯胺藍顆粒,且密集融合分布,顆粒也可以覆蓋在校上。
M3b(細顆粒型):胞質中嗜苯胺藍顆粒細小,而密集分布。
3、細胞免疫學檢查 蛋白標CD33,13(HLA-Dr陰性)。
4、細胞遺傳學檢查 染色體異常,t(15;17)(q22;q21)。
5、出凝血時間、3P試驗、纖維蛋白原含量、纖溶酶原含量及活性ATPP(活化部分凝血活酶時間)、PT(凝血酶原時間)。
其它輔助檢查
根據病情、臨床表現、症状、體征選擇X線CT、MRI、B超心電圖等檢查。
治療
1、APL 是急性白血病中病情十分兇險的一種類型,其出血症状是十分常見的,發生率達72%~94%,明顯高於其他急性白血病,往往是彌散性血管內血(DIC)的表現尤其是在化療過程中DIC可以加重,常致患者早期死亡由於APL有其獨特的染色體異常即t(15;17),產生融合基因PML-RARα及其編碼的蛋白故其治療與其他AML有所不同隨著近階段對APL的研究進展使得其治療成為白血病治療最成功的範例之一早在20世紀70年代就已明確,APL對蒽環要藥物非常敏感,單獨應用化療的治療效果優於AML的其他類型,維A酸(ATRA)和砷劑的出現使APL的療效發生了極大的改觀在誘導治療的同時,給予積極的支持治療也十分重要,包括抗感染輸血小板、輸血等。
誘導分化治療
在維A酸(ATRA)臨床應用之前體外實驗證實維A酸(ATRA)能誘導白血病細胞株(如HL-60細胞)和APL原代細胞分化。1986年中國學者在國際上首次使用全反式維A酸誘導分化治療APL並獲得了成功目前維A酸(ATRA)誘導分化療法主要用於APL,並已開始嘗試於其他類型的AML及一些實體瘤維A酸對腫瘤細胞的作用機制與化療藥物不同,它通過促進APL細胞的分化糾正出凝血機制的異常,避免化療所致的骨髓抑制和誘發DIC的可能,使白血病的治療出現了重大的突破,使APL的預後大為改觀。
① 維A酸(ATRA)的用法和療效:
A、一般劑量:維A酸(ATRA)治療APL的一般劑量為45mg/(m2.d)分次口服療程30~45天對初治APL患者,維A酸(ATRA)的CR率可達90%左右(表1)。
B、小劑量:小劑量維A酸(ATRA )15~25mg/(m2.d)分次口服治療APL以減輕維A酸的毒副反應結果表明小劑量治療可達到一般劑量的CR率。然而在降低維A酸(ATRA)毒副反應方面的報告不盡一致。Castaigne等分別以25mg/m2與15mg/m2 維A酸(ATRA)治療APL結果認為在療效、激發高白細胞症維A酸症候群和藥代動力學方面兩組之間無明顯差異。
② 誘導期治療方法的改進:一般主張在維A酸(ATRA)治療中合併化療,待白細胞已升至3×109/L以上應用化療,這樣既可防止維A酸症候群的發生又可提高CR率,延長CR期國內孟氏報導,服用維A酸(ATRA )15天後改用化療治療APL是安全的。歐洲協作組對93例白細胞數低於5×109/L的初發APL的研究顯示,先維A酸(ATRA後化療和維A酸(ATRA)+化療的兩組病人臨床完全緩解率無區別但維A酸(ATRA)+化療一組病人2年內的複發率顯著低於先維A酸(ATRA)後化療組。表明維A酸(ATRA)與化療同時使用更能發揮化療對維A酸( ATRA)的補充作用並降低複發率義大利協作組用維A酸(ATRA )45mg/m2誘導治療的第6~8天同時予DA 12mg/(m2.d),完全緩解率高達92%。另外有些病例單純應用ATRA不能控制病情,也可加用小量的阿糖胞苷(Ara-C)或減量的AADA方案。
單用維A酸(ATRA)誘導和維持治療患者的主要問題是早期複發,中位CR期僅5個月。此時產生ATRA耐藥和白血病複發的主要原因可能是長期使用維A酸(ATRA)使血漿中生成ATRA代謝酶,以致維A酸(ATRA)的血藥濃度下降不足以維持白血病細胞繼續分化成熟;或白血病細胞在維A酸(ATRA)誘導下合成ATRA結合蛋白從而阻止藥物進入細胞核發揮誘導分化作用不少作者發現在始終單用ATRA治療的緩解患者中大都PML-RARα融合基因表達持續陽性且其表達與白血病複發高度相關但若加用化療則可使PML-RARα表達轉陰患者的緩解生存期也顯著延長。因此儘管使用維A酸(ATRA)治療已經獲得高CR率,化療對APL的長期緩解乃至治癒依然是必不可少的。
然而誘導緩解治療採用維A酸(ATRA)也有助APL延長緩解。表2摘要介紹國外作者報導的APL治療效果:患者誘導緩解使用維A酸(ATRA)±化療,緩解後均用化療鞏固強化,結果顯示各家報導的EFS,凡在誘導化療時採用維A酸(ATRA)+化療組都明顯優於同期或歷史對照的單用化療組這說明維A酸(ATRA)能增加APL對化療的敏感性明顯減少本病複發兩者相輔相成。
③ 緩解後治療:維A酸(ATRA)聯合應用化療能顯著改善病人的預後上海血液病研究所對一組(70例)用DA或HA,維A酸(ATRA)巰嘌呤(6-MP)+甲氨蝶呤(MTX)序貫治療的回顧性研究表明,平均5年無病生存率為70%±6%另一項回顧性研究表明,64例聯合應用維A酸(ATRA)和化療的病人5年無病生存率為58.5%±10.4%,而另一組(47例)單用化療的病人只有26.7%±9.4%Tallman等開展的前瞻性研究也證實了這一點即誘導緩解和強化鞏固時都使用維A酸(ATRA)的病例療效好於單用化療者。在有效預防AT-RA症候群的基礎上聯合化療90%的初發病人都得到緩解而單用化療即使在初發病人緩解率也很難達到80%。法國Fenaux等報告一組54例APL用維A酸(ATRA)治療,CR率90%,以後用強化療鞏固,2年無事件生存(event free survival,EFS)率68%,生存率81%。日本成人白血病研究組於1995年報導109例APL予維A酸(ATRA)或維A酸(ATRA)加化療取得CR後(89%),予化療鞏固23個月的EFS為75%(66%~83%)取得CR的DFS為81%(7l%~91%)一般主張緩解後應該使用化療及維A酸交替應用的方案。
④ APL變異型治療:APL除有典型的t(15;17)易位外還有一種少見的變異型易位t(11;17)(q23;q21),該變異型易位佔APL的1%~2%它使RARα與另一轉錄因子PLZF(promyelocytic leukemia zincfinger)基因融合。t(11;17)的患者對ATRA誘導分化療法或化學療法反應均較差或無效其白血病細胞在體外培養時經ATRA處理不發生分化。該類患者對維A酸(ATRA)+G-CSF或維A酸(ATRA)+化療治療有效;另一種變異型易位t(11;17)(q13;q11)發生率更少累及的融合基因為NuMA- RARα該型ATRA治療有效。M3的另一變異型易位t(5;17)(q32;q21)累及5號染色體上的核磷酸蛋白(nucleophosmin,NPM)基因。形成NPM-RARα融合基因,這類患者維A酸(ATRA)治療有效。
⑤ 維A酸(ATRA)的副反應:包括口唇及皮膚乾燥(70%~90%)、頭痛(25%~40%)骨關節痛(15%~30%)肝功能受損和血脂增高(12%~30%)等。有2/3~3/4的患者發生不同程度的白細胞升高最嚴重的併發症是維A酸症候群和血栓形成前者表現為發熱、胸悶、呼吸困難水瀦留伴水腫、胸腔或心包積液高血壓、呼吸窘迫缺氧呼吸功能衰竭,少數腎功能衰竭。常發生在高白細胞的患者發生率10%~25%是致死原因。合用化療後這種嚴重併發症已降至5%~7%治療方法是大劑量地塞米松靜脈注射10mg/次2次/d共3~5天。
⑥ 治療機制:維A酸(ATRA)誘導分化治療APL的機制尚未完全闡明由於維A酸(ATRA)受體α、β、γ的發現以及它們結構與功能的進一步闡明,維A酸(ATRA)作用機制的研究,才得到了很大的發展據已有資料結合國內的研究結果可歸納為以下幾方面:維A酸(ATRA)在誘導分化的同時改變APL細胞的生物學性質,解除其對骨髓造血細胞的抑制作用;APL的特異融合蛋白PML/RARα在ATRA的作用下降解PML的分布恢復正常,RARαRARX的正常功能以及原受PML/RARα抑制的早幼粒細胞分化得以恢復;維A酸(ATRA)促進APL細胞凋亡;維A酸(ATRA)上調下列蛋白和基因RARα、RARβ、IRF-2STATlaSTATlbSTAT2、RIG-E、FGH、I、IL-lbG-CSF受體、GM-CSF受體、CD11cCD11bCDl5CD18、CD45RO、蛋白激酶C組織谷氨醯轉移酶鳥氨酸脫羧酶鹼性磷酸酶、尿激酶型纖溶酶原活化劑、MCP-1IFN-α纖溶酶活化劑抑制物(PAI)。相反aATRA下調下列蛋白和基因:組織因子腫瘤促凝物質、組織因子連接素ⅧC-MYCCD33端粒酶活性、BCL-2、PARP(多聚ADP核糖聚合酶)、組織彈力酶G彈性蛋白酶髓過氧化物酶、CD45RA抗原由此可見,維A酸(ATRA)的作用涉及範圍甚廣,有的直接影響維A酸(ATRA)的結合和作用,如與RARα結合;有的與早幼粒細胞的功能有關如一些酶的改變;有的涉及出凝血,如組織因子腫瘤促凝物質的下調可解釋為何在維A酸(ATRA)誘導分化過程中,DIC改善;有的基因與信號傳導密切有關,如STAT、PKC;不少基因的改變可闡明維A酸(ATRA)的促凋亡作用,如BCL-2、PARP的下降。G-CSF、GM-CSF受體的上調可解釋維A酸(ATRA)治療過程中白細胞增高的原因上海血液病研究所研究發現,由維A酸(ATRA)誘導上調的一些基因(RIG-E,FGHI)雖然已初步闡明它們的性質如RIG-G與干擾素刺激基因(ISG)中的一個家族有很高的同源性和相同的染色體定位RIG-E與某些受體如EGFR(上皮生長因子受體),LDL-RuPAR等有一定的同源性,但它們在維A酸(ATRA)誘導分化治療APL中的確切機制,尚待進一步闡明。
砷劑治療
① 誘導緩解:維A酸(ATRA)治療初治APL雖可取得很高的緩解率,但多數病例易產生耐藥性複發後再用維A酸(ATRA)治療,效果較差自20世紀70年代初期哈爾濱醫科大學用以砷劑為主要成分的「癌靈1號」治療APL,取得較好療效。誘導緩解治療方案:成人0.1% As2O3注射液10ml/d,加入5%葡萄糖液250~500ml中靜脈滴注3~4 h,兒童可按6mg/m2計量,4周為1個療程每療程可間歇5~7天也可連續用藥2個療程病情無緩解為無效。
1995年黃世林等報導,應用含巰化砷的中藥復方青黛片治療初治APL的結果。方案如下:口服復方青黛片,每天15片(0.25g/片),一周後逐漸加量至每天30片,持續用藥30~60天,CR率可達98.3%。1998年2月起陸道培等應用中等純度As4S4(TATS)治療APL,方法為:口服0.5g每天3次,持續2~4周休息2~3周,共維持3~4年後又開展了高純度TATS的臨床應用方法為:1g3次/d直至CR休息2~3周第4年休息間隔時間可延長至4~6周應用TATS後,血漿砷濃度於第15天達高峰(40~104mcg/L),停藥2周後血漿砷濃度降至<2~22mcg/L(平均15mcg/L),停藥30天後平均血漿濃度為3mcg/L。
A、As2O3治療APL的適應證:
a、初治APL特別是t(15;17)或PML-RARα融合基因陽性者
b、維A酸(ATRA)或聯合化療治療無效的難治或複發的APL
c、不能耐受或不宜應用維A酸(ATRA)或聯合化療的APLd.APL CR後鞏固維持治療。
e、伴有異常早幼粒細胞增多的其他類型白血病(慢性粒細胞白血病急變、ANLL M2M4、M6型)及MDS等。
不宜選用As203治療的APL:有非白血病本身所致的嚴重肝、腎功能障礙者;用As2O3鞏固治療複發者;有砷中毒表現者。
B、毒副反應:急性毒副反應主要有液體瀦留(胸腔積液、心包積液、體重增加),短期使用利尿劑有效,用地塞米松無明顯療效約20%的患者可出現消化道反應表現為噁心嘔吐、腹痛、腹瀉、食慾下降10%的患者有不同程度的手足麻木、顏面水腫。常規劑量下20%~30%的患者可能出現不同程度的腎功能異常,但停藥後1~2周大多恢復正常。對肝臟,在原有慢性肝炎的病例易誘發肝細胞壞死,引起肝功能衰竭。心電圖可出現竇性心動過速Ⅰ~Ⅱ度房室傳導阻滯完全性房室傳導阻滯及各種室性心律失常。必須指出,砷劑治療過程中也有2/3的患者白細胞升高,有10%~15%的患者並發類似維A酸症候群其臨床表現及處理與維A酸治療時發生的相同。部分患者出現有慢性副作用表現為皮膚色素沉著、掌角化病多神經病(感覺運動神經功能均受損),肌肉萎縮。劑量>0.2mg/(kg.d)時可出現弛緩性麻痹腎衰等嚴重副作用。慢性As203中毒不僅取決於所用的量而且取決於個體的易感性當出現砷劑嚴重中毒時可用藥物來減輕其副作用,如二巰基丙磺酸鈉(2,3-二巰基磺酸丙烷)等。
C、砷劑治療APL的機制:形態學上可見細胞核染質固縮形成凋亡小體。體外研究發現低濃度砷劑(0.1μmol/L)對NB4細胞有誘導分化作用在高濃度下(>0.5~1μmol/L),砷劑誘導凋亡。DNA分析,在細胞流式儀檢測中可見G1峰前出現凋亡峰DNA電泳示典型的凋亡梯形改變細胞及分子生物學研究結果顯示,As2O3可使PML/RARα融合蛋白降解BCL-2基因下調,對BAX基因無作用。以上結果提示As2O3治療APL的作用機制可能主要是誘導APL細胞凋亡,低濃度誘導分化此外砷劑作用中的一些分子機制包括:
a、絲裂原激活的蛋白激酶(cMAPK)信號通道與應激相關的JNK/SAPK(應激激活蛋白酶)和P38激酶被激活,導致凋亡。
b、砷劑使粒線體膜上的PT(通透性改變)孔通透性增高,致粒線體內AIF及細胞色素C釋放至粒線體外。
c、對G1/S及G2/M起作用,使細胞周期延長。
d、三價砷可誘導紅白血病細胞的鳥氨酸脫羧酶(ornithine decarboxylase,ODC)活力改變,影響多胺的合成抑制腫瘤生長。
② APL完全緩解後砷劑治療:應用常規劑量As2O3,每療程2~3周As2O3應用間歇期在CR後第12、3及3年後分別為123或4及6個月;也可將As203與聯合化療(HA、DA或Am-C+米托蒽醌(NVT)/依託泊苷(VP-16)交替進行間歇期同上。
ATBA聯合As203治療APL
維A酸(ATRA)治療APL可取得80%~90%的完全緩解率(CR)與典型的細胞毒藥物相比維A酸(ATRA)能夠改善APL患者的凝血障礙而不引起骨髓抑制然而維A酸(ATRA)可能引起致死性的藥物相關症候群,同時單用維A酸(ATRA)維持治療常引起白血病的複發,因而限制了其應用As203不但能誘導初治APL取得CR,還可誘導經細胞毒藥物、維A酸(ATRA)等治療後複發的患者達到90%的CR體外實驗證明As2O3的作用機制與維A酸(ATRA)不同,能引起白血病細胞發生凋亡維A酸(ATRA)聯合As203對APL細胞系與新鮮APL細胞作用的研究表明,兩種藥物聯合具有協同促分化作用,也可促進耐藥細胞對藥物的敏感性上海血液病研究所應用維A酸(ATRA )25mg/(m2.d)As203 0.16mg/(kg.d)聯合治療初發的APL直至CR。結果顯示31例患者早期死亡2例29例獲CRCR率為93.5%獲得CR的平均時間為(25.1±3.9)天66.5%的患者治療後白細胞升高65.5%出現肝功能異常,但減量或停用1周內恢復。至CR時10.3%的PML/RARα轉陰鞏固治療後77.0%轉陰。
造血幹細胞移植(HSCT)
初發病例用維A酸(ATRA)聯合化療CR可達70%~80%且大部分患者在首次複發後應用As203或再次應用維A酸(ATRA)與化療等,還可獲得較高的二次緩解率(CR2),因此一般認為首次緩解的患者並不主張行HSCT
治療儘管目前的治療方法可使APL獲得較高的緩解率,但複發率仍達25%,對於這些患者自體或異基因幹細胞移植不失為一種挽救的治療方法。在臨床應用維A酸(ATRA)之前,HSCT可使45%的二次緩解的患者治癒最近的研究顯示二次緩解後應用自體移植效果非常好,可減少白血病的複發使無病生存率超過70%。國內外報告表明CR後骨髓移植3年DFS在77%~80%以上,優於單化療或化療合併維A酸(ATRA)的CR後治療方案鑒於APL緩解患者使用化療、維A酸以及砷劑,5年生存率可達50%~70%,並且考慮到治療相關死亡率因而本病第一次完全緩解後不一定需要進行HSCT治療,主要適用於複發患者或PML-RARα融合基因長期持續陽性的患者。不過儘管存在15%~20%的移植相關死亡率異基因HSCT對於二次或多次緩解的患者仍是一種重要的治療選擇對年青和不能達到遺傳學緩解的患者,如果有合適的供者,也應選擇HSCT治療。
新的治療方法
① 脂質體維A酸(ATRA):目前臨床上的維A酸(ATRA)僅使用口服製劑,最近一種靜脈使用的脂質體維A酸(ATRA)已開發出來該製劑適宜不能吞咽或吸收的患者及兒童患者,可克服這些患者口服所致血藥濃度的不穩定。脂質體維A酸(ATRA)的最大耐受劑量為140mg/m2,90mg/m2的劑量可安全有效地使初發及複發的APL患者達到緩解。所以儘管口服製劑易於使用脂質體維A酸(ATRA)仍可能成為一種方便的替代品。
② 組蛋白去乙醯化酶抑制劑:許多基因的轉錄活性由組蛋白的乙醯化狀態所決定;組蛋白的乙醯化狀態由組蛋白乙醯基轉移酶(HATs)和組蛋白脫乙醯化酶(HDACs)調節。HDACs抑制劑具有促分化、抗增殖和凋亡的作用,主要包括有丁酸鹽、曲古抑菌素、苯甲醯胺、環狀多肽等這些成分與維A酸(ATRA)聯用具有明顯的抗白血病作用。
③ 單株抗體:HuM195是一種人源化的抗CD33單株抗體已成功地用於經過維A酸(ATRA)和(或)化療達到血液學緩解、PCR陽性的APL微小殘留病變的治療。HuM195可與131I90Y和213Bi連接其臨床治療作用尚待觀察另外一種人源化的抗CD33單株抗體與calicheamicin(CMA676Mylotary)結合的分子已開發出來這種單抗已被FDA批准用來治療複發的AML初步的結果顯示它可控制具有分子生物學複發證據的APL患者的微小殘留病變。
中藥對治療的效果
去年7月份,《自然》雜誌發表文章指出,對科學家來說,中藥是如此地「難以下咽」,中藥仍然籠罩在知其然不知其所以然的神秘面紗下。藉助於典型的還原法,研究人員希望尋找出治療特定疾病的中藥配方中的某種關鍵組分,但類似青蒿素的成功例子少而又少。文章呼籲用一種全新的科學方法來研究中藥。
僅僅半年多之後,今年3月14日,陳竺院士領導的團隊在《美國國家科學院院刊》(PNAS)發表一篇論文,對中藥方劑復方黃黛片治療急性早幼粒性白血病的分子機理做了系統分析,用生物化學的方法,從分子水平闡明了一個完全依據中醫理論研發出來的中藥復方黃黛片治療白血病的多成分多靶點作用機理,並將中藥方劑「君、臣、佐、使」的配伍原則用現代醫學的方法闡釋得淋漓盡致。
3月17日,全國兩會即將結束,被任命為新一屆政府衛生部長的陳竺院士,花了近兩個小時接受本報記者專訪,詳細地解釋了這項研究及成果,並談了他對中醫藥現代化的理解。
中醫藥可以「說得清道得明」
陳竺作為科學家,最被人稱道的研究成果是利用全反式維甲酸、三氧化二砷(砒霜)協同治療急性早幼粒細胞性白血病(APL)。按照這種方法治療,可以使病人的5年無病生存率超過90%。APL有望成為第一種可以被治癒的成人急性髓細胞性白血病。
據介紹,急性早幼粒性白血病被認為是最兇險的一種白血病,病人骨髓里積累大量的不成熟的早幼粒細胞,且具有嚴重的出血症状。該病的病因已經研究得比較清楚,主要是兩條染色體易位,即染色體臂斷裂後互相交換,在結合點就出現一個的融合基因PML-RARα,它編碼一個融合蛋白,最終導致細胞癌變。
一般的血細胞在分裂一定的代數後就會分化成熟,變成具有各種特定結構和功能的細胞。但癌變以後的細胞失去了分化能力,會不停地「瘋長」下去。全反式維甲酸正是通過修飾和代謝癌蛋白PML-RARα,使癌細胞重新分化,「改邪歸正」,停止「瘋長」;三氧化二砷則可以引起這種癌蛋白的降解,使癌細胞發生部分分化並最終進入程序化死亡(凋亡)。
有著西方醫學教育背景的陳竺,介紹自己的研究時,總是強調接受了中國傳統醫學思想的啟發。復方協同治療、以毒攻毒、祛邪扶正、好壞轉化……處處閃耀著東方哲學的智慧。這也就不難理解他熱衷於用現代分子生物學的方法來闡釋中藥復方了。
他介紹說,早在急性早幼粒細胞性白血病的分子研究尚未開始、癌蛋白PML-RARα尚未被認識的上世紀80年代,解放軍大連210醫院的中醫專家黃世林教授在辯證與辨病相結合的基礎上,設計了由雄黃、青黛、丹參、太子參組成的復方黃黛片。此後,安徽天康藥業有限公司按照嚴格的現代工藝批量生產。近年來一項多中心臨床研究,證實了復方黃黛片的療效,其治療急性早幼粒性白血病,5年生存率可達87%%。研究還發現,雄黃、青黛、丹參的有效成分分別為四硫化四砷、靛玉紅與丹參酮IIA。不過,復方黃黛片在分子水平的作用機理一直未被揭示。
於是,在陳竺院士、陳賽娟院士的領導下,上海交通大學瑞金醫院、中科院廣州生物醫藥與健康研究院等多個研究小組,經過4年的研究發現,對於急性早幼粒細胞性白血病的小鼠模型,單獨應用硫化砷可延長小鼠的生存期,而三藥聯合可取得明顯強於單獨或兩藥聯合產生的治療效果。在白血病細胞模型中,硫化砷、丹參酮單獨應用時可引起白血病細胞一定程度的分化,而三藥聯合可使白血病細胞發生相當程度的「改邪歸正」、分化成熟。
在正常情況下,造血細胞由幼稚到成熟的分化過程中,促進細胞分化的基因、屬「正」的因素必須逐漸增高,而抑制細胞分化的基因、屬「邪」的因素必須相應減少;在細胞周期的調控方面,促進細胞周期的蛋白「陽」與抑制細胞周期的因子「陰」必須維持平衡。患白血病,「正」往往受到壓制而「邪」盛,「陽亢」而「陰虛」。
在分子水平上,三藥聯合可顯著增強由硫化砷引起的對急性早幼粒細胞性白血病的致病性PML-RARα癌蛋白的降解破壞,因此具有「去邪」的作用,硫化砷是「君藥」。在藥物作用下,促進細胞分化的基因表達明顯增高,抑制細胞分化的基因顯著降低,丹參酮在其中起重要作用;促進細胞周期的蛋白明顯得到壓制,而抑制細胞周期的蛋白顯著增多,其中靛玉紅髮揮重要作用,研究證實丹參酮是「臣藥」、靛玉紅是「佐藥」。研究還發現,丹參酮與靛玉紅通過增加負責運輸硫化砷的水甘油通道蛋白9的含量,促使進入白血病細胞的硫化砷明顯增多,因此二者都起到「使藥」的作用。復方黃黛片通過聯合應用,產生協同效應。
中醫藥的生命力在於開放和創新
「這是一項十分令人感興趣、具有高度科學意義的研究,開啟了用中藥復方原理設計聯合治療方案的範例,勢必引起學界的極大關注。」一位藥理學國際權威專家對論文給予了如此的肯定。
不少專家認為從分子生物學和生物化學的角度看,這項研究幾乎近於無懈可擊、堪稱「完美」。非常經典地解析和闡明了,一個完全依據中醫理論研發出來的中藥復方,在細胞和分子水平的明確的作用靶點和機制。而且,每種藥物在分子水平的作用與中醫對每味藥物在復方中的地位和作用的認識竟然呼應得是如此之好,簡直令人驚嘆!
國際主流科學界也對這一研究成果給予積極評價,如《自然》雜誌發表題為「中醫藥:古老復方的現代新解」的述評,認為這一研究顯示了「古老藥方的主要成分是如何『和諧行動』治療疾病的,對於中國傳統醫學與現代醫學的溝通具有重要意義」;《科學》雜誌在對陳竺的訪談中也對該文進行了報導。
而陳竺卻認為,這項研究能夠獲得這樣的成果,是非常幸運的!
「我們有合適的物質基礎,包括純化的有效化合物、細胞模型與動物模型等。」陳竺說,「當然最重要的是復方黃黛片有非常好的臨床療效,並且被多中心臨床研究所證實,沒有這個基礎,所有的後續研究都是無源之水。從這一點來看,中醫藥自身的創新發展還是最重要的。」
中醫理論體系的豐富發展和實踐能力的提高,是中醫發展之本,既要講創新,更要講傳承。陳竺說:「我支持在中醫教育和臨床實踐中倡導發展『原汁原味』的中醫!」
陳竺認為,中醫藥的現代化同樣需要開放的心態。中醫幾千年的歷史,從來就不是故步自封的歷史,其內涵不斷豐富和進步。波斯醫學的傳入,「胡藥」與「南藥」的引入,都對中醫發展有著重要貢獻。利用現代科學技術手段與多學科方法研究中醫藥,對中醫發展會起到支撐和促進作用。
近年來,西醫正逐漸認識到聯合治療方法的益處,而中醫通過近10萬種復方倡導聯合療法已有兩千五百年的歷史了。中藥復方雖然在臨床實踐中取得一定療效,但是大多數復方的有效成分尚不明了,作用機理也不清楚,造成推廣應用受到限制。「在確定臨床療效的基礎上,開展機理研究,不僅有利於中醫的現代化、國際化,還可以為優化方藥配伍提供依據。」
陳竺認為,中醫藥系統在創新方面,應更加開放,更加善於汲取人類共同智慧的結晶。基因組學、蛋白質組學、代謝組學的最新研究成果,核磁共振、生物電、熱成像、基因剔除……所有的物理化學生物學的技術,動物模型,人體成像,不論是什麼,都可以拿來為中醫藥研究所用,而且有關體系都要接受生物醫學統計學的嚴格檢驗。現代生命科學並不姓「西」!要創造條件,把中國生命科學界的優秀科學家和優秀科研機構,吸引到中醫藥現代化創新體系中來。
現在系統生物醫學為中、西兩大醫學的匯聚創造了前所未有的機遇和平台,把中醫和西醫整合在一起,是促進中醫現代化的非常好的途徑。陳竺期望,中醫藥在保持自身特色,傳承發展的同時,更好地匯聚、融合現代科學技術,從而創造出一個高於傳統意義上的中醫和西醫的全新醫學。
急性早幼粒白血病的症状
頭暈 乏力 噁心 持續高燒 咳嗽 牙齦出血 牙齦腫痛 牙齦萎縮 眼底出血 心悸 脾大 便血 貧血症状
化療
主要用全反式維甲酸,三氧化二砷,柔紅,阿糖胞苷 VP16聯合化療 緩解率達90%
心態
平常心 別害怕 莫生氣 誰體驗誰知道 就當作是人生中的插曲 也是歷練心智的好機會 相信自己能行
效果
感覺很好 和正常人沒區別 基本可治癒 複發了也沒關係 還可繼續化療得到緩解.
預後
以往APL的治療效果差,病情兇險隨著對APL的細胞生物學的特性認識的不斷提高和治療方法的改進,使治療結果和預後有了很大的改善,早期死亡率明顯下降,持續緩解時間延長是目前白血病治療效果最好的一種類型。
|
|||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||
| 關於「急性早幼粒細胞白血病」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |