藥理學/喹諾酮類藥物
| 醫學電子書 >> 《藥理學》 >> 人工合成抗菌藥 >> 喹諾酮類藥物 |
| 藥理學 |
|
|
|
喹諾酮類quinolones是人工合成的含4-喹諾酮基本結構,對細菌DNA螺旋酶(DNA gyrase)具有選擇性抑制作用的抗菌藥物。目前發展迅速,臨床廣為使用。
目錄 |
一、喹諾酮類藥物概述
(一)簡史
萘啶酸(nalidixicacid)是1962年用於臨床的第一個喹諾酮類藥(實是萘啶酮),抗菌譜窄,口服吸收差,副作用多,現已不用。吡哌酸(pipemidicacid)抗菌活性強於萘啶酸,口服少量吸收,不良反應較萘啶酸少,可用于敏感菌的尿路感染與腸道感染。1979年合成諾氟沙星(norfloxacin),隨又合成一系列含氟的新喹諾酮類藥,通稱為氟喹諾酮類(fluoroquinolones)。
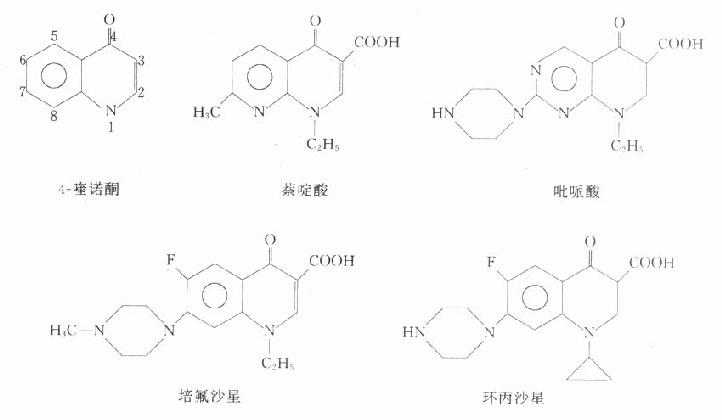
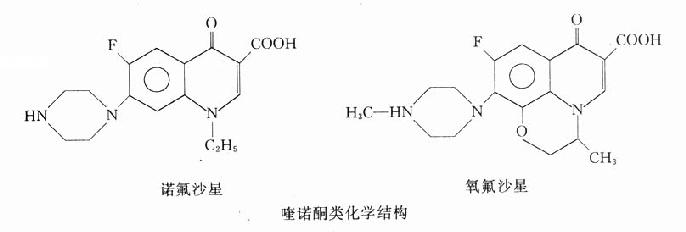
(二)化學結構與作用關係
本類藥物的構效關係研究表明:4-喹諾酮母核的3位均有羧酸基,6位引入氟原子可增強抗菌作用並對金葡菌有抗菌活性;7位引進哌嗪環可提高對金葡菌及綠膿桿菌的抗菌作用(如諾氟沙星),哌嗪環被甲基哌嗪環取代(如培氟沙星),則脂溶性增加,腸道吸收增強,細胞的穿透性提高,半衰期延長。在8位引進第二個氟原子,可進一步提高腸道吸收,延長半衰期(如洛美沙星等),N-1修飾以環丙基團(環丙沙星)或噁嗪基團(氧氟沙星)可擴大抗菌譜,增強對衣原體、支原體及分支桿菌(結核桿菌與麻風桿菌等)的抗菌活性,噁嗪環還可提高水溶性,使藥物在體內不被代謝,以原形經尿排泄。
(三)抗菌作用機制
喹諾酮類通過抑制DNA螺旋酶作用,阻礙DNA合成而導致細菌死亡。大腸桿菌的DNA螺旋酶是四疊體結構的蛋白,由2個A亞單位與2個B亞單位組成,分子量分別為105kD與95kD(見圖42-1)。細菌在合成DNA過程中,DNA螺旋酶的A亞單位將染色體DNA正超螺旋的一條單鏈(後鏈)切開,接著B亞單位使DNA的前鏈後移,A亞單位再將切口封住,形成了負超螺旋。根據實驗研究,氟喹諾酮類藥並不是直接與DNA螺旋酶結合,而是與DNA雙鏈中非配對鹼基結合,抑制DNA抑螺旋酶的A亞單位,使DNA超螺旋結構不能封口,這樣DNA單鏈暴露,導致mRNA與蛋白合成失控,最後細菌死亡。
本類藥體外對DNA螺旋酶的半抑制濃度(IC50)與其對細菌的MIC呈一定的平行關係。哺乳動物的細胞內也含有生物活性與細菌DNA螺旋酶相似的酶,稱為拓樸異構酶Ⅱ(topoisomerase Ⅱ)。氟喹諾酮類藥對人體細胞拓樸異構酶Ⅱ影響較小(見表42-1)。從該表可見氧氟沙星與環丙沙星對動物細胞內拓樸異構酶Ⅱ的作用明顯比依諾沙星與萘啶酸小,IC50很高,選擇指數很大。這可能是氧氟沙星與環丙沙星不良反應較少的原因。
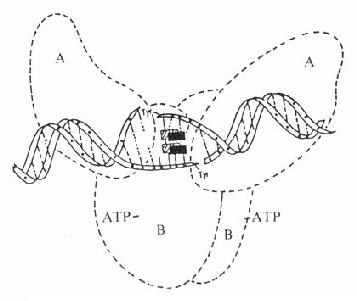
圖42-1 喹諾酮類藥物-DNA結合抑制DNA螺旋酶活性的示意圖
圖中實心和斜線長方形示喹諾酮類藥物分子,A、B為DNA螺旋酶的A、B亞單位。在DNA螺旋酶作用下,DNA雙鏈打開,而藥物分子嵌入雙鏈。與非配對鹼基結合,阻礙DNA雙鏈封口
(四)細菌耐藥機制
氟喹諾酮類藥物廣泛應用後,已出現細菌耐藥性。耐藥機理研究證實主要是染色體突變,不存在質體介導的耐藥性。耐藥機制有二:①細菌DNA螺旋酶的改變,與細菌高濃度耐藥有關;②細菌細胞膜孔蛋白通道的改變或缺失與低濃度耐藥有關。耐藥菌株DNA螺旋酶的活性改變主要由於gyrA基因突變所致。
(五)氟喹諾酮類藥理學共同特性
①抗菌譜廣,尤其對革蘭陰性桿菌包括綠膿桿菌在內有強大的殺菌作用,對金葡菌及產酶金葡菌也有良好抗菌作用;某些品種對結核桿菌,支原體,衣原體及厭氧菌也有作用;②細菌對本類藥與其他抗菌藥物間無交叉耐藥性;③口服吸收良好,部分品種可靜脈給藥;體內分布廣,組織體液濃度高,可達有效抑菌或殺菌水平;血漿半衰期相對較長,大多為3~7小時以上。血漿蛋白結合率低(14%~30%),多數經尿排泄,尿中濃度高;④適用于敏感病原菌所致的呼吸道感染、尿路感染、前列腺炎,淋病及革蘭陰性桿菌所致各種感染,骨、關節、皮膚軟組織感染;⑤不良反應少(5%~10%),大多輕微,常見的有噁心、嘔吐、食慾減退、皮疹、頭痛、眩暈。偶有抽搐精神症状,停藥可消退。
表42-1 喹諾酮類藥物對大腸桿菌和哺乳動物細胞DNA旋轉酶的選擇作用
| 藥物 | IC50(mg/L) | 選擇指數B/A | |
| A大腸桿菌KL-16DNA螺旋酶 | B胎牛胸腺局部拓樸異構酶Ⅱ | ||
| 氧氟沙星 | 0.76 | 1870 | 2461 |
| 環丙沙星 | 0.13 | 155 | 1192 |
| 依諾沙星 | 1.72 | 93 | 54 |
| 萘啶酸 | 23.0 | 385 | 17 |
二、各種喹諾酮類藥特點
吡哌酸(pipemidic acid,PPA)對革蘭陰性菌的抗菌作用較萘啶酸強,對革蘭陽性和部分綠膿桿菌有一定作用。口服400mg後血濃度達不到治療效果,但尿中濃度高,可達900mg/L以上,主要用於治療尿路和腸道感染。
諾氟沙星(norfloxacin)又名氟哌酸,是第一個氟喹諾酮類藥,抗菌譜廣,抗菌作用強,對革蘭陽性和陰性菌包括綠膿桿菌均有良好抗菌活性,明顯優於吡哌酸。口服吸收約35%~45%;易受食物影響,空腹比飯後服藥的血濃度高2~3倍,血漿蛋白結合率為14%,體內分布廣,組織濃度高,藥物消除半衰期為3~4小時。主要用於尿路及腸道感染。
氧氟沙星(ofloxacin)又名氟嗪酸,抗菌活性強,對革蘭陽性菌(包括甲氧西林耐藥金葡菌,MRSA)革蘭陰性菌包括綠膿桿菌均有較強作用;對肺炎支原體,奈瑟菌病,厭氧菌及結核桿菌也有一定活性。對感染小鼠的保護效果明顯強於諾氟沙星、依諾沙星。口服吸收快而完全,血藥濃度高而持久,血漿消除半衰期為5~7小時,藥物體內分布廣,尤以痰中濃度較高,70%~90%藥物經腎排泄,48小時尿中藥物濃度仍可達到對敏感菌的殺菌水平,膽汁中藥物濃度約為血藥濃度的7倍左右。
依諾沙星(enoxacin)又名氟啶酸,抗菌譜和抗菌活性和諾氟沙星相似,對厭氧菌作用較差。口服吸收好,不受食物影響,血藥濃度介於諾氟沙星與氧氟沙星之間,口服後約50%~65%經腎排泄,消除半衰期為3.3~5.8小時。副作用以消化道反應為主,偶有中樞神經系統毒性反應。
培氟沙星(pefloxacin)又名甲氟哌酸,抗菌譜廣與諾氟沙星相似,抗菌活性略遜於諾氟沙星,對軍團菌及MRSA有效,對綠膿桿菌的作用不及環丙沙星。口服吸收好,生物利用度為90%~100%。血藥濃度高而持久,半衰期可達10小時以上,體內分布廣泛,尚可通過炎症腦膜進入腦脊液。
環丙沙星(ciprofloxacin)又名環丙氟哌酸,抗菌譜廣,體外抗菌活性為目前在臨床應用喹諾酮類中最強,對耐藥綠膿桿菌,MRSA,產青黴素酶淋球菌、產酶流感桿菌等均有良效,對肺炎軍團菌及彎麴菌亦有效,一些對氨基甙類、第三代頭孢菌素等耐藥的革蘭陰性和陽性菌對本品仍然敏感。口服後本品生物利用度為38%~60%,血濃度較低,靜脈滴注可彌補此缺點。半衰期為3.3~5.8小時,藥物吸收後體內分布廣泛。
洛美沙星(lomefloxacin)抗菌譜廣,體外抗菌作用與諾氟沙星、氧氟沙星、氟羅沙星相似,但比環丙沙星弱;體內抗菌活性比諾氟沙星與氧氟沙星強,但不及氟羅沙星。本品口服吸收好,生物利用度為85%,血藥濃度高而持久,半衰期約7小時,體內分布廣,藥物經腎排泄。
氟羅沙星(fleroxacin)又名多氟沙星,抗菌譜廣,體外抗菌活性略遜於環丙沙星,但其體內抗菌活性強於現有各喹諾酮藥。口服吸收好,生物利用度達99%。口服同劑量(400mg)的血藥濃度比環丙沙星高2~3倍,半衰期為9小時。體內分布廣,藥物經腎排泄,約為給藥量50%~60%。
表42-2 幾種常用氟喹諾酮類藥的藥代動力學參數
| 藥物 | 單次口服劑量(mg) | Cmax(mg/L) | t1/2kel(h) | 絕對生物利用度(%) | Vd(L) | 總清除率(L/h) | 原藥尿中排泄率(%) | 糞便排泄率(%) |
| 諾氟沙星 | 400 | 1.58 | 3~4 | 35~45 | >100 | 51.6 | 25~30 | 28 |
| 培氟沙星 | 400 | 3.80 | 7.5~11 | 90~100 | 139 | 8.94 | 11 | |
| 依諾沙星 | 400 | 3.70 | 3.3~5.8 | 80~89 | 175 | 21.0 | 52 | 18 |
| 氧氟沙星 | 400 | 5.60 | 5.0~7.0 | 85~95 | 120 | 12.84 | 70~80 | 4 |
| 環丙沙星 | 500 | 2.56 | 3.3~4.9 | 38~60 | 307 | 39.12 | 29~44 | 15 |
三、應用注意事項
1.對幼年動物可引起軟骨組織損害,故不宜用於妊娠期婦女和骨骼系統未發育完全的小兒。藥物可分泌於乳汁,乳婦應用時應停止哺乳。
2.可引起中樞神經系統不良反應,不宜用於有中樞神經系統病史者,尤其是有癲癇病史的患者。
3.可抑制茶鹼類、咖啡因和口服抗凝血藥在肝中代謝,使上述藥物濃度升高引起不良反應。產生上述相互作用最顯著者為依諾沙星、其次為環丙沙星與培氟沙星,氧氟沙星無明顯影響。因此應避免與有相互作用的藥物合用,如有指征合用時,應對有關藥物進行必要的監測。
4.吸收,宜避免合用。
5.腎功能減退者應用主要經腎排的藥物如氧氟沙星和依諾沙星應減量。
參看
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 關於「藥理學/喹諾酮類藥物」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |