病理學/病毒性肝炎
| 醫學電子書 >> 《病理學》 >> 消化系統疾病 >> 肝膽疾病 >> 病毒性肝炎 |
| 病理學 |
|
|
病毒性肝炎(viral hepatitis)是由肝炎病毒引起的以肝實質細胞變性壞死為主要病變的傳染病。現已知肝炎有甲型、乙型、丙型、丁型及戊型5種,由各該型病毒引起。1974年以來提出的非甲非B型肝炎(NANB型),經近年研究證明,其中大部分為C型肝炎並檢出了C肝病毒(HCV)及其抗體,另一小部分則為戊型肝炎。肝炎在世界各地均有發病和流行,且發病率有不斷升高趨勢。其發病無性別差異,各種年齡均可罹患。
【病因】
從1970年起,經過20年的研究,目前對肝炎病毒已比較清楚,由最初僅知的A型肝炎病毒和B型肝炎病毒二種,增加到由甲到戊5種病毒(HAV~HEV)。其特點見表10-2。
表10-2 各型肝炎病毒特點
| 肝炎及其病毒分型 | 病毒類型 | 傳染方式 | 克隆化年代 |
|
HAV |
Enterovirus RNA型 |
腸道 | 1983年(1973檢出) |
|
Hepadnavirus DNA型 |
非腸道 | 1979年(1963檢出) | |
|
C型肝炎 HCV |
Flavivirus RNA型 |
非腸道 | 1989年 |
|
Viroidrelated RNA型 |
非腸道 | 1986年 | |
|
戊型肝炎 HEV |
Calcivirus RNA型 |
腸道 | 1990年 |
(采自Seeff)
在上述各型肝炎病毒中,以HBV發現最早,研究得最多。現知該病毒是由核心及外殼兩部分構成的病毒顆粒(Dane顆粒)。病毒基因組DNA在肝細胞核內進行複製、轉錄,合成核心顆粒後,被轉運到肝細胞漿內,在通過內質網和細胞膜時合成其外殼部分,並以「發芽」過程釋出肝細胞。Dane顆粒的核心部分含核心抗原(HbcAg),外殼部分含表面抗原(HBsAg)。目前認為引起肝細胞免疫損害的只是HBsAg誘發的免疫反應,其中以細胞免疫反應起主要作用。HAV是一種微小的RNA病毒,在肝細胞漿內增殖,現已被列入腸道病毒,該病毒顆粒可在糞便中檢出。HCV的整組基因近年也可克隆化並標記其病毒抗體。HDV是一種微小缺陷性RNA病毒,現知此種病毒為球形以HBsAg作為其外殼,只能在HBsAg陽性機體內生長,故丁型肝炎常與B型肝炎合併存在。HEV的顆粒為球形無包膜,表面有尖釘狀突起。我國學者已將HEV分離培養並建立了細胞系(Huang RT等,1992)。
【傳染途徑】
各型肝炎病毒均可存在於肝組織、血液、糞、尿及各種體液內。其傳染方式主要是經口、經血及體液傳播,但各型肝炎的傳染途徑各異。甲型、戊型多經口感染。常來源於飲水及食物的污染,有時呈流行性暴發。乙型、丙型經血感染,主要通過輸血、輸液也可通過經皮及性接觸傳播。丁型亦為非經口感染,常與B型肝炎傳播伴行。各型肝炎的潛伏期也不相同,如甲型15~50天,乙型60~180天。戊型2~9周。丙型7~8周。一般認為肝炎痊癒後均可獲得免疫力但均不穩固(甲型者稍好),有少部分患者還可發生再感染。
【基本病變】
各型肝炎病變基本相同,都是以肝細胞的變性、壞死為主,同時伴有不同程度的炎性細胞浸潤、肝細胞再生和纖維組織增生。
1.肝細胞變性、壞死
(1)胞漿疏鬆化和氣球樣變:為常見的變性病變,是由於肝細胞受損後細胞水分增多造成。開始時肝細胞腫大,胞漿疏鬆呈網狀、半透明,稱胞漿疏鬆化。進一步發展,肝細胞更形脹大呈球形,胞漿幾完全透明,稱為氣球樣變(ballooning degeneration)(圖10-34)。電鏡下,可見內質網擴張、囊泡變、核蛋白顆粒脫失;粒線體腫脹、嵴消失等。
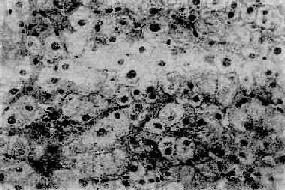
圖10-34 急性病毒性肝炎
肝細胞胞漿疏鬆化和氣球樣變,肝竇受壓變窄
(2)嗜酸性變及嗜酸性壞死:嗜酸性變多累及單個或幾個肝細胞,散在於小葉內。肝細胞胞漿水分脫失濃縮,嗜酸性染色增強,胞漿顆粒性消失。如進一步發展,胞漿更加濃縮之外,胞核也濃縮以至消失。最後剩下深紅色均一濃染的圓形小體,即所謂嗜酸性小體(acidophilic body或Councillman body)(圖10-35)。上述改變稱嗜酸性壞死(acidophilic necrosis),為單個細胞壞死(細胞凋謝)。
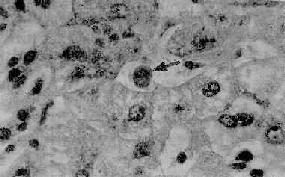
圖10-35 急性病毒性肝炎
游離於肝竇內的嗜酸性小體(↑處),竇內皮細胞腫脹增生
(3)點狀壞死(spotty necrosis):肝小葉內散在的灶狀肝細胞壞死。每個壞死灶僅累及1至幾個肝細胞。同時該處伴以炎性細胞浸潤(圖10-36)。
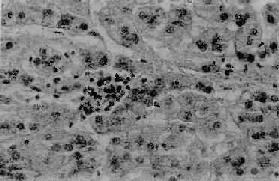
圖10-36 病毒性肝炎
肝細胞點狀壞死,壞死灶內有炎性細胞浸潤
(4)溶解壞死(lytic necrosis)最多見,常由高度氣球樣變發展而來。此時胞核固縮、溶解、消失,最後細胞解體。重型肝炎時肝細胞的變性往往不明顯,很快就發生此種壞死崩解。
2.炎細胞浸潤肝炎時在匯管區或肝小葉內常有程度不等的炎性細胞浸潤。浸潤的炎細胞主要是淋巴細胞、單核細胞,有時也見少量漿細胞及中性粒細胞等。
3.間質反應性增生及肝細胞再生
(1)Kupffer細胞增生肥大:這是肝內單核吞噬細胞系統的炎性反應。增生的細胞呈梭形或多角形,胞漿豐富,突出於竇壁或自壁上脫入竇內成為遊走的吞噬細胞。
(2)間葉細胞及纖維母細胞的增生:間葉細胞具有多向分化的潛能,存在於肝間質內,肝炎時可分化為組織細胞參與炎性細胞浸潤。在反覆發生嚴重壞死病例,由於大量纖維組織增生可發展成肝纖維化及肝硬變。
(3)肝細胞再生:肝細胞壞死時,鄰近的肝細胞可通過直接或間接分裂而再生修復。在肝炎恢復期或慢性階段則更為明顯。再生的肝細胞體積較大,核大而染色較深,有的可有雙核。慢性病例在匯管區尚可見細小膽管的增生。
上述肝炎基本病變中,肝細胞疏鬆化,氣球樣變,點狀壞死及嗜酸性小體形成對於診斷普通型肝炎具有相對的特徵性;而肝細胞的大片壞死、崩解則是重型肝炎的主要病變特徵。
【臨床病理類型】
各型肝炎病毒引起的肝炎其臨床表現和病理變化基本相同。現在常用的分類是,在甲、乙、丙、丁、戊5型病毒病因分類之外,把病毒性肝炎從臨床病理角度分為普通型及重型二大類。在普通型中分為急性及慢性兩類。急性有急性無黃疸型及黃疸型;慢性有持續性(遷延性)及活動性。重型中又分為急性及亞急性兩種。
1.急性(普通型)肝炎最常見。臨床上又分為黃疸型和無黃疸型二種。我國以無黃疸型肝炎居多,其中多為B型肝炎,一部分為丙型即過去所謂非甲非乙型的一部分。黃疸型肝炎的病變略重,病程較短,多見於甲型、丁型、戊型肝炎。兩者病變基本相同,故一併敘述。
病變:廣泛的肝細胞變性,以胞漿疏鬆化和氣球樣變最為普遍。壞死輕微,肝小葉內可有散在的點狀壞死。嗜酸性小體的出現並非經常。由於點狀壞死灶內的肝細胞索網狀纖維支架保持完整而不塌陷,所以該處通過再生的肝細胞可完全恢復原來的結構和功能。匯管區及肝小葉內也有輕度的炎性細胞浸潤。黃疸型者壞死灶稍多、稍重,毛細膽管管腔中有膽栓形成。
【臨床病理聯繫】
由於肝細胞瀰漫地變性腫脹,使肝體積增大,被膜緊張,為臨床上肝大、肝區疼痛或壓痛的原因。由於肝細胞壞死,釋出細胞內的酶類入血,故血清谷丙轉氨酶(SGPT)等升高,同時還可引起多種肝功能異常。肝細胞壞死較多時,膽紅質的攝取、結合和分泌發生障礙,加之毛細膽管受壓或有膽栓形成等則可引起黃疸。
結局:急性肝炎大多在半年內可逐漸恢復。點狀壞死的肝細胞可完全再生修復。一部分病例(多為乙型、C型肝炎)恢復較慢,需半年到一年,少數病例(約1%)可發展為慢性肝炎。極少數可惡化為重型肝炎。
2.慢性(普通型)肝炎病毒性肝炎病程持續在一年(國外定為半年)以上者即為慢性肝炎。其中B型肝炎占絕大多數(80%),也有近年明確的C型肝炎。按病程、肝功能情況、免疫狀態及病變等的不同將慢性肝炎分為持續性(遷延性)和活動性(進展性)二種。
(1)慢性持續性肝炎(chronic persistent hepatitis,CPH):臨床症状常較輕或僅有肝功能異常。鏡下,肝細胞變性、壞死較急性時減輕,Kupffer細胞增生活躍,匯管區或小葉內慢性炎性細胞浸潤明顯。有時匯管區可因有少量結締組織增生而變寬。肝小葉輪子廓清楚,小葉界板無破壞。肉眼觀,肝體積增大,但表面平滑。此型肝炎一般發展緩慢,經過較好,大多數可以恢復,少數可轉變為慢性活動性肝炎。
(2)慢性活動性肝炎(chuonic active hepatitis,CAH):此型肝炎病變較重,肝功能持續異常。鏡下,肝細胞變性壞死更為廣泛而嚴重。肝細胞壞死呈灶狀或條帶狀,並具有以下二種特徵。①小葉周邊的肝細胞界板受到破壞,界板肝細胞呈灶狀壞死、崩解,伴有炎性細胞浸潤,稱為碎片狀壞死(piecemeal necrosis)(圖10-37);②小葉中央靜脈與匯管區之間或兩個中央靜脈之間出現肝細胞壞死帶,稱橋接壞死(bridging necrosis)。壞死區可出現肝細胞不規則再生。小葉周邊部壞死區纖維組織增生呈星芒狀向小葉內伸展,並與小葉內肝細胞壞死處網狀纖維支架塌陷而膠原化的纖維條索相連接,形成纖維間隔而分割小葉結構。肉眼觀,在腫大的肝表面,上述纖維化明顯區呈不平滑顆粒狀,質地較硬。此型常見於乙、C型肝炎,除肝外,患者還有脾腫大等全身改變,如不及時治癒大都轉入肝硬變。
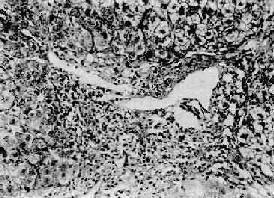
圖10-37 慢性活動性肝炎
肝細胞明顯氣球樣變和嗜酸性變,小葉界板破壞呈現碎片狀壞死,門管區見炎性細胞浸潤
毛玻璃樣肝細胞 多見於HBsAg攜帶者及慢性肝炎患者的肝組織。光鏡下,HE染色切片上,此等肝細胞漿內充滿嗜酸性細顆粒狀物質,不透明似毛玻璃樣故稱毛玻璃樣肝細胞(圖10-38)。這些細胞內含大量HBsAg,電鏡下呈線狀或小管狀積存在內質網池內。用免疫酶標法或免疫熒光法可呈HBsAg陽性反應。(圖10-39)。
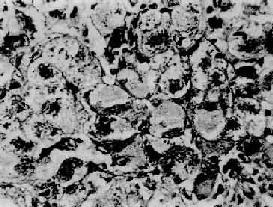
圖10-38 毛玻璃樣肝細胞
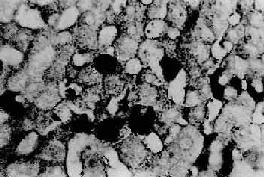
圖10-39 肝細胞內的B型肝炎表面抗原
免疫酶標法(雙PAP)染色顯示肝細胞漿內的HBsAg
3.重量病毒性肝炎本型病情嚴重。根據起病急緩及病變程度,可分為急性重型和亞急性重型二種。
(1)急性重型肝炎:少見。起病急,病變發展迅猛、劇烈,病死率高。臨床上又稱為暴髮型、電擊型或惡性型肝炎。
本型病變可見肝細胞壞死嚴重而廣泛。肝索解離,肝細胞溶解,出現瀰漫性的大片壞死。壞死多自小葉中央開始,向四周擴延,僅小葉周邊部殘留少數變性的肝細胞。肝竇明顯擴張充血並出血,Kupffer細胞增生肥大,并吞噬細胞碎屑及色素。小葉內及匯管區有淋巴細胞和巨噬細胞為主的炎性細胞浸潤(圖10-40)。殘留的肝細胞再生現象不明顯。肉眼觀,肝體積顯著縮小,尤以左葉為甚,重量減至600~800g,質地柔軟,表面被膜皺縮(圖10-41)。切面呈黃色或紅褐色,有的區域呈紅黃相間的斑紋狀,故又稱急性黃色肝萎縮或急性紅色肝萎縮。

圖10-40 急性重型肝炎
肝細胞大片壞死消失,小葉中心部最重,周邊部殘存的肝細胞變性。壞死區有炎性細胞浸潤

圖10-41 急性重型肝炎
肝體積顯著縮小,尤以左葉為著,表面被膜皺縮
臨床病理聯繫及結局:由於大量肝細胞的迅速溶解壞死,可導致:①膽紅質大量入血而引起黃疸(肝細胞性黃疸);②凝血因子合成障礙導致出血傾向;③肝功能衰竭,對各種代謝產物的解毒功能發生障礙。此外,由於膽紅素代謝障礙及血循環障礙等,還可導致腎功能衰竭(肝腎症候群hepatorenal syndrome)。急性重型肝炎的死因主要為肝功能衰竭(肝昏迷),其次為消化道大出血或急性腎功能衰竭等。彌散性血管內凝血(DIC)也較常見,是引起嚴重出血、致死的另一個因素。
本型肝炎如能渡過急性期,部分病例可發展為亞急性型。
(2)亞急性重型肝炎:多數是由急性重型肝炎遷延而來或一開始病變就比較緩和呈亞急性經過。少數病例可能由普通型肝炎惡化而來。本型病程可達一至數月。
病變特點為,既有大片的肝細胞壞死,又有肝細胞結節狀再生。由於壞死區網狀纖維支架塌陷和膠原纖維化,致使再生的肝細胞失去原有的依託呈不規則的結節狀,失去原有小葉的結構和功能。小葉內外有明顯的炎性細胞浸潤。小葉周邊部小膽管增生並可有膽汁淤積形成膽栓。肉眼觀,肝不同程度縮小,被膜皺隔,呈黃綠色(亞急性黃色肝萎縮)。病程長者可形成大小不等的結節,質地略硬。切面黃綠色(膽汁淤積),交錯可見壞死區及小島嶼狀再生結節。
此型肝炎如及時治療有停止進展和治癒的可能。病程遷延較長(如1年)者,則逐漸過渡為壞死後性肝硬變。病情進展者可發生肝功能不全。
【發病機制】
病毒性肝炎的發病是病毒與機體之間相互作用的結果。病毒的量、毒力和侵入途徑與發病有一定關係。小量病毒往往只引起隱性感染,而大量病毒則可導致嚴重的病變。肝炎的病變程度和類型與機體的免疫狀態也有密切關係。現僅就研究較多的B型肝炎的肝損傷及其不同類型的發病機制簡述如下。
(1)肝細胞損傷的機制:B型肝炎病毒侵入機體後進入肝細胞內複製繁殖,然後以「發芽」形式從肝細胞釋出入血。在肝細胞表面則留下病毒抗原成分,此時並不引起明顯的肝細胞損傷。病毒入血後,刺激機體免疫系統產生細胞免疫和體液免疫。前者通過殺傷性T細胞(K細胞)及NK細胞等的直接作用和抗體依賴性的細胞毒作用,後者通過產生各種特異性抗體,均能對血中病毒進行反應加以殺滅。但同時也能對受病毒感染的肝細胞(膜上含病毒抗原成分)進行攻擊,使肝細胞受到破壞發生壞死。一般認為,T細胞介導的細胞免疫反應是病毒感染後引起肝細胞損傷的主要因素。近年研究表明,在細胞免疫反應中,靶細胞抗原不一定只是HBsAg,還可有肝細胞膜脂蛋白及HBsAg。
(2)B型肝炎的發病機制:應用上述肝細胞免疫損傷機制可以解釋B型肝炎出現的不同類型:①T細胞功能正常,感染病毒量多,毒力強時受感染及免疫損傷的肝細胞多而重,表現為急性重型肝炎;②T細胞功能正常,病毒量較少,毒力較弱則發生急性普通型肝炎;③T細胞功能正常,病毒量甚少,毒力很弱則表現為輕型或亞臨床型肝炎;④T細胞功能不足,免疫反應僅能清除部分病毒和損傷部分受感染的肝細胞,未清除的病毒可繼續繁殖並感染,反覆發生部分肝細胞損傷,結果表現為慢性肝炎;⑤機體免疫功能缺陷,T細胞呈免疫耐受狀態,此時病毒與宿主共生。病毒在肝細胞內持續複製,感染的肝細胞也不受免疫損傷,此時則表現為無症状的病毒攜帶者。
參考
|
|||||||||||||||||||||||||||||||||||||||||||
| 關於「病理學/病毒性肝炎」的留言: | |
|
肝小葉界板的灶性壞死稱為—— 什麼? | |
| 添加留言 | |