奧沙利鉑
| A+醫學百科 >> 奧沙利鉑 |
目錄 |
藥物簡介
通用名
奧沙利鉑
商用名
樂沙定(進口);奧正南、艾恆、艾克博康、草鉑、多令、辰雅、佳樂同泰(國產)。
英文名
Oxaliplatin for Injection
性狀
本品為白色或類白色凍干疏鬆塊狀物或粉末. 分子式:C8H14N2O4Pt,分子量:397.29 CAS:61825-94-3
藥理毒理
奧沙利鉑的分類為具有細胞毒作用的其它抗癌藥物,ATC編號L01XA03。
奧沙利鉑屬於新的鉑類抗癌藥,其中鉑原子與1,2 二氨環己烷(DACH)及一個草酸基結合。奧沙利鉑是單一對映結構體。順式-[草酸(反式-1-1-1,2-DACH)鉑]。
奧沙利鉑在多種腫瘤模型系統,包括在人結直腸癌模型中,都表現出廣譜的體外細胞毒性及體內抗腫瘤活性作用。體內、體外試驗也證實在順鉑耐藥的腫瘤模型中,它仍然有效。
在體內和體外研究中,均可觀察到奧沙利鉑與5-氟尿嘧啶聯合應用的協同細胞毒作用。
關於奧沙利鉑的作用機制,雖然尚未完全清楚,但已有研究表明,奧沙利鉑通過產生水化衍生物作用於DNA,形成鏈內和鏈間交聯,從而抑制DNA 的合成,產生細胞毒作用和抗腫瘤活性。
藥代動力學
以130mg/m2的劑量連續滴注2小時,其血漿總鉑達峰值5.1±0.8mg/ml/h,模擬的曲線下面積為189±45mg/ml/h。當輸液結束時,50%的鉑與紅細胞結合,而另外50%存在於血漿中。25%的血漿鉑呈游離態,另外75%血漿鉑與蛋白質結合。蛋白質結合鉑逐步升高,於給藥第五天後穩定於95%的水平。藥物的清除分為兩個時相,其清除相半衰期約為40小時。多達50%的藥物在給藥48小時之內由尿排出(55%的藥物在6天之後清除)。由糞便排出的藥量有限(給藥11天後僅有5%經糞便排出)。在腎功能衰竭的病人中,僅有可過濾性鉑的清除減少,而並不伴有毒性的增加,因此並不需要調整用藥劑量。與紅細胞結合的鉑清除很慢。在給藥後的第22天,紅細胞結合鉑的水平為血漿峰值的56%,而此時大多數的總血漿鉑已被清除。在以後的用藥周期中,總的或不被離心的血漿鉑水平並無顯著升高;而紅細胞結合鉑出現明顯的早期累積現象。
適應症
與5-氟尿嘧啶和亞葉酸(甲醯四氫葉酸)聯合應用 :一線應用治療轉移性結直腸癌 ;輔助治療原發腫瘤完全切除後的III期(Duke』s C期)結腸癌,用於該適應症是基於國外臨床研究結果。
用法用量
限成人使用。
輔助治療時,奧沙利鉑推薦劑量為85 mg/m,靜脈滴注,每2周重複1次。共12個周期(6個月)。
治療轉移性結直腸癌,奧沙利鉑的推薦劑量為85 mg/m,靜脈滴注,每2周重複1次。
應按照病人的耐受程度進行劑量調整(見【注意事項】中「特殊警告和特殊使用注意事項」)。
奧沙利鉑應在輸注氟尿嘧啶前給藥。
將奧沙利鉑溶於5%葡萄糖溶液250-500 mL中(以便達到0.2 mg/mL以上的濃度),持續輸注2-6小時。
奧沙利鉑主要用於以5-氟脲嘧啶續輸注為基礎的聯合方案中。在雙周方案中,5-氟脲嘧啶採用推注與持續輸注聯合的給藥方式。
危險人群
腎功能不全者 :目前尚無奧沙利鉑用於嚴重腎功能不全患者的資料。中度腎功能不全者,開始治療時可給予推薦的劑量。對於輕度腎功能不全者,無需調整劑量。
肝功能不全者 :在I期臨床研究中對於不同程度肝功能不全者,肝膽管異常發生的頻率和嚴重程度可能與疾病進展程度及最初的肝功能紊亂有關。在臨床研究中,對肝功能異常者不需要進行特別的劑量調整。
用法
奧沙利鉑用於靜脈滴注,使用時無需水化。
將奧沙利鉑溶於5%葡萄糖溶液250-500 mL中(以便達到0.2 mg/mL以上的濃度),通過外周或中央靜脈滴注2-6小時。奧沙利鉑必須在5-氟脲嘧啶前滴注。
如果漏於血管外,必須立即終止給藥。
禁忌症
奧沙利鉑禁用於以下病人 :
已知對奧沙利鉑過敏者 ;
哺乳期婦女 ; 在第1療程開始前已有骨髓抑制者,如中性粒細胞計數 < 2 x 10/L和/或血小板計數 <100 x 10/L ;
有嚴重腎功能不全者(肌酐清除率小於30 mL/分)。
【不良反應】
奧沙利鉑與5-氟尿嘧啶/亞葉酸聯合使用期間,可觀察到的最常見的不良反應為 :胃腸道(腹瀉,噁心,嘔吐以及黏膜炎)、血液系統(中性粒細胞減少,血小板減少)以及神經系統反應(急性,劑量累積性,外周感覺神經病變)。總體上,這些不良反應在奧沙利鉑與5-氟尿嘧啶/亞葉酸聯合使用時比單獨使用5-氟尿嘧啶/亞葉酸時更常見、更嚴重。
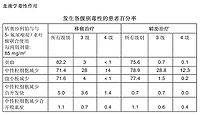
下列表格中顯示的不良反應發生率數據來自轉移癌治療和輔助治療所進行的臨床研究(奧沙利鉑與5-氟尿嘧啶/亞葉酸聯合治療組分別包括416和1108例患者),以及來自上市後經驗。
表格中顯示的不良反應發生率是採用下列標準定義的 : 很常見 (>1/10),常見 (>1/100,≤1/10),不常見 (>1/1000,≤1/100),少見 (>1/10000,≤1/1000) ,以及極少見(≤1/10000),包括個例。
表格後給出了更詳細的信息。
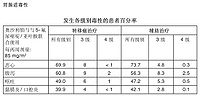
給藥部位情況 :很常見注射部位反應(* 滲漏可能引起局部疼痛和炎症,後者可能很嚴重並引起併發症,尤其是當奧沙利鉑通過外周靜脈途徑輸注時(見【注意事項】中「特殊警告和特殊使用注意事項」)。
自主神經系統異常 :常見面色潮紅。
全身異常* :很常見發熱(發熱很常見,包括感染性-中性粒細胞減少合併或不合併發熱,或免疫源性),疲勞,過敏/過敏性反應(常見過敏反應例如皮疹,尤其是蕁麻疹,結膜炎,鼻炎。常見過敏反應包括支氣管痙攣,血管性水腫,低血壓以及過敏性休克),無力,疼痛,體重增加(輔助治療) ;常見胸痛,體重減輕 (轉移癌治療) ;少見免疫過敏反應,血小板減少,溶血性貧血。
中樞以及外周神經系統異常 * :很常見外周感覺神經病變,頭痛,感覺異常 ;常見頭昏,運動神經炎,假性腦膜炎 ;少見構音障礙。
胃腸道異常 :很常見腹瀉,噁心,嘔吐,口腔炎/黏膜炎,腹痛,便秘,厭食 ;常見消化不良,胃食道返流,呃逆 ;不常見腸梗阻、小腸梗阻 ;少見結腸炎,包括由艱難梭菌引起的腹瀉。
血小板、出血及凝血異常 :很常見鼻出血 ;常見出血,血尿,血栓性深靜脈炎,肺栓塞,直腸出血。
呼吸系統異常 :很常見呼吸困難,咳嗽 ;常見鼻炎,上呼吸道感染 ;少見間質性肺病,肺纖維化**。
皮膚以及皮下組織異常 :很常見皮膚異常,脫髮 ;常見皮膚剝脫 (例如手足症候群),紅斑疹,皮疹,過度出汗,皮膚附屬組織異常。
影響其它感覺器官的異常 :很常見味覺異常 ;不常見耳毒性 ;少見耳聾。
眼睛異常 :常見結膜炎,眼睛功能異常 ;不常見視力敏度一過性減低, 影響視野的異常,視神經炎。
異常實驗室參數 :
血液系統* - 很常見貧血,中性粒細胞減少,血小板減少,白細胞減少,淋巴細胞減少 ;常見中性粒細胞減少合併發燒/中性粒細胞減少合併敗血症(例如3/4級中性粒細胞減少以及明確的感染) 。
生化 - 很常見鹼性磷酸酶水平升高,膽紅素升高,血糖異常,LDH升高,低鉀血症,肝臟酶水平升高(SGPT/ALAT、SGOT/ASAT),血清鈉異常 ;常見血液肌酐水平升高。
- 詳見下面部分。
- 見【注意事項】中「特殊警告和特殊使用注意事項」。
肝膽異常 :極少見(≤1/10000) :肝竇阻塞症候群,又稱為肝靜脈阻塞性疾病,或與此類症状相關的包括紫癜性肝病、肝結節狀再生性增生和竇周纖維化在內的組織學異常。由此,臨床表現可能包括門靜脈高壓症和/或轉氨酶升高。
胃腸道毒性 :
需要使用有效的止吐藥進行預防和/或治療。
嚴重的腹瀉和/或嘔吐可能引起脫水,麻痹性腸梗阻,小腸阻塞,低鉀血症,代謝性酸中毒和腎臟功能的損害,尤其當奧沙利鉑與5-氟尿嘧啶聯合使用時(見【注意事項】中「特殊警告和特殊使用注意事項」)。
神經系統 :奧沙利鉑的劑量限制性毒性反應是神經系統毒性反應。主要表現在外周感覺神經病變,表現為肢體末端感覺障礙或/和感覺異常。伴或不伴有痛性痙攣,通常遇冷會激發。這些症状在接受治療的病人中的發生率為95%。在治療間歇期,症状通常會減輕,但隨著治療周期的增加,症状也會逐漸加重。
病人症状持續的時間,疼痛和/或功能障礙的發生程度是進行劑量調整的指征,甚至有時需要中止治療(見【注意事項】中「特殊警告和特殊使用注意事項」)。
功能障礙包括不能完成精細動作,這種症状可能與感覺障礙有關。當累積劑量接近850 mg/m(或10個周期)時,出現持續症状的危險性接近10%,當累積劑量約為1020 mg/m(或12個周期)時,可達20%。
在大多數情況下,神經系統的症状和體征在治療停止後可以得到改善或完全消退。
在結腸癌的輔助治療中,治療終止6 個月後,87%患者不再有任何症状或者僅有中度症状。在超過3 年的隨訪後,大約3%的患者仍存在持續的、中度的感覺異常(2.3%)或者仍有可能影響日常活動的感覺異常(0.5%)。
已有關於應用奧沙利鉑後出現急性神經感覺症状的報導(見【藥理毒理】中「臨床前安全性研究資料」)。這些症状通常在服藥後幾小時內出現,多發於遇冷空氣時。症状特徵表現為一過性感覺異常、感覺遲鈍或感覺減退,或有可能發生急性咽喉感覺異常症候群。該症候群(其發生率約為1%和2%)主要特徵是伴有吞咽困難和呼吸困難的主觀感覺,但並無任何呼吸困難的客觀徵象(無發紺和缺氧症發生),也不伴有喉痙攣或支氣管痙攣(無哮鳴和喘鳴)。也曾報導出現頜痙攣、舌部感覺異常以及隨後可能出現的語言障礙和胸悶等症状。
雖然發生以上症状時,可以給予抗組胺藥和支氣管擴張劑,但即使不做任何處理,這些症状也可以迅速逆轉。在以後的治療中延長輸注時間可以減少症状的發生率(見【注意事項】中「特殊警告和特殊使用注意事項」)。
奧沙利鉑治療期間還有其它神經學上的症状,如發音困難、腱反射消失及Lhermitte』s 征等的報導。還有視神經炎的個例報導。
過敏反應 :奧沙利鉑與與5-氟尿嘧啶/亞葉酸聯合使用,每2周劑量為85 mg/m,根據患者和級別的過敏反應/過敏發生率 :
轉移癌治療 - 所有級別9.1% ;3級1% ;4級<1%。
輔助治療 - 所有級別10.3% ;3級2.3% ;4級0.6%。
注意事項
不要使用含鋁的注射材料 ;
未經稀釋不能使用 ;
不得用鹽溶液配製或稀釋本品 ;
不要與其它任何藥物混合或經同一個輸液通道同時使用,(特別是5-氟尿嘧啶,鹼性溶液,氨丁三醇,和含輔料氨丁三醇的亞葉酸類藥品)。奧沙利鉑輸完後需沖洗輸液管道。
奧沙利鉑與亞葉酸可通過在注射部位前使用Y 型輸液管連接器同時給予,置Y形管於緊靠靜脈穿刺端, 但是2種藥物不能混入同一個輸液袋中。
亞葉酸必須用等滲溶液,如5%葡萄糖,配製輸注液,不要用鹽或鹼溶液。
輸注奧沙利鉑後,需沖洗輸液管。
只能使用推薦的溶劑(見後)。
如果配製的溶液中有任何沉澱物,都不能再使用,且應該按照法規要求對危險品的處理原則進行銷毀。
【孕婦及哺乳期婦女用藥】
目前尚無資料確定奧沙利鉑在孕婦中使用的安全性。根據臨床前的經驗,臨床推薦劑量的奧沙利鉑可以致死和/或致畸。因此,在孕婦中,不主張用奧沙利鉑。只有在對胎兒的危險性進行了充分的評價並徵得了病人的同意後,方可考慮使用奧沙利鉑。
既往未曾研究過該藥物是否會通過乳汁排泄。在使用奧沙利鉑期間應當避免哺乳。
【藥物相互作用】
在接受5-氟尿嘧啶治療前已接受單劑量奧沙利鉑85 mg/m治療的病人,給予5-氟尿嘧啶的藥物暴露劑量水平沒有什麼變化。
體外研究證明,下列藥物不影響奧沙利鉑與血漿蛋白的結合 :紅霉素、水楊酸鹽、格拉司瓊、紫杉醇和丙戊酸鈉等。
【規格】凍乾粉:50mg, 100mg/瓶.
【國產上市】
原料13家,江蘇恆瑞、哈爾濱三聯藥業等。
注射液2家,齊魯製藥、江蘇海正藥業。
凍乾粉針6家,江蘇恆瑞、江蘇奧賽康等
【進口上市】
1家,比利時Laboratoires Thissen。
|
||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 關於「奧沙利鉑」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |