蒽環類藥物
| A+醫學百科 >> 蒽環類藥物 |
蒽環類藥物(英語:Anthracyclines)或蒽環類抗生素(英語:Anthracycline antibiotics)是一類來源於波賽鏈黴菌青灰變種(Streptomyces peucetius var. caesius)的化療藥物。[1] 它們能夠治療的癌症種類比任何其他類型的化療藥物都要多,並且使用它們的化療是目前最有效的抗癌療法之一;[2][3][4] 可用於治療的癌症包括白血病、淋巴瘤、乳腺癌、子宮癌、卵巢癌和肺癌等。
這類藥物的主要副作用是心臟毒性,這極大程度地限制了它們的進一步使用。其他副作用包括骨髓抑制、嘔吐、脫髮等。
第一個被發現的蒽環類抗生素是柔紅霉素,由放線菌門的波賽鏈黴菌(Streptomyces peucetius)自然產生。不久之後科學家研製出了阿黴素,隨後又有很多衍生物被合成出來(儘管只有很小一部分在臨床上被投入使用)。[2]
目錄 |
例子
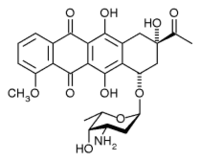
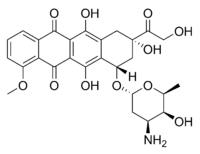
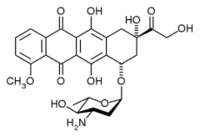
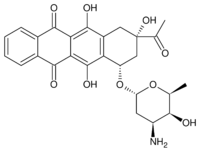
常用的蒽環類藥物包括:
作為抗生素的一種,蒽環類藥物也具有抗菌活性,但由於毒性過大,它們從未被用於治療感染。
作用機理
蒽環類藥物主要有三種作用機理:
- 通過嵌入DNA雙鏈的鹼基之間,形成穩定複合物,抑制DNA複製與RNA合成,從而阻礙快速生長的癌細胞的分裂。[5]
- 抑制拓撲異構酶II,影響DNA超螺旋轉化成為鬆弛狀態,從而阻礙DNA複製與轉錄。有研究顯示拓撲異構酶II抑制劑(除蒽環類藥物還包括依託泊苷等)能夠阻止拓撲異構酶II的翻轉,而這點對於它從它的核酸底物上脫離是必需的。這就意味著,拓撲異構酶II抑制劑使拓撲異構酶II的複合物在DNA鏈斷裂之後才能更穩定,導致後者催化了DNA的破壞;同時,拓撲異構酶II抑制劑還能阻礙連接酶對DNA的修復。[6][7]
- 螯合鐵離子之後促進破壞DNA和細胞膜的自由基的生成。[5]
心臟毒性
蒽環類藥物以其嚴重的心臟毒性而著稱。這種心臟毒性可能由許多因素引起,包括對心肌細胞肌質網上蘭尼鹼受體的影響、心臟中自由基的產生及藥物代謝產物的蓄積。它們的心臟毒性通常表現為心電圖變化(尤其是QRS複合波的頻率變化)和心律不齊;心肌病及其引發的心力衰竭(有時數年後才表現出來)也時有發生。毒性主要與患者終生累積劑量有關。因此,在治療的過程中,醫生會根據藥物種類及患者情況計算所適用的終生劑量,當劑量達到上限的時候,一般來說會停止繼續使用蒽環類藥物(或者重新估算上限)。[8]
有研究顯示蒽環類藥物引起心力衰竭的幾率不僅與劑量有關,還隨著接受治療之後的時間的推移而增加——由2年之後的2%到15年之後的5%。[9]
除了保持在累積劑量上限以下之外,腫瘤科醫生還會使用許多其他方法降低心臟毒性。一般來說,在化療結束的3、6、9個月之後醫生會建議檢查一次心臟。此外,保護心臟的措施還包括了使用右雷佐生輔助化療,使用脂質體藥物,和改用持續靜脈滴注:[8]
- 右雷佐生是一種心臟保護劑,能夠通過競爭性螯合鐵離子來減少蒽環類藥物產生的自由基數目。研究顯示它能夠將心臟毒性發生幾率減少約三分之二,同時並不影響化療的效果或者是總體生存率。[10]
- 相對於普通蒽環類藥物來說,較少的脂質體藥物會被運輸到心臟,因此毒性較小。[11]
- 持續靜脈滴注能夠減小藥物在心臟(尤其是左心室)中的的峰濃度。[8]
另見
參考資料
- ↑ Fujiwara, A.; Hoshino, T.; Westley, J. W.. Anthracycline Antibiotics. Critical Reviews in Biotechnology. 1985, 3 (2): 133. doi:10.3109/07388558509150782.
- ↑ 2.0 2.1 Weiss RB. The anthracyclines: will we ever find a better doxorubicin?. Semin. Oncol.. December 1992, 19 (6): 670–86. PMID 1462166.
- ↑ Minotti G, Menna P, Salvatorelli E, Cairo G, Gianni L. Anthracyclines: molecular advances and pharmacologic developments in antitumor activity and cardiotoxicity. Pharmacol. Rev.. June 2004, 56 (2): 185–229. doi:10.1124/pr.56.2.6. PMID 15169927.
- ↑ Peng X, Chen B, Lim CC, Sawyer DB. The cardiotoxicology of anthracycline chemotherapeutics: translating molecular mechanism into preventative medicine. Mol. Interv.. June 2005, 5 (3): 163–71. doi:10.1124/mi.5.3.6. PMID 15994456.
- ↑ 5.0 5.1 Takimoto CH, Calvo E. "Principles of Oncologic Pharmacotherapy" in Pazdur R, Wagman LD, Camphausen KA, Hoskins WJ (Eds) Cancer Management: A Multidisciplinary Approach. 11 ed. 2008.
- ↑ Osheroff Neil, Eukaryotic Topoisomerase II: characterisation of enzyme turnover, 1986, The Journal of Biological CHemistry, vol. 261, no. 21, pp. 9944-9950
- ↑ Peter Buhl Jensen et al., Different modes of anthracycline interaction with topoisomerase II: Separate structures critical for DNA-cleavage, and for overcoming topoisomerase II-related drug resistance, 1993, Biochemical Pharmacology, vol. 45, no. 10, pp. 2025-2035
- ↑ 8.0 8.1 8.2 Minotti, G.; Menna, P.; Salvatorelli, E.; Cairo, G.; Gianni, L.. Anthracyclines: Molecular Advances and Pharmacologic Developments in Antitumor Activity and Cardiotoxicity. Pharmacological Reviews. 2004, 56 (2): 185–229. doi:10.1124/pr.56.2.6. PMID 15169927.
- ↑ Kremer L, van Dalen E, Offringa M, Ottenkamp J, Voûte P. Anthracycline-induced clinical heart failure in a cohort of 607 children: long-term follow-up study. J Clin Oncol. 2001, 19 (1): 191–6. PMID 11134212.
- ↑ van Dalen EC, Caron HN, Dickinson HO, Kremer LCVan Dalen, Elvira C. . Cardioprotective interventions for cancer patients receiving anthracyclines. 考科藍實證醫學資料庫. 2008 (2): CD003917. doi:10.1002/14651858.CD003917.pub3. PMID 18425895.
- ↑ Forssen, E. A.; Tökes, Z. A.. In vitro and in vivo studies with adriamycin liposomes. Biochemical and biophysical research communications. 1979, 91 (4): 1295–1301. doi:10.1016/0006-291X(79)91207-5. PMID 526304.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
參考來源
| 關於「蒽環類藥物」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |