營養學/維生素A
| 醫學電子書 >> 《臨床營養學》 >> 維生素 >> 維生素A |
| 臨床營養學 |
|
|
(1)維生素A 維生素A亦名視黃醇(Retinol,VA),在自然界中的多是全反式棕櫚酸酯。他的衍生物具有特殊的生理功能,如視黃醛(Retinyl Aldehyde,VA醛)對暗適應有效;甘露糖視黃醇磷酸(MannosylRetiny Phosphate,MRP)也具有某些生理功能。VA衍生物的分子式列於圖5-1,活性列於表5-2。
維生素A及其衍生物易氧化。氧化劑MnO2可使之成為醛,還原劑雙可將維生素A酸還原到要醛或醇。對鹼較穩定,但對酸不穩定,使其脫氫或將雙鍵重新排列。在光或碘的作用下,全反式可變為較穩定的11順式異構體。在強光下形成二聚體或多聚體。
(2)胡蘿卜素 植物中胡蘿卜素在體內分解為維生素A,並具有維生素A的生理作用。
表5-2 維生素A及基其衍生物的活性
| 化學變化 | 產物 | 生物活性 |
| 酯化 | 自然及人工產品 | 100 |
| 氧化 | 醛 | 100 |
| 順式異構 | 順式異構體 | 23~75 |
| 醚 | 苯及甲基醚 | 10~100 |
| 脫氫 | 維生素A2(3-脫氫視黃醇) | 30 |
| 失去氧 | Axerophene | 10 |
| 酮 | C21-酮 | 3 |
| 去甲基 | 新維生素A | 3 |
| 增加-CH2- | 高維生素A | 1.5 |
| 脫水 | 脫水維生素A | 0.4 |
| 氧化 | 環氧物 | 0 |
| 氫化 | 二氫維生素A等 | 0 |
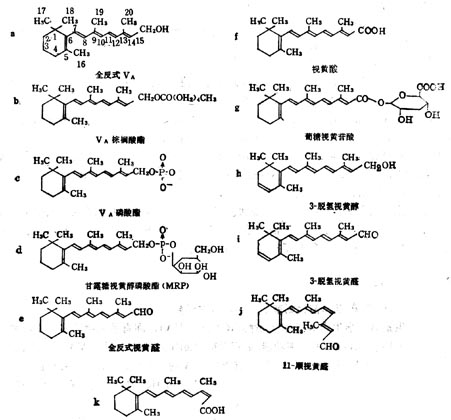
圖5-1 維生素A衍生物的分子式
β-胡羅卜素含有兩個β-紫羅蘭酮環(β-Ionone ring)和四個異戊二烯側鏈,加水斷裂為兩分子維生素A如圖5-2。但實際上膳食中β-胡蘿卜素只有1/6右變為維生素A。自然界中有環與維生素A相同,他們的維生素A活性低於β-胡蘿卜素,有的沒有與維生素A相似的環,沒有生物活性(表5-3,5-4)。
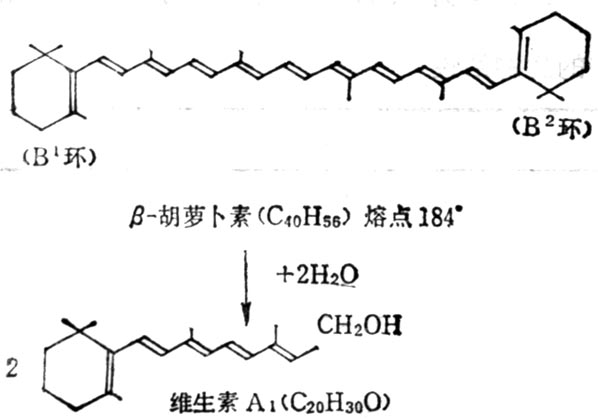
圖5-2 β-胡蘿止素水解為維生素A
5.2.2 維生素A及胡蘿卜素的代謝
(1)胡蘿卜素的吸收 胡蘿卜素的微膠粒溶液在小腸內吸收。油溶液中者吸收最好,磷脂有助於形成微膠粒溶液而利於吸收。膽鹽不但促進胡蘿卜素運輸至腸細胞,助其與細胞表面相結合,並促進胡蘿卜素的分解。維生素E及其他抗氧化劑可保護側鏈的共軛雙鍵系統免於氧化。胡蘿卜素進入到小腸細胞內,在胞漿內胡蘿卜素雙氧化酶(Carotene Dioxygenase)作用下,將1mol氧加入到中間位置的雙鍵上,將其分解為視黃醛,但也可從一端將其分解生成具有與維生素A相同的環,側鏈較長的醛即apo胡蘿卜醛。所生成的醛雙為脫氫酶作用還原為醇再酯化。小腸及肝都有胡蘿卜素雙氧化酶,但其活力以小腸中者較高,以器官計,腸為肝的2倍,以重量計為4~7倍。靜脈注射β-胡蘿卜素,在肝中也可轉變為視黃醇,也以視醇酯形式儲存,但能力有限。
胡蘿卜素吸收是擴散性的,其吸收量與劑量大小有相反關係。類胡蘿卜素都可吸收進入血漿內。血漿中的類胡蘿卜素可分為β-胡蘿卜素、葉黃素,番茄紅素及其他類胡蘿卜素,視攝入情況而定。可存在於肝、脂肪、腎、皮膚及血管粥樣硬化的斑塊中。
表5-3胡蘿卜素化合稱的環結構
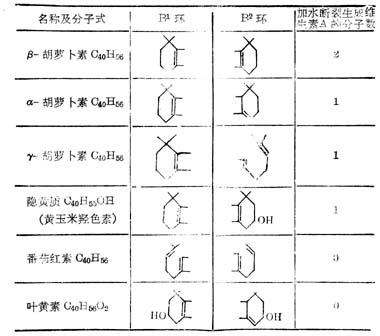
表5-4 類胡蘿卜素化合物的生物活性(以β-胡蘿卜生物活性為100%)
| 類胡蘿卜素 | 活性 | 類胡蘿卜素 | |
| β-胡蘿卜素 | 100 | β-半胡蘿卜素 | 有 |
| α-胡蘿卜素 | 50~54 | β-apo-8'-胡蘿卜醛 | 72 |
| γ-胡蘿卜素 | 42~50 | β-apo-8'-胡蘿卜酸 | 有 |
| β-新胡蘿卜素 | 20~40 | 脫水葉黃素 | 21 |
| 3,4去氫-β-胡蘿卜素 | 75 | 玉米黃素(隱黃質) | 57 |
| β-胡蘿卜素 | 21 | 反-順異構體比全反式的活性要小 | |
| β-胡蘿卜素 | 50 |
(2)維生素A的吸收及儲存維生素A為主動吸收,需要能量,速率比胡蘿卜素要快7~30倍。食物中的維生素A為酯式,經腸中胰液或絨毛刷狀緣中的視黃酯水解酶分解為游離式進入到小腸壁內,又為腸內細胞微粒體中的酯酶所酯化,合成維生素A棕櫚酸酯,攝取維生素A3~5h後,吸收達到高峰。維生素A也需要膽鹽。維生素E也可防止維生素A氧化破壞。維生素A與乳糜微粒相結合由淋巴系統輸送到肝,酯式水解進入肝,然後又再酯化為棕櫚酸酯。肝實質細胞負責攝取及新進入的維生素A代謝,一部分維生素A由實際細胞轉入類脂儲存細胞(Lipocyte),這種細胞中有許多類脂滴,如維生素A攝取量大,這些類脂滴大而多。85%的維生素A在類脂滴中,還有一些在高爾基體中。
維生素A的吸收與儲存量均較大,大鼠每可吸收20,000IU。若維生素A攝入速度很快,VA酯與脂蛋白的結合已達飽合,多餘者以酯式流入到血漿中。每日給大鼠50,000IU,4周後給以無維生素A膳食3周,血漿中維生素A酯較正常者多,而維生素A值正常。一方面由於組織的需要,維生素A從肝中釋放經血流到靶組織,另一方面過剩的維生素A也從肝到血流中。
高蛋白膳食可以增加維生素A的利用,因而加速維生素A儲存的空竭(Depletion)。蛋白質營養不良時,維生素A的吸收及胡蘿卜素轉變為維生素A的能力都受到影響,因而使維生素A的肝儲存量降低。懷孕可使儲存量增加,大鼠孕娠17~21天時,肝儲存可增加2倍,為製造維生素A豐富的初乳及乳汁作準備。胎兒維生素A儲存量甚少,不受母親營養情況的影響。初生嬰兒肝維生素A濃度僅為成人1/10。60歲以後儲存量又低於成人。肝儲存量可能與性別有關係,雌鼠比雄鼠儲存較多。吃維生素A缺乏飼料,雄鼠肝儲存空竭比雌鼠要快。男性的血清維生素A水平比女性稍高。夜盲的發生亦以男性較多。腎臟內也能儲存維生素A,但其量僅為肝的1%。眼色素上皮組織內的維生素A是以酯式存在的,專為視網膜使用而儲備,其空竭速率比肝中者要慢一些。
(3)維生素A的運輸當靶組織需要維生素A時,維生素A從肝中釋放出來,運輸到靶組織。這個過程首先將肝內儲存維生素A酯經酯酶水解為醇式,與視黃醇結合蛋白(Retionl BindingProetin,RBP)結合,再與前白蛋白(Prealbumin,PA)結合,形成維生素A-RBP-PA複合體後,才離開肝臟。經血流入靶組織。維生素A在一般情況下必須與蛋白質結合,使之具有水溶性,並較穩定。此外,還可減少維生素A對細胞的毒性,因細胞膜對複合體有識別能力,但對未結合的維生素A無識別力,以致對維生素A的攝取失去控制,過多維生素A進入細胞而產生毒性。
RBP為肝實質細胞合成的多肽,分子量21,000,電泳在α部分。肝每天能合成190mg,一分子RBP與一分子維生素A結合。維生素A-RBP-PA進入血流中,由於分子較大,不能從腎臟濾出。血流中RBP的水平受維生素A的影響,如果無維生素A可資運輸時,RBP則積累於肝內。正常血漿RBP水平為40~50μg.m-1,維生素A缺乏的夜盲症状出現時,RBP則降為20μg.m-1。蛋白質缺乏,RBP合成減少,維生素A-RBP不能形成,維生素A結合的RBP-PA,其量為正常值的20%,但已變性,不能再與維生素A結合。PA的血漿濃度受維生素A營養狀況的影響較少,其正常值為200~300μg.m-1,他不但與RBP結合,而且也與甲狀腺素結合,兩者互不影響。
維生素A-RBP-PA複合體隨血流到腸粘膜、膀胱、角膜及上皮組織等靶細胞後,細胞膜上有RBP的特殊受全,可與RBP結合,並將維生素A釋放出來,進入細胞內。RBP與維生素A分開後已變性,喪失與維生素A,PA或細胞膜上受體的結合能力。此種游離的RBP在腎小球中可濾過,而在腎小管重吸收,為腎皮層細胞所攝取,並在其溶酶體中分解為胺基酸。血漿中還有一種未與PA結合的維生素A-RBP,其量約為1μg.m-1。這部分可從腎小球濾過,在腎小管中重吸收,並漿維生素A釋放出來。因此腎中有少量維生素A積累,然後酯化輸送至肝。
維生素A進入到靶細胞後,立即與細胞視醇結合蛋白(Cellular retinol Binding Protein,CRBP)相結合。維生素A酸在運輸過程中不需要與RBP相結合,但進入細胞內必須視黃酸結合蛋白相結合。
肝病患者的血漿蛋白合成受到影響,RBP及PA水平偏低而影響維生素A的血漿水平。腎病患者RBP分解代謝減弱,使RBP值增高。但囊纖維變性患者,肝內維生素A儲存量適當,但血漿中RBP、PA及維生素A的水平均低。RBP也受內泌的調節,雄性動物血漿的RBP水平比雌性高。月經期或口服避孕藥的婦女的RBP都有變化。新生兒的RBP只有成人的一半。這種水平一直維持至青春期,以後將增高。
(4)維生素A分解代謝及排出維生素A分解代謝途徑可能如圖5-3。視黃醇通過氧化轉變為維生素A酸,其中一部分異構為β順式。全反式或β順式者均為維生素A的代謝產物,有維持上皮組織分化的活性,但體內不能儲存,很快消失。注射維生素A酸4h後,肝中只剩下10%,24h後肝中已無。以後5,6位環氧化形成5,6環氧維生素A酸(5,6-epoxyretinoic acid)或環上4位羥基化,再進一步氧化形成4-氧-絡維生素A酸(4-oxo-Retinoicaxcid)或形成葡萄視黃苷酸(retinoylglucronide)。大鼠注射標記維生素A酸後,在膽汁中60%為維生素A酸及基葡萄糖苷酸,少於40%的為13順式葡糖視黃苷酸,還有少量5,6位從環氧維生素A酸及基葡萄糖視黃苷酸為0.2~0.4μg,這些維生素A代謝從膽汁流入小腸,形成肝腸循環。正常大鼠注射標記維生素A酸2h後,在小腸中的放射性約佔劑量的7.2%,而膽道插管者僅為2.4%。在腎臟中也有維生素A代謝物。大鼠經胃給以標記的視黃醇或其酯後,在腎臟中除攝入物外,尚有全反式維生素A酸及5,6位環氧維生素A酸,但在血漿中並未發現後者,這種氧化作用可能僅在靶組織(如腎)中發生。他的活性僅為維生素A酸之1%,生物半壽期很短。
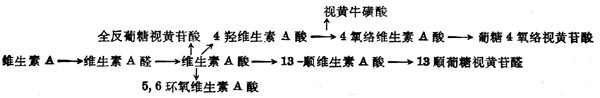
圖5-3 維生素A的氧化代謝的可能途徑
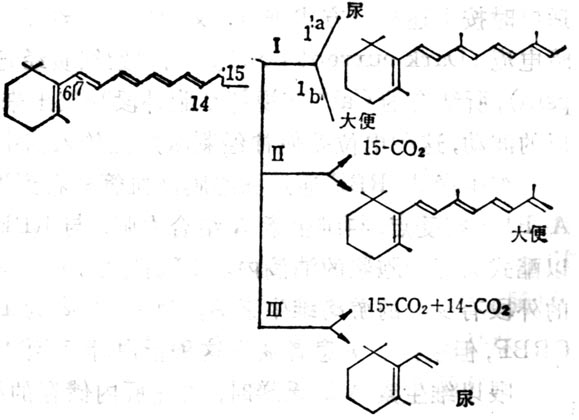
圖5-4 維生素A的氧化代謝的可能途徑
大鼠攝入維生素A後,大便及尿中都有其代謝物的排出。2/3排出物的異戊二烯側鏈部分無改變。也有15-C氧化為CO2,有的側鏈氧化分解成CO2及短鏈產品。大鼠給以20μg維生素A後,大便中排出以葡糖視苷酸為主,為主要排出途徑,大便排出量變化較大,第2,3天達到高峰,約為劑量的9%,然後下降到較小數量。尿中排出24h內為劑量的8.7%,其中一半為水溶性者,一半為脂溶性者,尿排出量逐漸下降至第八天達到穩定,約為0.55%。尿中代謝產物β-紫羅蘭酮環部分可氧化,甲基可脫去側鏈中的雙鍵可飽合,鏈也可縮枯木短。水溶性代謝物目前了解很少。
肝內儲存的及攝入的維生素A都能被補充到需要維生素A的靶組織中去。因此,肝內維生素A的靶組織中。因此,肝內維生素A的儲存量能影響維生素A的代謝率(即維生素A轉變為尿及大便中維生素A代謝物之量)。SauberLich測定人的代謝率每天570~1250μg,這種差異由於肝儲存量不同所致。注射標記維生素A,在試驗中,發現維生素A有三種不同速率從尿中排出,亦即有三種不同代謝庫:代謝庫1代表新吸收的維生素A;代謝庫2代表功能性和非功能性的維生素A;代謝庫3代表功能性的代謝。在肝內儲存空竭後的代謝率,才代表靶組織的功能性代謝率。新吸收的維生素A與體內儲存者不同,二者在24h內不混合,血漿中新吸收者佔90%,內源者僅佔10%,二者逐漸混合,大鼠至第八天才完全混合。如果肝中維生素A儲存量少,新吸收者在血漿中比例大,持續時間較長。如果肝儲存量為0.6μg.m-1時,新吸收者由於其他維生素A已經空竭,需要維生素A補充,不能儲存於肝內,而進入其他組織如腎等。若維生素A儲存量較多時,肝儲存量為18μg.m-1,60%存於肝內。從代謝庫2來看,非功能性的代謝,即代表肝儲存維生素A的分解。所以維生素A空竭的速率隨維生素A儲存量的指數而變化。大鼠的維生素A肝儲存量可為全部生命需要量的數倍,但也可空竭,人體也是如此,儲存量高代謝率亦高,攝入量高,代謝率也高。
5.2.3 生理功能
維生素A具有維持正常生長、生殖、視覺及抗感染的功能,但其作用機理迄今尚未完全清楚。
(1)維生素A與視覺的關係視網膜上有兩種視細胞,即視桿細胞與視錐細胞,人類前者數量多,與暗視黨有關;後者數量少,與明視覺及色覺有關,他們都有視色素,由視蛋白與生色團組成。各種動物的細胞的視蛋白不同,生色團由不同類型的維生素A醛組成。視桿細胞外段含有視色素是感光部分。視桿細胞膜連續不斷地內陷,折起形成片層膜結成,每一層膜又由兩層脂類分子膜由兩層脂類分子膜構成稱為雙分子膜。視色素鑲嵌在這種脂類雙分子膜中。視色素視紫紅質,由維生素A醛與視蛋白結合而成。維生素A醛由維生素A氧化而來,經異構酶作用使其變為11-順式維生素A醛。維生素A醛由維生素A氧化而來,經異構酶作用使其變為11-順式維生素A醛。維生素A醛由視蛋白之間的一級結構是11-順維生素A醛的醛基與視蛋白中賴氨酸ξ氨基形成希夫鹼(Schiff base)鍵,隨之引起視蛋白高級結構改變,產生相互保護的二級結構,在黑暗中非常穩定。當光照時,一個視紫紅質接受一個光子後,維生素A醛在11-C上扭成轉成全反維生素A醛,視蛋白的立體構形也發生變化,維生素A醛又經視細胞外端的維生素A還原酶使成其變為維生素A,然後由色素上皮細胞微粒體中酯酶將其酯化而儲存於色素上細胞內,需要時再異構為11-順維生素A。暗適應按上述相反方式進行,又形成視紫紅質。暗時Na+從視桿細胞內段移到外段,形成暗電流(Dark current flow)。當視紫紅質經光異構後變為前光視紫紅質(Prelumirhodopsin),所結合的Ca2+在視桿細胞外段釋放出來,中止了Na+流動及暗電流,其結果產生電壓的波動,這種電位差使神經刺激加強傳入腦中發生光感,也可用視網膜電圖測定。
維生素A-RBP通過脈絡膜微血管分布到視網膜上皮組織,其細胞表面有維生素A-RBP接受點,與維生素A結合力強,與RBP結合弱,維生素A進入到色素上皮細胞內以酯式儲存於胞漿的油滴內。暗適應的眼中,有一半的維生素A為11-順式,在視桿細胞的外段有少量的游離維生素A,其中60%為11-順式,生理上很重要,視網膜細胞中有CRBP,但視網膜炎患者缺少這種蛋白,因而維生素A不能進入到細胞內。
喂以維生素A缺乏膳食時,首先肝內儲存的維生素A釋放供給其他組織,肝的儲存量下降,血漿維生素A正常。當肝儲存量將近空竭時,血漿維生素A水平才下降,但由於視網膜的色素上皮組織有維生素A積累,視紫紅質的維生素A醛下降較慢。色素上皮細胞內維生素A缺乏時,才有夜盲症出現。若視桿細胞內視紫紅質減少,影響光的吸收,電流也減少。如視紫紅質為正常值之74%,光閾上升14倍,若為正常值之16%,光閾上升680倍,維生素A非常缺乏時,光蛋白也減少,視細胞可以溶解。
(2)對糖蛋白質合成的影響 缺乏維生素A的動物的某組織,如小腸、角膜、氣管上皮組織及血清等的特殊糖蛋白減少,給以維生素A或維生素A酸可以促進其合成。細胞膜表面的蛋白主要為糖蛋白,細胞膜的功能如接觸抑制、分化及識別環境的能力,可能與糖蛋白有關。膜上有糖基視黃醇磷酸,所以,維生素A可能與膜的糖蛋白合成有關。免疫球蛋白也是糖蛋白,維生素A營養狀況影響免疫功能,可能與此有關。
糖蛋白的合成步驟,首先為合成多肽鏈,然後納入單糖,單糖與多肽鏈上的絲或蘇氨酸的羥基或門冬醯胺相偶聯形成糖蛋白。糖蛋白中的糖為甘露糖、岩藻糖、半乳糖、葡萄糖及乙醯葡萄胺。糖蛋白的合成需要脂類-糖作為中間體,其中脂類多為異戊二烯醇類的多萜醇或視黃醇。將單糖從GDP-單糖或UDP-章糖轉移到維生素A或多萜醇上。如章糖為甘露糖結合到維生素A上,則生成甘露糖視黃醇磷酸酯(Mannosylretinylphosphate,MRP),若結合到多萜醇上生成甘露糖多萜醇磷酸酯(Dilichylphosphomannose,DMP),再將單糖轉移至糖蛋白上。
維生素A在糖蛋白合成中變化分為三個步驟:①形成維生素A磷酸酯(Retinylphosphate,RP);②由RP合成MRP,這一步驟在微粒體內合成;③將單糖轉移至糖蛋白上(圖5-5)。
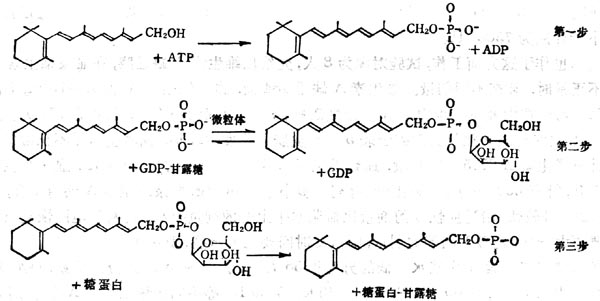
圖5-5 VA在糖蛋白合成中的作用
MRP與DMP都是蛋白糖基化的中間體,由MRP合成的糖蛋白的分子量比從DMP合成要小一些。維生素A缺乏的倉鼠肝微粒體合成的MRP少而合成的DMP多。有些特殊蛋白,如大鼠血清糖蛋白(α1-巨球蛋白)的合成需要VA,他在肝內合成,含有2~7%甘露糖。維生素A嚴重缺乏時,降低至正常值的20%。維生素A的靶組織(肝、膽管、腸)的上皮組織中,都有MRP或半乳糖視黃醇磷酸酯。維生素A可使上皮細胞正常,呈柱狀分泌粘液。維生素A缺乏時,上皮組織鱗狀變形而角化。維生素A在糖蛋白合成中的作用與上皮組織的生理功能的關係,尚須進一步研究。
5.2.4 來源
動物的肝、腎、蛋及奶中的都有維生素A,尤以肝中最豐富,綠色蔬菜及紅黃色蔬菜與水果中有胡蘿卜素,但各種胡蘿卜素的生物效用不一樣,以β-胡蘿卜素最高。供應量為1500~4000IU時,食物中1μgβ-胡蘿卜素相當於0.167μg的維生素A,其他胡蘿卜素僅為其一半。植物中有些黃紅色素並無維生素A的效用(表5-4)。
胡蘿卜素為脂溶性的,在動植物中與脂類相結合,在消化道中可以酶解,烹調中胡蘿卜素比較穩定。我國的炒菜方法,胡蘿卜素的保存率為76~94%,如烹調時間短,用水量少,溫度低都可減少損失。植物老化過程中,胡蘿卜素轉變為環氧化合物,為氧化破壞的第一步。加工烹調及儲存過程也容易異構,減少生物活性,食物加工中使用亞硫酸,產生自由基,對胡蘿卜素也有破壞作用。食品製作方法也影響胡蘿卜素的利用。胡蘿卜片的胡蘿卜素76%由大便排出,在勻漿中者只有44%排出。
5.2.5 需要量的研究
VA過去以國際單位IU表示,現在以視黃醇當量RE表示,
1視黃醇當量=1μg維生素A
二次大戰時,英國醫學研究會給16人以維生素A缺乏膳食作為試驗組,為期61/2~25個月。7人為對照組(其中2人每日補充25IU維生素A,5人每日補充5000IU胡蘿卜素)。當被試者有缺乏症状後,補充不同劑量的維生素A或胡蘿卜素以測定需要量,在此研究中觀察指標較多,但僅血漿維生素A及暗適應較為靈敏。結果最低需要量為1300IU維生素A,1500IU胡蘿卜素(從大便中排出者不計算在內),正常需要量為2500IU維生素A,胡蘿卜素為3000IU,但各種食物的胡蘿卜素有效劑量不一樣,所以正常需要量以食物中胡蘿卜素計應為7500IU。
美軍也作了這方面工作,試驗對象為8人,先給以維生素A缺乏膳,在血漿維生素A及視力不正常時,補充不同劑量。維生素A缺乏184天,血漿維生素A從57~78μg%降至20~32μg%。視力及血漿維生素A顯出缺乏症的最短時間為361天,最長為771天。血漿維生素A濃度與缺乏症的關係列於表5-5。皮膚角化發生較早,視網膜電圖不正常發現較晚。補充維生素A37.5~150,血漿維生素A上升不明顯,補充300μg,血漿維生素A略有上升,補充600μg者,明顯上升,補充胡蘿卜素1200μg,血漿維生素A略有上升,補充2400μg上升較快,暗適應恢復的劑量比漿水平上升的劑量要小,視網膜電圖恢復正常的劑量要更大一些,若攝入同等的劑量。則恢復時間要延長一些(表5-6)。
我國曾將維生素A血漿水平低的男青年56人(血漿30~65IU),分成7組,每組8人,分別給以400,2000,3100,3500,3800,4500,5500IU等不同劑量維生素A。試驗期為11周,觀察血漿維生素A、暗適應及生理盲點的變化,每日入2000~3000IU者,血漿維生素A水平略有上升,但未達到100~120IU%,3500~5000IU者,在9周時使血漿維生素A達到100IU%,11周時維持在107~130IU%,這次試驗未觀察到暗適應的變化,但在試驗初期,幾乎所有試驗對象都有生理盲點擴大的現象,攝取量為400IU者,生理盲點繼續擴大,一次,000,000IU大劑量,24h內恢復正常。攝取量2000~3000IU兩組,至11周時恢復正常,攝取量3500IU以上的各組,至5~9周時大都恢復正常。因此,維生素A供應量為3500IU時,不僅能使血漿維生素A達到正常,而且生理盲點也正常。上述三次人體試驗的地區、人種、工作不同,但其維生素A正常需要量均為1200~1300μg。
表5-5 美軍維生素A缺乏症狀與相應的血漿濃度
| 維生素A血漿濃度μg% | |||
| 被試者 | 暗適應不正常 | 視網膜電圖不正常 | 皮膚角化 |
| 1 | 22~24 | 9~11 | 29~35 |
| 2 | 25~30 | 未發現 | 32~37 |
| 3 | 20~25 | 未發現 | 29~38 |
| 4 | 4~5 | 7~10 | 20~25 |
| 5 | 4~8 | 4~8 | 5~10 |
| 65 | 30~35 | 未發現 | 25~30 |
| 7 | 2~5 | 5~9 | 13~ 20 |
| 8 | 3 | 5~10 | 20 ~ 24 |
表5-6 美軍維生素A需要量
| 維生素A需要量 | ||
| 維生素A(μg/日) | β-胡蘿卜素(μg/日) | |
| 暗適應正常 | 150~300 | 300~600 |
| 視網膜電圖正常 | 300~600 | 600~1200 |
| 皮膚正常 | 600 | 1200 |
| 血漿維生素A水平大於20μg% | 600 | 1200 |
| 大於30μg% | 1200 | 2400 |
①血漿30μg%以上肝儲存量為中等水平。維生素A代謝率為570~1250μg。
5.2.6 臨床應用
維生素A除用以防治缺乏病外,尚用以治療皮膚角化,並對某些癌有預防作用。
(1)維生素A與皮膚病維生素A可抑制皮膚角化,維生素A酸也有這種功能,但它不儲存於肝內,運輸不需要RBP,可進入組織中,迅速代謝,很快從體內消失,毒性較少。所以用維生素A酸及其衍生物治療毛囊角化、痤瘡等。β-順式維生素A及芳香族維生素A酸衍生物(如Etretinate)療效分別為全反式維生素A酸的2.5及10倍。β-順式維生素A酸用以抑制皮脂形成治療痤瘡有效。用Etretinate治療牛皮癬及其他衍生物可迅速達到上皮真皮。
(2)維生素A癌維生素A可維持正常上皮組織的分化,維生素A缺乏的某些組織的形態變化與某些上皮組織癌症的早期病變(癌前期)相近,都是上皮組織鱗狀變形。因此,維生素A可能在這一階段中,對癌細胞起迴轉修復作用。維生素A缺乏,可能增加某些靶組織對致癌物質的敏感性。維生素A只在癌前期起作用,到第三期癌出現後已無效。大鼠的試驗證實上述說法。
攝取大量的維生素A,儲存於肝,血液中含量受到RBP的 限制,到靶組織之量有限。預防癌變也多用維生素A酸。現在正研製無毒或毒性較小而又能作用於靶組織的維生素A酸衍生物:①β-紫羅蘭酮環的改變,β變為α,或變為二甲基乙醯戊烯環。如3甲基甲氧基環已烯環酸即Etretinate,可以有效地減低吸煙者的氣管組織變形,膀胱癌複發病也減低;②側鏈上的改變,9,11,13共軛雙鍵為維生素A活性必要部分,必須保留。順式異構體有活性,β-順式維生素A酸最先臨床應用於防治膀胱癌呼吸道癌,但他的毒性比維生素A酸酯或維生素A乙基醯胺要大;③末端極性基團的改變,維生素A甲酯或丁酯毒性低,活性高,肝中積累少,而在乳腺中較多,可用以預防乳腺癌的誘導,但尚未用於人體。
維生素A對免疫系統也有影響,他不但對疾病抵抗力有關。而且對一病毒引起的癌也有預防作用。小鼠黑瘤癌細胞移植給小鼠,未補充維生素A者,75%在3~5周內發展成瘤,而補充維生素A(每日IU,共補充5日者僅5%有瘤。關於這方面工作也在進行。
維生素A對癌預防作用可能由於它與核作用使基因改變。維生素A靶細胞中有維生素A或維生素A酸結合蛋白(CRBP,CRABP),維生素A或維生素A酸與之結合後,可能被攜帶運輸至細胞核從而改變基因,影響細胞分化。CRBP在腎、肝、小腸、肺、脾、眼及睾丸中較多,而血清、腦、肌肉、脂肪、心臟中較中少。CRABP在胚胎及未分化的組織中多,有些癌組織中,CRABP的量比正常組織中者要多。組織中CRBP及CRABP之量決定維生素A或維生素A酸及其衍生物的生物作用。不同癌組織對維生素A及其衍生敏感性可能取決於細胞中CRABP之不同。
維生素A及胡蘿卜素也試用於輔助治療。癌在切除、放療及化療後,可使癌細胞水平降至低水平。維生素A或胡蘿卜素對殘餘的癌細胞的分裂起到抑制作用,從而減少複發率或延長潛伏期。
(3)胡蘿卜素與癌 流行病學調查中發現肺癌的發病率與胡蘿卜素攝取量有相反關係,對於胃癌及前列腺癌也有相似的結果。美國麻省調查66歲以上的老人在5年內的死亡率,發現胡蘿卜素攝取量多者,癌的危險性少些。
口腔粘膜細胞在煙、酒、X照射及咀嚼檳榔等刺激下,易有微核細胞(micronuclei cell),這種細胞是DNA損傷染色體破碎的標記,可能發展為癌前期的病變,如果給以維生素A及胡蘿卜與檳榔咀嚼者,可以減低這種細胞的百分率,補充的時間愈長,減少的愈多。
在小鼠試驗中,大劑量β-胡蘿卜素可抑制2甲基苯蒽誘導的皮膚致癌作用,有些類胡蘿卜素無此作用。
一般認為,胡蘿卜素在小腸及肝中轉變為維生素A,腎中僅有少量的可轉變。但最近小鼠的試驗給以β-胡蘿卜素後,肺及皮膚中可積累維生素A,所以有可能β-胡蘿卜至少轉變為維生素A後才起作用。有些人認為胡蘿卜素能熄滅單線態氧(Singlet O2)或捕捉自由基,這種單線態氧的反應性強,對機體有副作用,動植物代謝中產生,植物中類胡蘿卜素有熄滅光合作用下產生的這類有害物質。胡蘿卜素的抗癌作用可能由於這些作用。
胡蘿卜素大量攝取後,除在皮膚脂肪積累使基呈黃色外,尚未發現有其他毒性。
參看
| 關於「營養學/維生素A」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |