營養學/維生素B2
| 醫學電子書 >> 《臨床營養學》 >> 維生素 >> 維生素B2 |
| 臨床營養學 |
|
|
5.7.1 結構及性質
維生素B2又名核黃素(Riboflavin,VB2),它是核醇與7,8-二甲基異略嗪的縮合物(圖5-1`6);為黃褐色針狀結晶,溶解度較小,在27.5℃時溶解度為12mg%。核黃素5-磷酸較易溶解,二者在鹼性溶性液及光照下均易分解,其熒光由於三位亞氨基。光分解側鏈可得光色素、光黃素及甲醯甲基黃素。在消化道內,腸內微生物也可將其分解為甲醯甲基黃素等(圖5-170。
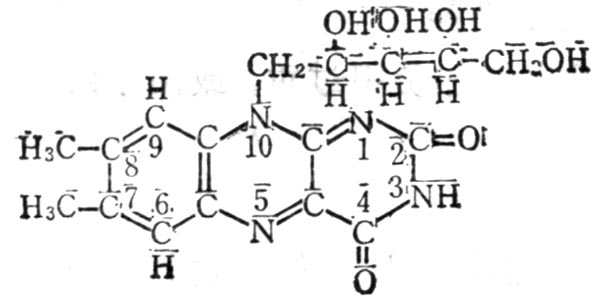
圖5-16 維生素B2結構式
植物能合成核黃素,動物一般不能合成,必須由食物供給,但在哺乳動物腸道中的微生物可以合成並為動物吸收,但其量甚微,不能滿足需要。
核黃素的輔酶有二種形式;即黃素單核苷酸(FMN)和黃素腺嘌呤二核苷酸(FAD)(圖 5-18)。
5.7.2 代謝
核黃素或其輔酶在食物中與蛋白質結合形成複合物——黃素蛋白,從乳、蛋中得來後,經消化道內蛋白酶、焦磷酸酶水解為核黃素。有些黃素蛋白釋放出8α-胺基酸(半胱氨酸或組氨酸)核黃素可以吸收,但無生物效用。
人在小腸近端吸收核黃素。正常人吸收迅速,吸收量與劑量成比例,直到攝取量為25mg時都很穩定。核黃素與其他食品一起攝入,增加其吸收。腸胃道功能紊亂及膽管阻塞都可導致吸收不良。維生素B2在大腸內也可吸收、吸收的機理因劑量大小而異,低劑量時為主動吸收,需要Na+。在劑量為0.2ugmol時,有最大的吸收率,大劑量時為擴散吸收。
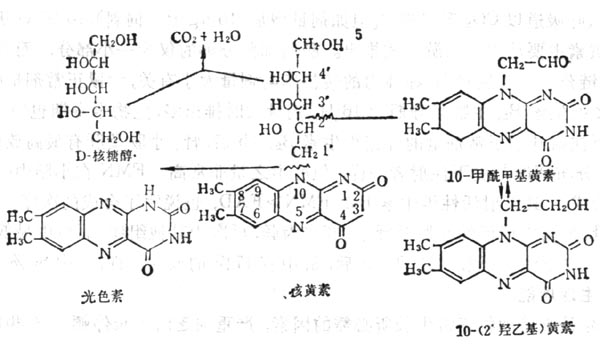
圖5-17 核黃素5-磷酸的分解產物
維生素B2都是以輔酶形式存在於血、組織及體液中,從血流到組織(如肝)細胞中,游離式的核黃素,才能透過細胞膜到細胞內。核黃素類似物如半乳糖黃素及核黃黃素,可能阻止維生B2在黃素激酶(Flavokinase)作用下,轉變為FMN。這種激酶存於許多細胞漿內,但在肝及小腸內的活力特別高。黃素激酶作用時需要ATP及二價陽離子,它也作於維生素B2的類似物,胺基酸的衍生物為干擾劑。維生素B2除掉側鏈後生成物,如光黃素都是干擾劑。
FAD是由FMN通過FAD合成酶作用形成的。此酶廣泛存在於組織的胞漿內,也需要ATP二價陽離子,FMN及其類似物都可作為底物、異核黃素干擾其活力,對FMN及FAD有拮抗作用。維生素B2缺乏及甲狀腺過多時,FAD合成酶活力增加。
水解FMN及FAD的酶廣泛存在各組織中。FMN磷酶在鹼性或酸性中都能作用,在肝中酸性磷酸對FMN的作用較強,在維生素B2缺乏時,並不影響FMN磷酸酶的活力。FAD焦磷酸酶也能促使FAD水解。它在肝病病人的血清中升高。
維生素B2經腎小球濾過,可在腎小管中再吸收。在血清維生素B2濃度低時,尿排出量較少,為一常數。但血清維生素B2達到1μg.ml-1時,排出增多。維生素B2攝取量愈小,體內儲存百分率愈大。給予大鼠55μg14C-一維生素B2,10%的14C從尿中排出,3%在大便中排出,1%從呼吸道以CO2形式排出。但如劑量增加(15μg.ml-1飼料),10%14C從便中排出。所以核黃素主要從尿中以游離式排出。腸道細菌分解的僅為一小部分,而且環狀部比較穩定,僅側鏈分解。維生素B2在體內的轉換率與劑量大小有關,大鼠正常劑量時,每日排出15~20μg維生素B2,生物半壽期為16日,劑量大時排出多,生物半壽期也短。
大鼠皮下注射6倍正常劑量的標記維生素B2,1h後,腎、小腸及肝有最高放射活性。腹腔注射後,其分泌情況與皮下注射者一樣,但肝中之量非常高。FMN在腸中合成,FAD在腎中及肝中合成。其合成放射活性維生素B2>FMN>FAD,說明了合成的次序。如腹腔內注射中等劑量,量高放射活性在肝及腎中,其次為腸,再次為其他組織,而血中最低。在肝中主要為FAD。皮下注射正常劑量,1.5h後,肝中有17%的放射活性。其中80%為FAD。
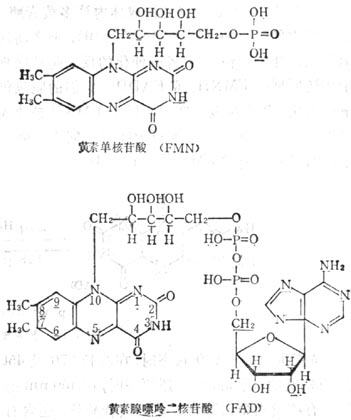
圖5-18 核黃素嘌呤二核苷酸(FAD)
5.7.3 生理功能
維生素B2是維持動物正常生長所必需的因素,嚴重缺乏時生長停頓。有些局部損害,如在口角處因維生素B2的缺乏而發生糜爛。在懷孕時,如維生素B2缺乏,可致畸胎,但在人類尚未發生這種情況。動物試驗證明有些白內障與維生素B2缺乏有關,可用FAD預防。
維生素B2主要功能是構成體內許多黃素酶中的輔酶(FMN,FAD)。這些酶為電子傳遞系統中的氧化酶及脫氫酶(圖5-19),前者將還原型的輔酶與分子氧直接起作用,生成過氧化氫,作用較快。後者所催化的反應是從底物上將一雙氫原子直接遞給FMN或FAD,形成還原型的FMNH2或FADH2,它們的脫氫仍需呼吸鏈上的其他因素,不能直接被分子氧所氧化,作用緩慢。在緩慢。在呼吸鏈上FMNH或FADH氧化能力比NADPH要強一引起,它可以直接與氧作用,而NAPH只能間接與氧作用。FMN或FAD常常是接受NADPH遞給的氫使其變成FMNH或FADH。
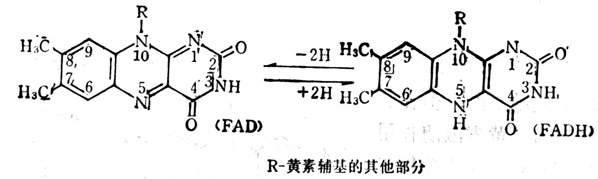
圖5-19 黃素酶的作用
黃素蛋白處於氧化狀態時,在波長370及450nm處,有較寬的吸收峰;處於還原態時,在450nm的峰消失。有些黃素蛋白除含黃核苷酸外,還含有金屬離子(如鐵、鉬、鋅),也是這些酶所需要的。
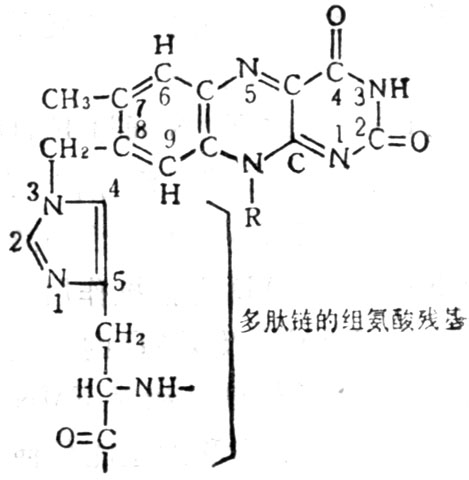
圖5-20 琥珀酸脫氫酶中的組氨酸
FMN或FAD與酶蛋白結合,一般是通過 8位上的亞甲基與酶蛋白上的半胱酸、組氧酸或氨酸相聯結。(圖5-20)。維生素B2輔酶有三種功能形式圖5-21。
(1)以維生素B2為輔酶的氧化酶可分為下列類型:
① 黃素接受電子後又被氧化形成H2O2如葡萄糖氧化酶。
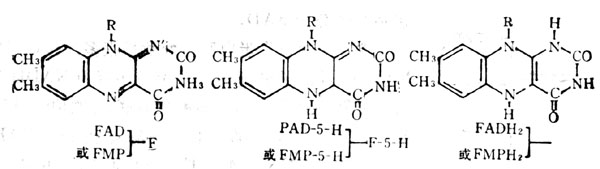
圖5-21 維生素B2輔酶三種功能形式
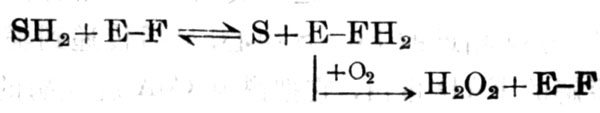
D-葡萄糖+O2→D-葡萄糖內酯+H2O2
② 形成底物-酶複合體並繼續繼續形成中間體,直到與O2作用後,此底物脫氫與複合體分開,如d,1-胺基酸氧化酶。中間體可能為輔酶與底物相偶聯,與O2作用後,亞胺基酸水解為α-酮酸及氨,並生成氧化型的酶及H202。
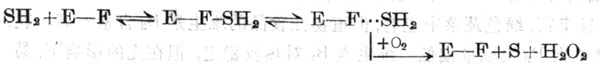
③黃嘌呤氧化酶更為複雜,有二個活動點,一個活動點有1個Mo原子與二個Fe-S中心,Fe-S中心為了維持Mo在氧化狀態,另一活動點為FAD分子。底物首先與氧化Mo(6價)作用,再與FAD作用形成FADH2形成FADH2,最後與氧化作用形成H2O2。
④混合功能氧化酶(黃素單氧化酶),如此類酶催化氧分子中的一個氧原子到底物中去另一個原子形成水。如底物本身供給電子以水者叫做內部黃素氧化酶,其反應式如下:其中-XH可為-OH或-NH2。
![]()
如果由NADPH(或NADH)作為還原劑以形成水者,叫做外部黃素氧化酶,一些芳香族化合物的羧基化(如肝犬尿氨酸羧化酶)需要此酶,反應式如下:
AH+NAD(P)H+H++O2→A-OH+H2O+NAD(P)+(AH為底物)
實際上這些羧基化酶的輔酶(核黃素部分)先氧化為氧化型者,則與NAD(P)H作用又還原為還原型者。
⑤微粒體混合功能氨氧化酶,此酶在肝微粒體中,其底物為半胱胺,氧化為胱胺,除黃素蛋白外,還需要NADPH及氧的參加,此反應產生-S-S-以合成蛋白的雙硫鍵。
(2)維生素B2脫氫酶。無金屬黃素蛋白的脫氫酶,包括有二氫硫辛醯胺脫氫酶(dihydro lipoamide dehydrogenase)、麥胱甘肽還原酶(glutathione reduetase)、硫氧還蛋白還原酶(thioredoxin reductase)、NADH-細胞色素b3還原酶(NADH-cyutochrome b2reductase)及NAD(P)H-細胞色素P450還原酶(NAD(P)H-cytoehrome P-450reductase)前三者為NAD(P)雙硫氧化原酶系統(圖5-22)。
NADH-細胞色b3還原酶催化NADH的H轉移至FAD而形成FADH2再將電子轉移到氧化型細胞色素b3上將其還原,NADPH-細胞色素P450還原酶電子供體為NADPH,但還有一分子FAD及一個分子FMN,微粒體中NADPH-細胞色素C還原酶包括2個分子FAD。
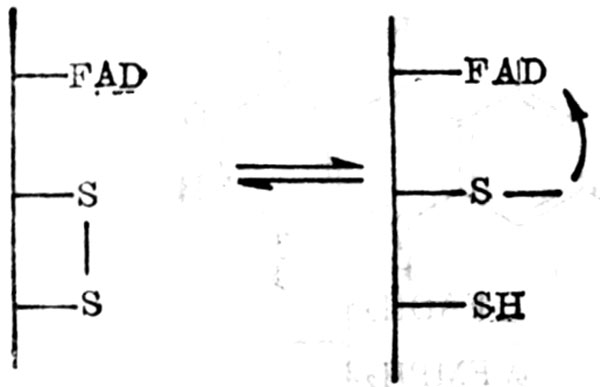
圖5-22 FAD-雙硫氧化還原酶系統
含金屬的黃素蛋白脫氫酶數量很多,包括呼吸鏈中含有NAD(P)H的脫氫酶,其中研究較多者為NADH脫氫酶及琥珀酸脫氫酶,因其與氧化磷酸化有聯繫。琥珀酸脫氫酶與FAD及2個Fe-S中心偶聯,再與輔酶Q相聯。NADH-輔酶Q脫氫酶每個FMN有4個Fe-S中心,每個中心有2~4個鐵原子,NADH還原黃素蛋白,然後將電子傳遞到離NAD相近Fe-S中心,再傳遞到與輔酶Q相近的Fe-S中心,最後傳遞到輔酶Q上。
另外在粒線體中有溶解的FAD蛋白,它把醯基CoA脫氫酶的氧化作用與輔酶Q的還原聯繫起來。這種FAD蛋白叫做電子傳遞蛋白(electron-transferring flavoprotein,ETF)。
5.7.4 來源
腸中細菌可以合成維生素B2,但為量不多,主要尚須依賴食物中供給。牛奶、雞蛋含維生素B2比較豐富,綠色蔬菜中也有,但植物性食品的維生素B2含量不高。我國以植物性食品為主,維生素B2攝取量偏低。維生素B2熱較穩定,但在光的影響下,易於破壞。牛奶中的維生素B2暴露在光中,在不正常味道發生前,光分解就已發生。放置在光中4h,維生素B2損失約71%,烹調損失較小,但如將烹調水廢棄,溶於水的維生素B2遭到損失。將維生素B2混入食物中,在儲藏過程也比較穩定。在室溫中,充氨密封條件下,儲存1~2年,還能保存50%以上。
5.7.5 需要量
(1)營養評價指標 一般仍以尿中維生素B2排出量、紅細胞維生素B2含量及紅細胞麥胱甘胱還原酶活力等為維生素B2的營養指標,其中較為靈敏者為紅細胞麥胱甘肽還原酶。大鼠肝及器官中都有磷吡哆胺氧化酶(pyridoxamine 5'-phosphate oxidase),如大鼠缺乏維生素B2,此酶活力有改變,缺乏4周時達到嚴重缺乏程度,此酶活力也降至最低值,這個指標仍在動物試驗階段。
(2)需要量 從我國維生素B2需要量的試驗結果來看,每日取量0.70~1.16mg者,試驗期共計10周,舌面乳頭漸趨扁平、光滑甚或萎縮,但無其他缺乏症象。攝取量12.53mg組,尿排出量上升,根據其轉折點計算相當1.2mg攝取量,所以以此為最低需要量,1.5mg為適宜要量。這與Horwitt綜合其他作者之結果是一致的。他認為每日取量的0.8~0.9mg2年久,並無缺乏症象的出現,從尿排出量來看,攝取量1.2mg,維生素B2在組織中可能有少量儲存。攝取量0.55~1.10mg.d-1尿中維生素B2排出量為攝取量的10%,每日取量1.3mg或更高時,排出量大於20%。
維生素B2的需要量與熱量及勞動強度沒有關係,但與蛋白質需要量有關係,生長迅速,創傷恢復,懷孕與哺乳期蛋白質需要增加,維生素B2需要量也增加。供應量嬰兒每日~0.6mg,兒童0.6~1.2mg,成人1.3~1.7mg,孕婦及乳母1.8~2.0mg。治療劑量為一次mg或一次mg.d-1,每日3次,由於維生素B2不易溶解,如期望治療效果快一些,可用肌肉注射25mg維生素B2。為了預防我國維生素B2缺乏,以維生素B2月桂酸酯150mg(相當於75mg維生素B2)油針劑肌肉注射,由於釋放緩慢,注射一次可維持成人維生素B2正常達2~3月久。
參看
| 關於「營養學/維生素B2」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |