營養學/維生素D
| 醫學電子書 >> 《臨床營養學》 >> 維生素 >> 維生素D |
| 臨床營養學 |
|
|
5.3.1 結構與性質
維生素D(VD)是環戊烷多氫菲類化合物,可由維生素D原(ProvitaminD)經紫外線270~300nm激活形成。動物皮下7-脫氫膽固醇,酵母細胞中的麥角固醇都是維生素D原,經紫外線激活分別轉化為維生素D3及維生素D2量少,但人工照射者多為此型(圖5-6)。維生素D的最大吸收峰為265nm,比較穩定,溶解於有機溶媒中,光與酸促進異構作用,應儲存在氮氣、無光與無酸的冷環境中,油溶液加抗氧化劑後穩定,水溶液由於有溶解的氧不穩定。雙鍵系統還原也可損失其生物效用。
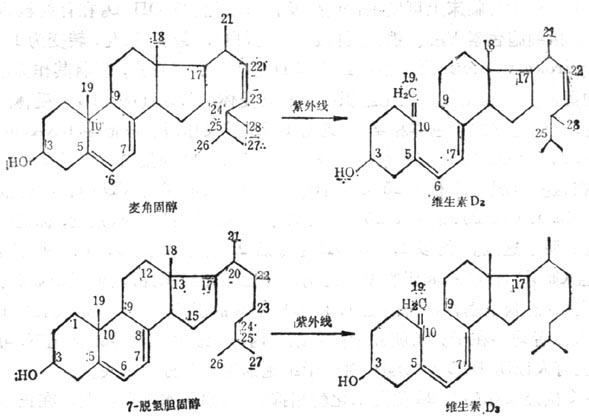
圖5-6 麥解固醇及7-脫氫基膽固醇在紫外線作用下轉變為維生素D2及維生素D3
5.3.2 代謝
從食物中得來的維生素D,與脂肪一起吸收,吸收部位主要在空腸與迴腸。膽汁幫助其吸收。脂肪吸收受干擾時,如慢性胰腺炎、脂肪痢及膽道阻塞都會影響他的吸收。吸收的維生素D與乳糜微粒相結合,由淋巴系統運輸,但也可與維生素D運輸蛋白(α-球蛋白部分)相結合在血漿中運輸。有些與β-脂蛋白相結合,口服維生素D與乳糜微粒結合,比從皮膚中來的與蛋白結合者易於分解。
當維生素D運到肝臟中,在微粒體中經單氧酶系統作用,將其25位羥基化形成25(OH)D(25-hydroxy vitamin D3)(圖5-7),肝外的其他組織也可吸取維生素D及25-(OH)D3,因此組織中維生素D及25(OH)D3及其總量比血漿中多,如果靶組織需要,可將其釋放出來,他們在脂肪組織中最多,釋放速度最慢,當體重減輕,脂肪減少時,他們也可釋放出來。靜脈注射維生素D,較快的由血漿進入到組織中。血漿中25(OH)D3在注射後1~3天達到高峰,其濃度可達到20~40ng.ml-1,最高可達80ng.ml-1。濃度與攝入量有一定的關係,小於4 ng.ml-1,臨床上可發生佝僂病及骨質軟化。25(OH)D3在腎粒線體單氧酶作用下(酶系統包括細胞色素P450、鐵硫蛋白及黃素蛋白),經羧基化,轉變為1,25(OH)2D3(1,25-dihydroxy vxtamin D),他是維生素D的生物作用形式,現將其作為激素。其作用方式與其他固醇類激素相似。在靶組織中都有其受體,1,25(OH)2D3與受體形成複合物內,與細胞核或染色體相結合,通過DNA轉錄作用合成信使RNA(mRNA),並轉譯為蛋白質,1,25(OH)2D3在血漿中由分子量為52,00的蛋白質輸送至靶組織(如小腸、骨、腎等),在這些組織中既有1,25(OH)2D3的受體,又有需要VD的鈣結合蛋白(Calcium binding Protein,CaBP),說明1,25(OH)2D3的影響。最近,報導胰臟內有1,25(OH)2D3及CaBP,二者均存在於分泌胰島素的β細胞內,在維生素D空竭情況下,可以阻止胰島素的分泌,也有人證明1,25(OH)2D3對於幹細胞的生長與分化有關。
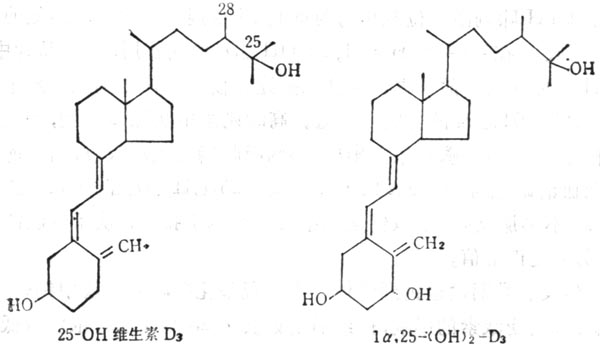
圖5-7 25-(OH)D3及1a;25(OH)2D3的結構式
在腎中1位羧基化酶與24位羧基化酶相抑制,為血鈣水平所控制。在正常血鈣濃度下(9.5mg%)腎中1α羧基化酶與24位羧基化酶都有活力,所以既能合成1,25(OH)2D3也能合成24,25(OH)2D3,血清鈣低時,刺激1位羧基化酶,鈣多時抑制此酶。由此以調節1,25(OH)2D3合成之量。1,25(OH)2D3合成量多,24,25(OH)2D3合成量少,除血鈣外,尚有其他因素影響1,25(OH)2D3如甲狀旁腺素(Parthormone,PTH)、降鈣素(Calcitonin,CT)、催乳激素都可使其增多。腎為2個羧基化的主要組織,但在體外試驗已證明骨、胎盤、腸及蛋黃均有此功能。
1,25(OH)2D3的分解代謝與24,25(OH)2D3的途徑相類似。24位羧基化後可進一步氧化成24位氧絡物,然後23位羧基化,側鏈分裂。26-C,27-C可氧化CO2水溶性代謝物有維生素D3-23羧酸(Calcitroic acid),也可產生內酯及酸酯,維生素D的分解代謝主要場所在肝內,並將其代謝物排入到膽汁中,口服維生素D比從皮膚中得來的易於分解。25(OH)2D3及1,25(OH)2D3也可以葡糖苷酸形式通過膽肝形成肝腸循環或從大便中排出。口服生理劑量48h後,30%的劑量從大便中排出,僅2-~4%從尿中排出。
5.3.3 生理功用
(1)維持血清鈣磷濃度的穩定 血鈣濃度低時,誘導甲狀旁腺素分泌,將其釋放至腎及骨細胞。在腎中PTH除刺激1位羧化酶與抑制24位羧基化酶外,還促使磷從尿中排出,鈣在腎小管中再吸收。在骨中PTH與1,25(OH)2D3協同作用,將鈣從骨中動員出來。在小腸中1,25(OH)2D3促進鈣的吸收。從這三條途徑使血鈣恢復到正常水平,又反饋控制PTH的分泌及1,25(OH)2D3的合成。在血鈣高時刺激甲狀腺C細胞,產生降鈣素,阻止鈣從骨中動員出來,並促使鈣及磷從尿中排出。小腸吸收磷為主動吸收,需要能量,鈉、葡萄糖、1,25(OH)2D3及血清磷低時(8mg%以下),刺激1,25(OH)2D3的合成,促進小腸對鈣、磷的吸收。由於PTH不參加反應,所以鈣從尿中排出而磷不排出,從而使血鈣略有上升,而磷上升較多,使血磷恢復正常值。
(2)促進懷孕及哺乳期輸送鈣到子體 1位羧基化酶除受血清中鈣磷濃度及膳食中鈣磷供給量的影響外,還受激 素的影響,停經後的婦女1,25(OH)2D3濃度減低,易有骨質軟化等症状。
在懷孕期間1,25(OH)2D3血漿濃度上升,哺乳期繼續上升,斷乳後母體逐漸恢復到正常水平。24,25(OH)2D3之水平與之相反,懷孕期下降,斷乳後恢復到正常。胎盤也有1位羧基化酶,在懷孕期間無腎動物也能合成1,25(OH)2D3。乳腺也是1,25(OH)2D3的靶組織,對乳中鈣的水平直接關係,懷孕及哺乳期間母親可從自身的骨中將鈣輸出以維持胎兒嬰兒正常生長,維生素D供應充足者,在斷乳後,又可重新獲得鈣,維生素D缺乏者,這種恢復能力較差。
(3)1,25(OH)2D3作用機理 1,25(OH)2D3對小腸作用為誘導合成CaBP.1,25(OH)2D3與小腸細胞的受體形成複合體進入細胞核染色體上,促使CaBP的信使RNA(mRNA)的合成,此mRNA在胞漿內轉錄為CaBP。這種蛋白促使鈣離子通過微絨毛刷狀緣(microvillus brush border),積累於腸細胞的粒線體或其他部位。通過Na+將Ca2+擠出基底-外側膜外(basal-lataaral mebrace)。1,25(OH)2D3對腎小管Ca2+的再吸收作用與在小腸中是一樣的。1,25(OH)2D3也可以在低血漿鈣及膳食中鈣缺乏時,將鈣從骨中動員出來,但在骨中未發現有CaBP,1,24,25(OH)2D3可以促進小腸吸收鈣,但不能從骨中將鈣動員出來,所以1,25(OH)2D3對骨的作用機理與對小腸者是不同的,但目前還不清楚。
骨的礦物化作用的機理尚未闡明,補充1,25(OH)2D3給缺乏維生素D的動物及人體,都不能有助於骨中礦物質的沉積。動物體內雖然分離出許多維生素D代謝產物但迄今尚未找出對骨的礦物化有明顯作用者。在現階段中只了解到維生素D促進鈣磷的吸收,又可將鈣磷從骨中動員出來,使血漿鈣、磷達到正常值,促使骨的礦物化,並不斷更新。
5.4.3 需要量
(1)維生素D的營養指標血清中鹼性磷酸酶增加比維生素D缺乏的臨床症状出現要早一些,他的增加幅度也與維生素D缺乏的程序有關,但是他是非特異性的(表5-7)。血清中Ca與P的乘積(mg%),正常值為36~40。佝僂病及骨質軟化患者的乘積在30以下。
表5-7 正常人及病人血清鹼性磷酸酶、鈣、磷濃度
| 血清鹼性磷酸酶(布氏單位.ml-1 (國際單位umol.mm-1.L-1) | 血清Ca(mg%) | 血清P(mg%) | ||
| 正常嬰兒 | 5~15 | 26~80 | 10 | 5 ~ 8 |
| 正常成人 | 3~5 | 16~26 | 10 | 3~4.5 |
| 佝僂病人 | >20 | >115 | 8~9 | 3 |
| 骨質軟化病人 | 15 | 80 | 9 | 2~3 |
| 甲狀旁腺素過多 | 4~20 | 20~120 | 12~16 | 2~8 |
| 骨質疏鬆 | 2 | 10 | 10~12 | 4~5 |
| 變形性骨炎(Paget's) | 50 | 268 | 10 | 4 |
| 成骨細胞瘤 | 30 | 160 | 10 | 4 |
靜脈注射1mg維生素D後,測定其血清磷值,隔5天後再測定飢餓時血清磷值,若其值增加,則可為維生素D缺乏的指標。口服磷酸鈉鹽24h後,血漿Ca值減低。腕部骨骺部增大也是一個簡單診斷佝僂病的方法。
現在用同位素蛋白結合方法測定25-(OH)D3,或1,25(OH)D3,正常人血中25-(OH)D3濃度為15.2±5.6ng.ml-1,若小於4ng.ml-1,臨床上易有佝僂病及骨質軟化。1,25(OH)D3血漿正常。水平為3~6ng.ml-1,但由於這方面工作不多,其正常低限與最理想水平尚未確定。
(2)維生素D需要量由於日光照射皮膚可產生維生素D,從外界應予補充量受日光照射的影響,宇身航員未得到日光照射1~3個月久,每天給以維生素D或25(OH)D310ug可以維持血漿25(OH)D3的正常水平。從出生到青春期供應量為10ug(400IU)孕婦乳母10ug。在整個生命過程中,鈣磷進行動態平衡,骨骼不斷進行重建,成人也需要一定量的維生素D約為5ug。
5.3.5 來源
魚肝油、牛奶、蛋黃等動物性食品中有維生素D3,蕈及麥角中維生素D2,皮膚中7-脫氫膽固醇經紫外線照射變為維生素D3前體(Previtamin D3),然後在一定溫度下異構為維生素D3,這一過程比較緩慢,37℃時維生素D3可達80%,溫度低時轉換率小些。皮膚中維生素D3與前體仍繼續異構為維生素D3為機體所利用。因其轉變過程緩慢,不致產生毒性,血漿25(OH)維生素D3不超過80%,溫度低時轉換率小些。皮膚中維生素D3與前體呈一定的平衡。血漿中有維生素D3結合蛋白,可將維生素D3從皮膚中帶到血流中,這種蛋白不與前體結合。為了獲得新的平衡,前體不斷地變成維生素D3。停止照射後,皮膚中儲存的前體仍繼續異構為維生素D3為機體所利用。因其轉變過程緩慢,不致產生毒性,血漿25(OH)維生素D3不超過80ng.ml-1,攝取大劑量者可上升到400 ng.ml-1,易產生毒性。
5.3.6 臨床應用及大劑量的毒性
維生素D除防治維生素D3缺乏病外1,25(OH)2D3可防治下列病症:①腎性骨病,腎功能不全缺少1位羥基化酶,體內不能合成1,25(OH)2D3必須從體外攝取;②難治療抗維生素D3佝僂病,由於遺傳因素,磷從腎排出過多;③甲狀旁腺素缺少症,患者不能在低血漿Ca時產生1,25(OH)2D3;④抗維生素D的佝僂病,維生素D供應正常但仍有佝僂病,由於代謝上的缺陷,不能1位羧基化;⑤癲癇病人使用苯巴比妥可能導致骨病。也可用25(OH)2D3的生理劑量為1μg/天。此劑量也可作為治療劑量。
維生素D中毒劑量與生理劑量相差不多,嬰兒服用50μg(200IU)或更少一些可以導致血鈣過多,腎功能不全。成人中毒劑量個體差異較大,有人口服2000IU中毒現象,口服5000IU者易中毒,口服量不能超過800IU。用維生素D治療時,要檢查血鈣水平,如血鈣正常不致中毒,輕度中毒有嘔吐,食欲不振等現象,重者可致死亡。維生素D毒性可由於血流中25(OH)2D3水平高代替1,25(OH)2D3與蛋白受體結合,因此1,25(OH)2D3不能進入細胞,也不能起控制鈣的吸收及動員骨鈣的作用,因此血鈣水平高,而使腎、心臟及主動脈鈣化,治療維生素D過多時可用低鈣膳及動員骨鈣的作用,因此血鈣水平高,而使腎、心臟及主動脈鈣化,治療維生素D過多時可用低鈣膳及糖皮質激素以減低血清鈣的水平。
中毒時尿中排出Ca量過多比血鈣過高發生較早,尿鈣過高易形成腎結石。
維生素D及25(OH)D3可以儲存,維生素D儲存時間一般為1~4個月,有的可達18個月久。維生素D代謝物也可產生中毒現象,但由於其生物半衰期短,中毒時間也較短,25(OH)D3可達數周,1,25(OH)2OH3僅有數日。
參看
| 關於「營養學/維生素D」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |