病理學/變性和物質沉積
| 醫學電子書 >> 《病理學》 >> 細胞和組織的損傷 >> 損傷 >> 變性和物質沉積 |
| 病理學 |
|
|
所謂變性(degeneration)乃指細胞或細胞間質的一系列形態改變並伴有結構和功能的變化(功能下降),表現為細胞間質內出現異常物質或正常物質而數量顯著增多。但使用這一定義時必須慎重,因為有時細胞內某種物質的增多恰屬生理現象而並非病理性改變。
一般而言,變性是可復性改變,當原因消除後,變性細胞的結構和功能仍可恢復。但嚴重的變性則往往不能恢復而發展為壞死。
變性可概括分為二大類;細胞含水量異常;細胞內物質的異常沉積。
(一)細胞水腫
人 體約一半由水構成,其中約2/3存在於細胞內,約1/3存在於細胞外。在正常情況下細胞內外的水分互相交流,協調一致,保持著機體內環境的穩定。但當因缺 氧、缺血、電離輻射以及冷、熱、微生物毒素等的影響,而致細胞的能量供應不足、細胞膜上的鈉泵受損,使細胞膜對電解質的主動運輸功能發生障礙,或細胞膜直 接受損時,則導致細胞內水分增多,形成細胞水腫,嚴重時稱為細胞的水變性(hydropic degeneration)。
形態學:水腫的 細胞體積增大,胞漿基質內水分含量增多,變得較為透明、淡染,胞核也常常被波及而增大、染色變淡、從而使整個細胞膨大如氣球,故有氣球變之稱(圖 1-17)。電鏡下,除可見胞漿基質疏鬆變淡外,尚可見粒線體腫脹及嵴變短、變少甚至消失;內質網則廣泛解體、離斷和發生空泡變。嚴重的水變性有時與漸進 性壞死和壞死難以區分。
在電鏡技術問世之前,有混濁腫脹之稱,用以形容細胞腫脹和胞漿出現顆粒而變混濁,相應的器官(如心、肝、腎等實質性 器官)在肉眼觀上腫脹、邊緣變鈍、透明度降低(混濁)。電鏡檢查表明,胞漿內的顆粒實乃水腫時腫大的粒線體和擴張斷裂的內質網,但有時也可為小泡狀的蛋白 質或其他物質的沉積。故為避免誤解,現已放棄混濁腫脹這一名稱。
結果:細胞水腫通常為細胞的輕度或中等度損傷的表現,當原因消除後仍可恢復正常。但如進一步繼續發展,則可能形成脂肪變性甚或壞死。
(二)細胞內物質沉積
在病理狀態下,不同的原因可以導致多種不同的物質在細胞和間質內異常沉積,為變性的主要表現。
1.脂肪沉積 正常情況下,除脂肪細胞外,其他細胞內一般不見或僅見少量脂滴。如這些細胞中出現脂滴或脂滴明顯增多,則稱為脂肪變性(fatty degeneration)。電鏡下可見脂滴形成於內質?
■[此處缺少一些內容]■
碳 水化合物等結合,形成細胞的結構成分,即成為結構脂肪。因此,上述過程中的任何一個環節發生障礙便能導致肝細胞的脂肪變性;①脂蛋白合成障礙,以致不能將 脂肪運輸出去,造成脂肪在肝細胞內堆積。這常系由於合成脂蛋白的原料如磷脂或組成磷脂的膽鹼等物質缺乏,或由於化學毒物(如酒精、四氯化碳)或其他毒素 (如黴菌毒素)破壞內質網結構或抑制某些酶的活性,使脂蛋白及組成脂蛋白的磷脂、蛋白質等的合成發生障礙所致。②中性脂肪合成過多。這往往是由於飢餓或某 些疾病(如消化道疾病)造成飢餓狀態,或糖尿病患者對糖的利用障礙時,從脂庫動員出大量脂肪,其中大部分以脂肪酸的形式進入肝,致肝合成脂肪增多,超過了 肝將其氧化利用和合成脂蛋白輸送出去的能力,於是導致脂肪在肝內的蓄積。③脂肪酸的氧化障礙,使細胞對脂肪的利用下降。例如白喉外毒素等能干擾脂肪酸的氧 化過程,而缺氧即影響脂蛋白的合成,又影響脂肪酸的氧化。總之,肝細胞的脂肪變性乃上述某一因素或幾種因素綜合利用的結果。
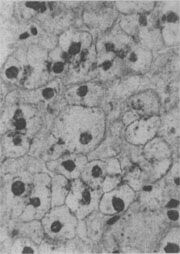
圖1-17 肝細胞氣球樣變
病毒性肝炎時,肝細胞明顯腫脹,胞漿疏鬆呈氣球樣
形 態學:輕度肝脂肪變性時,肝肉眼觀可無明顯改變,或僅輕微黃染。如脂仿變性比較顯著和廣泛,則肝增大,色變黃,觸之質如泥塊並有油膩感。鏡下,肝細胞內的 脂肪空泡較小,起初多見於核的周圍,以後變大,較密集散佈於整個胞漿中,嚴重時可融合為一個大空泡,將細胞核擠向胞膜下,狀似脂肪細胞(圖1-18)。脂 肪變性在肝小葉中的分布與其病因有一定的關係,例如肝淤血時,小葉中央區缺氧較重,故脂肪變性首先在此處發生。但長期淤血後,小葉中央區的肝細胞大多萎 縮、變性或消失,於是小葉周邊區肝細胞也因缺氧而發生脂肪變性。磷中毒時,肝細胞脂肪變性則主要發生於小葉周邊區,這可能是由於此區肝細胞對磷中毒更為敏 感的緣故。
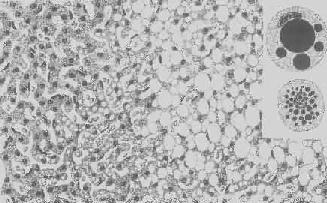
圖1-18 肝細胞脂肪變性
肝細胞胞漿內出現大小不等的脂肪空泡;右上角為餓酸染色的脂肪細胞, 脂滴染成黑色
(2) 心肌脂肪變性:心肌在正常情況下可含有少數脂滴,脂肪變性時脂滴明顯增多。鏡下,脂肪空泡較細小,呈串珠狀成排排列,主要位於肌纖維Z帶附近和粒線體分布 區。常為貧血和中毒的結果。在嚴重貧血時,可見心膜下尤其是乳頭肌處出現成排的黃色條紋,與正常心肌的暗紅色相間排列,狀若虎皮斑紋,故有「虎斑心」之 稱。嚴重感染、白喉外毒素以及其他毒物(如磷、砷、氯仿等)也能引起心肌的瀰漫性脂肪變。肉眼觀,心肌均勻變濁,略呈黃白色。但通常心功能並不受明顯影 響。顯著的心肌脂肪變性如今並不常見。
(3)腎脂肪變性;在嚴重貧血、缺氧和中毒過程中,或腎小球毛細血管通透性升高時,腎小管特別是近曲小管的上皮細胞可吸收漏出的脂蛋白而導致脂肪變性。脂滴起初多位於細胞基底部。肉眼觀,腎稍腫大,切面上可見皮質增厚,略呈淺黃色。
2.玻璃樣變性 又稱透明變性(hyaline degeneration),為十分常見的變性,主要見於結締組織、血管壁,有時也可見於細胞內。
1. 結締組織玻璃樣變:常見於纖維瘢痕組織、纖維化的腎小球,以及動脈粥樣硬化的纖維性瘢塊等。此時纖維細胞明顯變少,膠原纖維增粗並互相融合成為梁狀、帶狀 或片狀的半透明均質,失去纖維性結構(圖1-19)。質地堅韌,缺乏彈性。玻璃樣變的發生機制尚不甚清楚,有人認為在纖維瘢痕老化過程中,原膠原蛋白分子 的交聯增多,膠原原纖維也互相融合,其間並有較多的糖蛋白積聚,形成所謂玻璃樣物質;也有人認為可能由於缺氧、炎症等原因,造成局部pH升高或溫度升高, 致使原膠原蛋白分子變性成明膠並互相融合所致。
2.血管壁玻璃樣變:這種改變常見於高血壓病時的腎、腦、脾及視網膜的細動脈。此時,可能是 由於細動脈的持續性痙攣,使內膜通透性增高,血漿蛋白得以滲入內膜,在內皮細胞下凝固成無結構的均勻紅染物質。此外,內膜下的基底膜樣物質增多。這些改變 使細動脈的管壁增厚、變硬,管腔變狹,甚至閉塞(圖1-20),此即細動脈硬化症(arteri-olosclerosis),可引起腎及腦的缺血。
3. 細胞內玻璃樣變:亦稱為細胞內玻璃樣小滴變性。這種情況常見於腎小球腎炎或其他疾病而伴有明顯蛋白尿時。此時腎近曲小管上皮細胞胞漿內可出現許多大小不等 的圓形紅染小滴(圖1-21),這是血漿蛋白經腎小球濾出而又被腎小管上皮細胞吞飲的結果,並在胞漿內融合成玻璃樣小滴,以後可被溶酶體所消化。此外,在 酒精中毒時,肝細胞核周胞漿內亦可出現不甚規則的紅染玻璃樣物質。電鏡下,這種物質由密集的細絲構成,據認為可能是細胞骨架中含角蛋白成分改變的結果,並 被稱為Mallory小體。
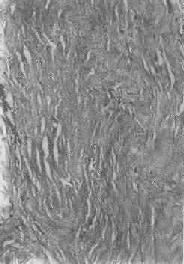
圖1-19 纖維瘢痕組織的玻璃樣變
膠原纖維變粗,互相融合呈均質梁狀
3.纖維素樣變性(纖 維蛋白樣變性)為間質膠原纖維及小血管壁的一種變性。病變部位的組織結構逐漸消失,變為一堆境界不甚清晰的顆粒狀、小條或小塊狀無結構物質,呈強嗜酸性紅 染,狀似纖維素,並且有時呈纖維素染色,故稱此改變為纖維素樣變性(fibrinoid degeneration),其實為組織壞死的一種表現,因而也稱為纖維素樣壞死(fibrinoid necrosis)。
纖維素樣變性 主要見於急性風濕病及結節性動脈周圍炎等變態反應性疾病。至於所謂纖維素樣物質的性質和形成機制,至今尚無統一意見。一般認為,在早期,結締組織基質中有 PAS陽性的粘多糖增多,以後纖維崩解為碎片,從而失去原來的組織結構而變為纖維素樣物質。此外,還有免疫球蛋白增多,有時還有纖維蛋白增多。這種改變可 能是抗原抗體反應時形成的生物活性物質使間質受損、膠原纖維崩解所致。同時,附近小血管也可受損,引起通透性升高、血漿滲出,並在組織凝血系統的酶的催化 作用下,使血漿纖維蛋白原轉化為纖維蛋白。
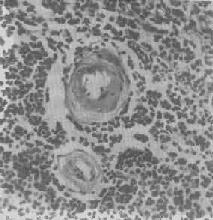
圖1-20 脾中央動脈玻璃樣變
中央動脈管壁明顯增厚,呈玻璃樣均質狀,管腔變窄
4.粘液性變性 組織間質內出現類粘液的積聚稱為粘液樣變性(mucoid degeneration)。鏡下可見病變處的間質變疏鬆,充以染成淡藍色的膠狀液體,其中有一些多角形、星芒狀細胞散在,並以突起互相聯綴。
結 締組織粘液樣變性常見於間葉性腫瘤、急性風濕病時的心血管壁、動脈粥樣硬化的血管壁。甲狀腺功能低下時,全身皮膚的真皮及皮下組織的基質中有較多類粘液 (mucoid)及水分瀦留,形成粘液水腫(myxedema),其機制可能是甲狀腺功能低下時,能促進透明質酸酶活性的甲狀腺素分泌減少,致透明質酸 (類粘液的主要成分之一)降解減弱而大量瀦積於組織內。
粘液樣變性當病因消除後可以逐漸消退,但如長期存在,則可引起纖維組織增生,從而導致組織硬化。
5.澱粉樣變性 組織內有澱粉樣物質沉積稱為澱粉樣變性(amyloid degeneration,amyloidosis)。澱粉樣物質為一種結合粘多糖的蛋白質,遇碘時被染成赤褐色,再加以硫酸則呈藍色,與澱粉遇碘時的反 應相似,故稱之為澱粉樣物質。此物質常浸潤於細胞間或沉積於小血管的基底膜下,或沿網狀纖維支架分布(圖1-22)。澱粉樣物質在HE染色切片中為淡紅色 均質狀,電鏡下則為纖細的絲狀。
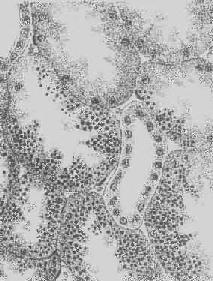
圖1-21 腎近曲小管上皮細胞玻璃樣小滴變
上皮細胞胞漿內出現大小不等的均質圓形小滴

圖1-22 肝澱粉樣變
淀 粉樣變可為全身性和局部性二種。前者在我國極為罕見,多發生在長期慢性化膿、骨髓瘤及結核病等情況下。局部性澱粉樣變則較常見,並好發於瞼結膜及上呼吸道 等處的慢性炎症而伴有大量漿細胞浸潤時,發生機制不清。根據澱粉樣物質中常有丙種球蛋白和血清中球蛋白增多的現象,有人認為這是由於抗原抗體反應在血中形 成的蛋白複合物,也有人認為是漿細胞產生的免疫球蛋白與纖維母細胞、內皮細胞所產生的含硫粘多糖相結合而形成的複合物。
6.病理性色素沉積 組織中可有各種色素沉積,其中有的來源於機體自身,稱為內源性色素,如含鐵血黃素、膽色素、脂褐素、黑色素等;有的則來自體外,為外源性色素,如炭末及紋身所用的色素。常見的病理性色素沉積有以下幾種:
(1) 含鐵血黃素:含鐵血黃素(hemosiderin)是由鐵蛋白(ferritin)微粒集結而成的色素顆粒,呈金黃色或棕黃色而具有折光性。顆粒大小不 一,是巨噬細胞吞食紅細胞後在胞漿內形成的一種色素,為血紅蛋白被巨噬細胞溶酶體分解而轉化所成。由於鐵蛋白分子中含有高鐵(Fe3+),故遇鐵氰化鉀及 鹽酸後出現藍色反應,稱為普魯士藍或柏林藍色反應。細胞破裂後,此色素亦可散佈於組織間質中。左心衰竭時,在發生淤血的肺內可有紅細胞漏出肺泡中,被巨噬 細胞吞噬後形成含鐵血黃素。這種細胞可出現於患者痰內,即所謂心衰細胞。當溶血性貧血時有大量紅細胞被破壞,可出現全身性含鐵血黃素沉積,主要見於肝、 脾、淋巴結、骨髓等器官。
(2)膽紅素(bilirubin):也是在吞噬細胞內形成的一種血紅蛋白衍生物。在生理情況下,衰老的紅細胞在 單核吞噬細胞中被破壞,其血紅蛋白被分解為珠蛋白、鐵及膽綠素,後者還原後即成為膽紅素,進入血液。血中膽紅素過多時則將組織染成黃色,稱為黃疸。膽紅素 一般呈溶解狀態,但也可為黃褐色折光性小顆粒或團塊。在膽道阻塞及某些肝疾患時,肝細胞、毛細膽管及小膽管內可見許多膽紅素。黃疸明顯時,膽紅素顆粒亦可 見於Kupffer細胞、腎小管上皮細胞內,並可在腎小管腔內形成膽汁管型。但人體因有血腦屏障的保護,膽紅素通常不能進入腦和脊髓,而在新生兒則由於血 腦屏障尚不完善,故在高膽紅素血症(hyperbilirubinemia)時,大量膽紅素可進入腦細胞內,使其氧化磷酸化過程受障,能量產生受抑,細胞 乃發生變性,引起神經症狀。肉眼觀可見多處神經核(豆狀核、下丘腦、海馬回等)明顯黃染,故稱之為核黃疸。
(3)脂褐素 (lipofuscin):為一種黃褐色細顆粒狀色素,其成分約50%為脂質,其餘為蛋白質及其他物質。脂褐素顆粒為細胞內自噬溶酶體 (autophagolysosome)中的細胞器碎片發生某種理化改變後,不能被溶酶體酶所消化而形成的一種不溶性殘存小體。正常人的附睾上皮細胞、睾 丸間質細胞以及某些神經細胞的胞漿中可含有少量脂褐素。老年人及一些慢性消耗性疾病患者的肝細胞、腎上腺皮質網狀帶細胞的胞漿以及心肌細胞核兩側的胞漿 中,均可出現脂褐素,故此色素又有消耗性色素之稱。脂褐素顆粒在電鏡下呈典型的殘存小體(residual bodies)結構。
(4)黑 色素(melanin):為大不、形狀不一的棕褐色或深褐色顆粒色素。正常人皮膚、毛髮、虹膜及脈胳膜等處均有黑色素存在。皮膚黑色素由黑色素細胞 (melanocyte)產生:黑色素細胞中的酪氨酸在酪氨酶的作用下,氧化為二羥苯丙氨酸(dihydroxyphenylalanine,DOPA, 多巴)。多巴被進一步氧化為吲哚醌,失去CO2後轉變為二羥吲哚,後者聚後成一種不溶性的聚合物,即黑色素,再與蛋白質結合為黑色素蛋白。黑色素細胞內因 含有酪氨酸酶,故當加上多巴時,則出現與黑色素相似的物質,謂之多巴反應陽性;相反,表皮下的噬黑色素細胞(melanophore),即吞噬了黑色素的 組織細胞,因不含酪氨酸酶,故多巴反應陰性。用此方法可以鑒別黑色素細胞和噬黑色素細胞。人的垂體所分泌的ACTH能刺激黑色素細胞,促進其黑色素形成。 當腎上腺功能低下時(例如Addison病時),全身皮膚黑色素增多,這是由於腎上腺皮質激素分泌減少,對垂體的反饋抑制作用減弱,致ACTH分泌增多, 促進黑色素細胞產生過多的黑色素所致。局限性黑色素增多則見於黑色素痣及黑色素瘤等。
7.病理性鈣化 正常機體內只有骨和牙含有固態的鈣鹽,如在骨和牙之外的其他部位組織內有固態的鈣鹽沉積,則稱為病理性鈣化。沉積的鈣鹽主要是磷酸鈣,其次為碳酸鈣。
在HE染色時,鈣鹽呈藍色顆粒狀,開始時顆粒微細,以後聚集成較大顆粒或片塊,量多時肉眼可見為白色石灰樣質塊,難以完全吸收而成為機體內長期存在的異物,並刺激周圍結締組織增生而將其包裹。
病理性鈣化主要有營養不良性鈣化和轉移性鈣化兩種。前者頗常見,乃變性壞死組織或異物的鈣鹽沉積,如結核壞死灶、脂肪壞死灶、動脈粥樣硬化斑塊內的變性壞死區,壞死的寄生蟲蟲體、蟲卵以及其他異物等。此時,因無全身性鈣磷代謝障礙,故血鈣不升高。
營 養不良性鈣化的機制尚未闡明,可能與局部鹼性磷酸酶升高有關:鹼性磷酸酶能水解有機磷酸酶,使局部磷酸增多,超過3Ca2+×2PO43-的常值,於是形 成磷酸鈣沉澱。至於磷酸酶的來源,一部分顯然是來自壞死細胞中的溶酶體,另一部分則可能系吸收自周圍組織液中的磷酸酶。此外,鈣化與局部組織的pH變動有 關。變性壞死組織的酸性環境可使局部鈣鹽溶解,鈣離子濃度升高,爾後由於組織液的緩衝作用,局部組織鹼性化,故鈣鹽乃析出沉積。
轉移性鈣化 較少見,是全身性鈣、磷代謝障礙致血鈣和(或)血磷升高,使鈣鹽在未受損的組織上沉積所致。如甲狀旁腺功能亢進及骨腫瘤造成骨質嚴重破壞時,大量骨鈣進入 血液,使血鈣升高,以致鈣在腎小管、肺泡和胃粘膜等處沉積,形成轉移性鈣化。此外,接受超劑量的維生素D時,因促進鈣從腸吸收,也可引起轉移性鈣化。
鈣 化對機體的影響視具體情況而異。轉移性鈣化可使鈣化的組織、細胞喪失;血管壁鈣化使血管失去彈性變脆,容易破裂出血。但結核病灶的鈣化則有可能使其中的結 核菌逐漸失去活力,減少複發的危險。然而結核菌在鈣化灶中往往可以繼續存活很長時間,一旦機體抵抗力下降,則仍有可能引起複發。
| 關於「病理學/變性和物質沉積」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |