寄生蟲學/寄生蟲學實驗診斷技術
| 醫學電子書 >> 《人體寄生蟲學》 >> 寄生蟲學實驗技術 >> 寄生蟲學實驗診斷技術 |
| 人體寄生蟲學 |
|
|
|
一、病原檢查
(一)糞便檢查
糞便檢查是診斷寄生蟲病常用的方法。要取得準確的結果,糞便必須新鮮,送檢時間一般不宜超過24小時。如檢查腸內原蟲滋養體,最好立即檢查。盛糞便的容器要乾淨,並防止污染與乾燥;糞便不可混雜尿液等,以免影響檢查結果。
1.直接塗片法 用以檢查蠕蟲卵、原蟲的包囊和滋養體。方法簡便,連續作3次塗片,可提高檢出率。
⑴蠕蟲卵檢查:滴一滴生理鹽水於潔淨的載玻片,用棉簽棍或牙籤挑取綠豆大小的糞便塊,在生理鹽水中塗抹均勻;塗片的厚度以透過塗片約可辨認書上的字跡為宜。一般在低倍鏡下檢查,如用高倍鏡觀察,需加蓋片。應注意蟲卵與糞便中異物的鑒別。蟲卵都具有一定形狀和大小;卵殼表面光滑整齊,具固有色澤;卵內含卵細胞或幼蟲。
⑵原蟲檢查:
1)活滋養體檢查:塗片應較薄,方法同查蠕蟲卵。氣溫愈接近體溫,滋養體的活動愈明顯。必要時可用保溫台保持溫度。
2)包囊的碘液染色檢查:直接塗片方法同上,以一滴碘液代替生理鹽水。如碘液過多,可用吸水紙從蓋片邊緣吸去過多的液體。若同時需檢查活滋養體,可在用生理鹽水塗勻的糞滴附近滴一滴碘液,取少許糞便在碘液中塗勻,再蓋上蓋片(圖21-1)。塗片染色的一半查包囊;末染色的一半查活滋養體。
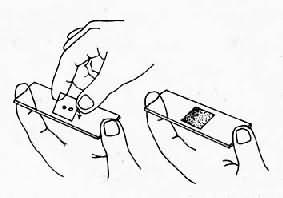
圖21-1 原蟲包囊碘液染色操作方法
3)隱孢子蟲卵囊染色檢查:目前較佳的方法為金胺酚改良抗酸染色法。對於新鮮糞便或經10%福爾馬林固定保存(4℃1個月內)的含卵囊糞便都可用此法染色。染色過程是先用金胺-酚染色,再用改良抗酸染色法復染。方法步驟如下:
金胺-酚染色法:
①染液配製:1g/L金胺-酚染色液(第一液):金胺0.1g,石碳酸5.0g,蒸餾水100ml;3%鹽酸酒精(第二液):鹽酸3ml,95%酒精100ml;5g/L高錳酸鉀液(第三液):高錳酸鉀0.5g,蒸餾水100ml。
②染色步驟:滴加第一液於晾乾的糞膜上,10~15分鐘後水洗;滴加第二液,1分鐘後水洗;滴加第三液,1分鐘後水洗,待干;置熒光顯微鏡檢查。
低倍熒光鏡下,可見卵囊為一圓形小亮點,發現乳白色熒光。高倍鏡下卵囊呈乳白或略帶綠色,卵囊壁為一薄層,多數卵囊周圍深染,中央淡染,似環狀,或深染結構偏位,有些卵囊全部為深染。但有些標本可出現非特異的熒光顆粒,應注意鑒別。
改良抗酸染色法:
①染液配製:石炭酸復紅染色液(第一液):鹼性復紅4g, 95%酒精20ml,石炭酸8ml,蒸餾水100ml;10%硫酸溶液(第二液):純硫酸10ml,蒸餾水90ml(邊攪拌邊將硫酸徐徐傾入水中;20g/L孔雀綠液(第三液):20g/L孔雀綠原液1ml,蒸餾水10ml。
②染色步驟:滴加第一液於糞膜上,1.5~10分鐘後水洗;滴加第二液,1~10分鐘後水洗;滴加第三液,1分鐘後水洗,待干;置顯微鏡下觀察。
經染色後,卵囊為玫瑰紅色,子孢子呈月牙形,共4個。其他非特異顆粒則染成藍黑色,容易與卵囊區分。
不具備熒光鏡的實驗室,亦可用上述方法先後染色,然後在光鏡低、高倍下過篩檢查,發現小紅點再用油鏡觀察。效果好,可提高檢出速度和準確性。
2.厚塗片透明法(改良加藤法)取約5mg(已用100目不鏽鋼篩除去糞渣)糞便,置於載玻片上,覆以浸透甘油-孔雀綠溶液的玻璃紙片,輕壓,使糞便鋪開(20×25mm)。置於30~36℃溫箱中約半小時或25℃約1小時。待糞膜稍干,即可鏡檢。
玻璃紙準備:將玻璃紙剪成22×30mm大小的小片,浸於甘油-孔雀綠溶液(含純甘油100ml、水100ml和3%孔雀綠1ml的水溶液)中,至少浸泡24小時,至玻璃紙呈現綠色。
使用此法需掌握糞膜的合適厚度和透明的時間。如糞膜厚,透明時間短,蟲卵難以發現;如透明時間過長,則蟲卵變形,也不易辨認。
3.濃聚法
⑴沉澱法:原蟲包囊和蠕蟲卵的比重大可沉集於水底,有助於提高檢出率。但比重較小的鉤蟲卵和某些原蟲包囊則效果較差。
1)重力沉澱法:取糞便20~30g、加水成混懸液,經金屬篩(40~60孔)或2、3層濕紗布過濾,再加清水沖洗殘渣;過濾糞液在容器中靜置25分鐘,倒去上液,重新加滿清水,以後每隔15~20分鐘換水一次(3~4次),直至上液清晰為止。最後倒去上液,取沉渣作塗片鏡檢。如檢查包囊,換水間隔時間宜延長至約6小時換一次(圖21-2)。
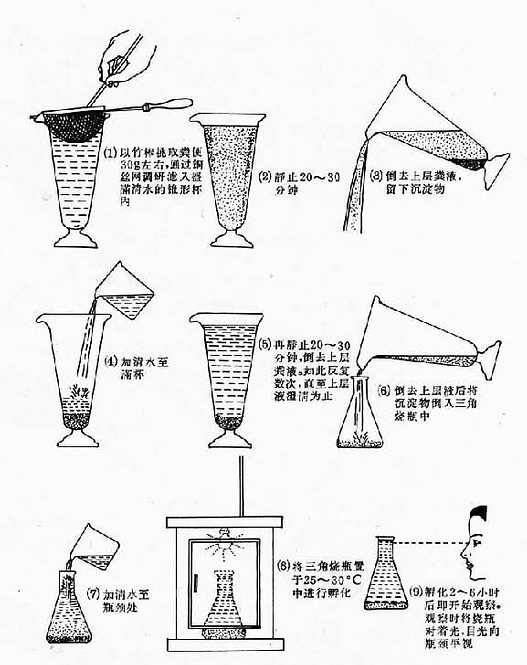
圖21-2 糞便沉澱及毛蚴孵化法
2)離心沉澱法:將上述濾去粗渣的糞液離心(1500~2000rpm/min)1~2分鐘,倒去上液,注入清水,再離心沉澱,如此反覆沉澱3~4次,直至上液澄清為止,最後倒去上液,取沉渣鏡檢。
3)汞碘醛離心(MIFC)沉澱法:糞便1g,加適量(約10ml)汞碘醛液,充分調勻,用2層脫脂紗布過濾,再加入乙醚4ml,搖2分鐘,離心(2000rpm/min)1~2分鐘,即分成乙醚、糞渣、汞碘醛及沉澱物4層。吸棄上面3層,取沉渣鏡檢。
汞碘醛配製:
①汞醛(MF)液:1/1000硫柳汞酊200ml,甲醛(40%)25ml,甘油50ml,蒸餾水200ml。
②盧戈氏液:碘5g,碘化鉀10g,蒸餾水100ml。
檢查時取汞醛液2.35ml及5%盧戈氏液0.15ml混合備用。但混合液在8小時後即變質,不應再用;碘液亦不這且於1周後再用。
4)醛醚沉澱法:置糞便1~2g於小容器內,加水10~20ml調勻,將糞便混懸液經2層紗布(或100目金屬篩網)過濾,離心(2000rpm/min)2分鐘;倒去上層糞液,保留沉渣,加水10ml混勻,離心2分鐘;倒去上液,加10%甲醛7ml。5分鐘後加乙醚3ml,塞緊管口並充分搖勻,取下管口塞,離心2分鐘,即可見管內自下而上分為4層。取管底沉渣塗片鏡檢。如檢查原蟲包囊,可加盧戈氏液染色,加蓋片鏡檢。
⑵浮聚法:利用比重較大的液體,使原蟲包囊或蠕蟲卵上浮,集中於液體表面。常用的方法有兩種:
1)飽和鹽水浮聚法:此法用以檢查鉤蟲卵效果最好。用竹籤取黃豆粒大小的糞便置於浮聚瓶(高3.5cm,直徑約2cm的圓形直筒瓶)中,加入少量飽和鹽水調勻,再慢慢加入飽和鹽水到液面略高於瓶口,但不溢出為止。此時在瓶口覆蓋一載玻片,靜置15分鐘後,將載玻片提起並迅速翻轉,鏡檢(圖21-3)。
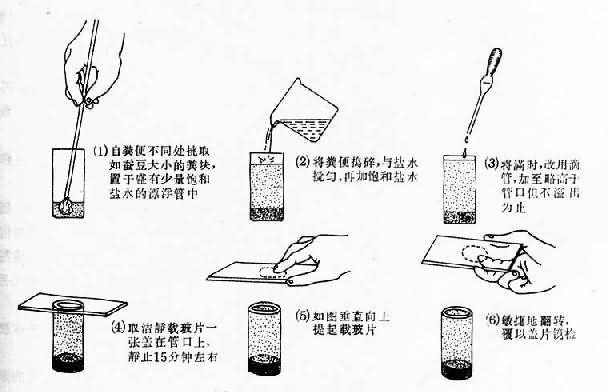
圖21-3 飽和鹽水浮聚法
飽和鹽水配製:將食鹽徐徐加入盛有沸水的容器內,不斷攪動,直至食鹽不再溶解為止。
2)硫酸鋅離心浮聚法:此法可用於檢查原蟲包囊,球蟲卵囊和蠕蟲卵。取糞便約1g,加10~15倍的水,充分攪碎,按離心沉澱法過濾,反覆離心3~4次,至水清為止,最後倒去上液,在沉渣中加入比重1.18的硫酸鋅液(33%的溶液),調勻後再加硫酸鋅溶液至距管口約1cm處,離心1分鐘。用金屬環取表面的糞液置於載玻片上,加碘液一滴,鏡檢。
3)蔗糖離心浮聚法:此法適用於檢查糞便中隱孢子蟲的卵囊。取糞便約5g,加水15~20ml,以260目尼龍袋或4層紗布過濾。取濾液離心5~10分鐘,吸棄上清液,加蔗糖溶液(蔗糖500g,蒸餾水320ml,石炭酸6.5ml)再離心,然後如同飽和鹽水浮聚法,取其表液膜鏡檢(高倍或油鏡)。卵囊透明無色,囊壁光滑,內有一小暗點和發出淡黃色的子孢子。隱孢子蟲的卵囊在漂浮液中浮力較大,常緊貼於蓋片之下,但1小時後卵囊脫水變形不易辨認,故應立即鏡檢。也可用飽和硫酸鋅溶液或飽和鹽水替代蔗糖溶液。
常見蠕蟲卵、包囊的比重如表21-1。
表21-1 蠕蟲卵及包囊的比重
| 蟲卵或包囊 | 比 重 |
| 華支睾吸蟲卵 | 1.170~1.190 |
| 薑片吸蟲卵 | 1.190 |
| 肝片形吸蟲卵 | 1.200 |
| 日本血吸蟲卵 | 1.200 |
| 帶絛蟲卵 | 1.140 |
| 微小膜殼絛蟲卵 | 1.050 |
| 鉤蟲卵 | 1.055~1.080 |
| 鞭蟲卵 | 1.150 |
| 蟯蟲卵 | 1.105~1.115 |
| 受精蛔蟲卵 | 1.110~1.130 |
| 未受精蛔蟲卵 | 1.210~1.230 |
| 毛圓線蟲卵 | 1.115~1.130 |
| 溶組織內阿米巴包囊 | 1.060~1.070 |
| 結腸內阿米巴包囊 | 1.070 |
| 微小內蜒阿米巴包囊 | 1.065~1.070 |
| 藍氏賈第鞭毛蟲包囊 | 1.040~1.060 |
4.毛蚴孵化法 依據血吸蟲卵內的毛蚴在適宜溫度的清水中,短時間內可孵出的特性而設計的方法,適用於星期血吸蟲病患者的糞便檢查。取糞便約30g,先經重力沉澱法濃集處理,將糞便沉渣倒入三角燒瓶內,加清水(城市中需用去氯水)至瓶口,在20~30℃的條件下經4~6小時後肉眼或放大鏡觀察結果。如見水面下有白色點狀物作直線來往遊動,即是毛蚴。必要時也可用吸管將毛蚴吸出鏡檢。如無毛蚴,每隔4~6小時(24小時內)觀察一次。氣溫高時,毛蚴可在短時間內孵出,因此在夏季要用1.2%食鹽水或冰水沖洗糞便,最後一次才改用室溫清水(圖21-2)。
毛蚴促孵法:將沉澱法處理後的糞便沉渣置於三角瓶內,不加水,或將糞渣置於吸水紙上,再放在20~30℃溫箱中過液。檢查時,加清水,2小時後就可見到孵出的毛蚴。此法毛蚴孵出時間較一致,數量也較多。
5.肛門拭子檢查法 適用於在肛周產卵(蟯蟲),或常在肛門附近發現蟲卵(帶絛蟲)的蟲卵檢查法。
⑴棉簽拭子法:先將棉簽浸泡在生理鹽水中,取出時擠去過多的鹽水,在肛門周圍擦拭,隨後將棉簽放入盛有飽和鹽水的試管中,用力攪動,迅速提起棉簽,在試管內壁擠干鹽水後充去,再加飽和鹽水至管口處,覆蓋一載玻片,務使其接觸液面,5分鐘後取載玻片鏡檢。也可將擦拭肛周的棉簽放在盛清水的試管中,經充分浸泡,取出,在試管內壁擠去水分後棄去。試管靜置10分鐘,或經離心後,倒去上液,取沉渣鏡檢。
⑵透明膠紙法:用長約6cm,寬約2cm的透明膠紙粘擦肛門周圍的皮膚,取下膠紙,將有膠面平貼玻片上,鏡檢。
6.試管濾紙培養法 也稱鉤蚴培養法。根據鉤蟲卵在適宜條件下可在短時間內孵出幼蟲的原理設計的方法。如冷開水約1ml於潔淨試管內(1×10cm),將濾紙剪成與試管等寬但較試管稍長的T字型紙條,用鉛筆書寫受檢者姓名或編號於橫條部分。取糞便約0.2~0.4g,均勻地塗抹在緊豎條紙條的上部2/3處,再將紙條插入試管,下端浸泡在水中,以糞便不接觸水面為度。在20~30℃條件下培養。培養期間每天沿管壁補充冷開水,以保持水面位置。3天後肉眼或放大鏡檢查試管底部。鉤蚴在水中常作蛇形遊動,蟲體透明。如未發現鉤蚴,應繼續培養觀察至第5天。氣溫太低時可將培養管放入溫水(30℃左右)中數分鐘後,再行檢查(圖21-4)。
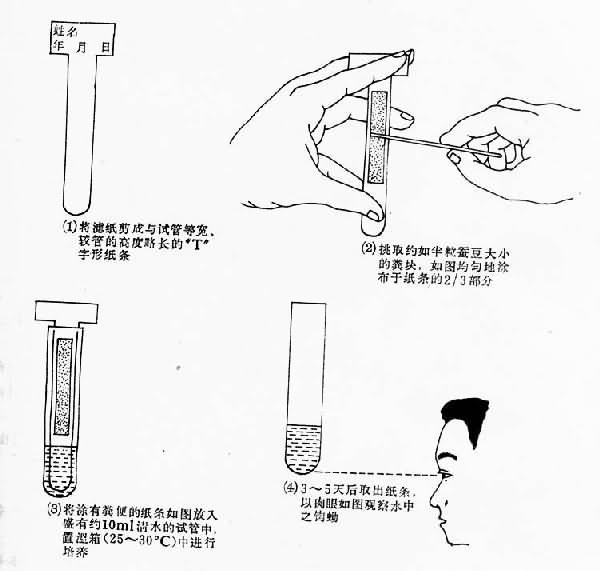
圖21-4 鉤蚴培養法
此法亦可用於分離人體腸道內各種阿米巴滋養體及人毛滴蟲滋養體,且能提高檢出率。但是,每管糞便量應為1.0g;適宜溫度為25~30℃;培養時間為2~4天。臨床上為了及時報告致病原蟲,可於培養48小時後鏡檢。檢查腸道各種原蟲,仍應結合碘液塗片法以檢出原蟲包囊。
7.蟲卵計數法 蟲卵計數用於估計人體內寄生蟲的感染度,常用司徒爾(Stoll)氏法,即司氏稀釋蟲卵計數法(圖21-5)。
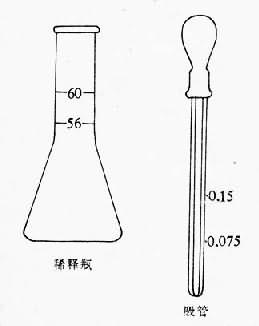
圖21-5 司氏蟲卵計數法
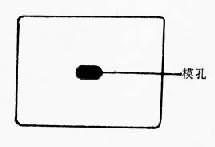
圖21-6 定量板
用特製的三角燒瓶(或普通三角燒瓶),容量為65ml左右,在燒瓶的頸部相當於56和60ml處有兩個刻度。先把0.1mol/lNaOH溶液倒入瓶內至56ml處,再慢慢地加入糞便,到液面上升到60ml處,然後放進玻璃珠10餘顆,用橡膠塞塞緊瓶口,充分搖動,使其成為十分均勻的混懸液。
計數時充分搖勻,用有刻度的小吸管取0.075或0.15ml糞液置於載玻片上,加蓋片,在低倍鏡下計算全片的蟲卵數。乘以200(吸0.075ml)或100(吸0.15ml)即得每克為糞便蟲卵數。由於糞便的性狀明顯地影響估算結果,因此不成形的糞便的蟲卵數應再乘糞便性狀係數,即半成形糞便×1.5,軟濕形糞便×2,粥狀糞便×3,水瀉形糞便×4。
每克糞便含卵數×24小時糞便克數
雌蟲數= 已知雌蟲每天排卵總數
成蟲總數=雌蟲總數×2
8.定量透明法 適用於各種糞便內蠕蟲卵的檢查及計數。此法系應用改良聚苯乙烯作定量板(圖21-6),大小為40×30×1.37mm,模孔為一長圓孔,大小為8×4mm,兩端呈半圓形,所取的糞樣平均為41.7mg。操作時將大小約4×4cm的100目尼龍網或金屬篩網覆蓋在糞便標本上,自篩網上用刮片刮取糞便,置定量板於載玻片上,用一手的兩指壓住定量板的兩端,將刮片上的糞便填滿模孔,颳去多餘糞便。掀起定量板,載玻片上留下一個長形糞樣,然後在糞條上覆蓋含甘油-孔雀綠溶液的大小約為5.0~2.6cm的玻璃紙條,展平後加壓,使玻璃紙下的糞便鋪成長橢圓形。經1~2小時糞便透明後置鏡下計數。將所得蟲卵數×24,再乘上述糞便性狀係數,即為每克糞便蟲卵數(eggs per gram,EPG)。常見蠕蟲的每條雌蟲每天排卵數如表21-2。
表21-2 各種蠕蟲每條雌蟲每日排卵數
| 蟲 名 | 產卵數/日/條(平均數) |
| 華支睾吸蟲 | 1600~4000(2400) |
| 薑片蟲 | 15000~48000(25000) |
| 衛氏並殖吸蟲 | 10000~20000 |
| 日本血吸蟲 | 1000~3500 |
| 豬帶絛蟲 | 30000~50000/孕節 |
| 牛帶絛蟲 | 97000~124000/孕節 |
| 十二指腸鉤蟲 | 10000~30000(24000) |
| 美洲鉤蟲 | 5000~10000(9000) |
| 蛔蟲 | 234000~245000(240000) |
| 鞭蟲 | 1000~7000(2000) |
9.淘蟲檢查法 為考核驅蟲療效,常需從糞便中淘取蠕蟲進行鑒定與計數。取患者服藥後24~72小時的全部糞便,加水攪拌,用篩(40目)或紗布濾出糞渣,經水反覆沖洗後,倒在盛有清水的大型玻皿內。檢查混雜在糞渣中的蟲體時,應在玻皿下襯以黑紙。
10.帶絛蟲孕節檢查法 絛蟲節片用清水洗淨,置於兩載玻片之間,輕輕壓平,對光觀察內部結構,並根據子宮分支情況鑒定蟲種。也可用注射器從孕節後端正中部插入子宮內徐徐注射炭素墨汁或卡紅,待子宮分支顯現後計數。
卡紅染液配製:鉀明礬飽和液100ml,卡紅3g,冰醛酸10ml。混合液置於37℃溫箱內過夜,過濾後即可應用。
(二)血液檢查
血液檢查是診斷瘧疾、絲蟲病的基本方法。塗制血膜用的載玻片用前需經洗滌液處理,自來水、蒸餾水沖洗,在95%酒精中浸泡,擦乾或烤乾後使用。
洗滌液配製:常用玻璃器皿的洗滌液為鉻酸洗液,含工業濃硫酸100ml,重鉻酸鉀80g,水1000ml。先用冷水將重鉻酸鉀溶化,然後徐徐加入濃硫酸,同時用玻璃棒攪拌。
1.檢查瘧原蟲
⑴取血與塗片:用75%酒精棉球消毒耳垂,待干後用左手拇指與食指捏著耳垂下方,並使耳垂下側方皮膚繃緊,右手持取血針、刺破皮膚,擠出血滴。薄、厚血膜可塗制在同一張玻片上(圖21-7)。
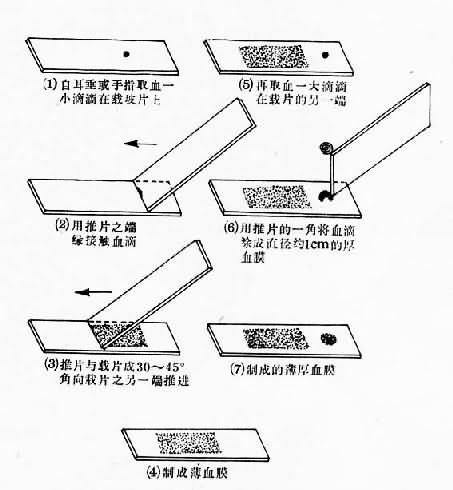
圖21-7 薄厚血膜製作步驟
1)薄血膜製片:在載玻片1/3與2/3交界處蘸血一小滴,以一端緣光滑的載片為推片,將推片的一端置於血滴之前,待血液沿推片端緣擴散後,自右向左推成薄血膜。操作時兩載片間的角度為30~45℃,推動速度適宜。理想的薄血膜,應是一層均勻分布的血細胞,血細胞間無空隙且塗血膜末端呈掃帚狀。
2)厚血膜製片:載玻片的另一端(右)1/3處蘸血一小滴(約10mm³),以推片的一角,將血滴自內向外作螺旋形攤開,使之成為直徑約0.8~1cm,厚薄均勻的厚血膜。厚血膜為多層血細胞的重疊,約等於20倍薄血膜的厚度。
⑵固定與染色:血片必須充分晾乾,否則染色時容易脫落。固定時用小玻棒蘸甲醇或無水酒精在薄血膜上輕輕抹過。如薄、厚血膜在同一玻片上,須注意切勿將固定液帶到厚血膜上,因厚血膜固定之前必須先進行溶血。可用滴管滴水於厚血膜上,待血膜呈灰白色時,將水倒去,晾乾。在稀釋各種染液和沖洗血膜時,如用緩衝液則染色效果更佳。緩衝液的配製如下:
磷酸氫二鈉液:磷酸氫二鈉(Na2HPO4)無水0.464g或Na2HPO4. 2H2O11.867g或Na2HPO4. 7H2O17.872g或Na2HPO4. 2H2O23.877g,蒸餾水1000ml。
M/15磷酸二氫鉀液:磷酸二氫鉀(Na2HPO4)9.073g,蒸餾水1000ml。
使用時將上述原液按下頁表配成不同的pH緩衝液:
| pH | M/15KH2PO4(ml) | M/15Na2HPO4(ml) | 蒸餾水(ml) |
| 6.8 | 4.9 | 5.1 | 90 |
| 7.0 | 6.3 | 3.7 | 90 |
| 7.2 | 7.3 | 2.7 | 90 |
染色時臨時配成pH7.0或7.2的緩衝液。
常用的染色劑有姬氏染劑(Giemsa's stain)、瑞氏染劑(Wright's stain)。
1)Giemsa染色法:此法染色效果良好,血膜褪色較慢,保存時間較久,但染色需時較長。
染液配製:姬氏染劑粉1g,甲醇50ml,純甘油50ml。將姬氏染粉置於研缽中(最好用瑪瑙研缽),加小量甘油充分研磨,加甘油再磨,直至50ml甘油加完為止,倒入棕色玻瓶中。然後分幾次用少量甲醇沖洗缽中的甘油染粉,倒入玻瓶,直至50ml甲醇用完為止,塞緊瓶塞,充分搖勻,置65℃溫箱內24小時或室溫內一周過濾。
染色方法:用pH7.0~7.2的緩衝液,將姬氏液稀釋;比例約為15~20份緩衝液加1份姬氏染液。用蠟筆划出染色範圍,將稀釋的姬氏染液滴於已固定的薄、厚血膜上,染色半小時(室溫),再用上述緩衝液沖洗。血片晾乾後鏡檢。
2)快速姬色染色法:姬氏染液1ml,加緩衝液5ml,如前法染色5分鐘後用緩衝液沖洗,晾乾後鏡檢。
3)Wright染色法:此法操作簡便,適用於臨床診斷,但甲醇蒸發甚快,掌握不當時易在血片上發生染液沉澱,並較易褪色,保存時間不長。多用於臨時性檢驗。
染液配製:瑞氏染劑粉0.1~0.5g,甲醇97ml,甘油3ml。將瑞氏染劑加入甘油中充分研磨,然後加入少量甲醇,研磨後倒入瓶內,再分幾次用甲醇沖洗研缽中的甘油溶液,倒入瓶內,直至用完為止,搖勻,24小時後過濾待用。一般1、2周後再過濾。
染色方法:瑞氏染液含甲醇,薄血膜不需先固定;而厚血膜則需先經溶血,待血膜干後才能染色。染色前先將溶過血的厚血膜和薄血膜一起用蠟筆劃好染色範圍,以防滴加染液時四溢。滴染液使覆蓋全部厚、薄血膜上,30秒至1分鐘後用滴管加等量的蒸餾水,輕輕搖動載玻片,使蒸餾水和染液混合均勻,此時出現一層燦銅色浮膜(染色),3~5分鐘後用水緩慢地從玻片一端沖洗(注意勿先倒去染液或直對血膜沖洗),晾乾後鏡檢。
2.檢查微絲蚴
⑴新鮮血片檢查:晚間9時至次晨2時取血1滴滴於載玻片上,加蓋片,在低倍鏡下觀察,發現蛇形遊動的幼蟲後,仍須作染色檢查,以確定蟲種。
⑵厚血膜檢查:厚血膜的製作、溶血、固定與姬氏液染色同瘧原蟲。但需取血3滴,也可用Delafieid蘇木素染色法染色。該染液的配製方法如下:
蘇木素1g溶於純酒精或95%酒精10ml中,加飽和硫酸鋁銨(8%~10%)100ml,倒入棕色瓶中,瓶口用兩層紗布紮緊,在陽光下氧化2~4周,過濾,加甘油25ml和甲醇25ml,用時稀釋10倍左右。
已溶血、固定的厚血膜在德氏蘇木素液內染10~15分鐘,在1%酸酒精中分色1~2分鐘,蒸餾水洗滌1~5分鐘,至血膜呈藍色,再用1%伊紅染色0.5~1分鐘,以水洗滌2~5分鐘,晾乾後鏡檢。
⑶活微絲蚴濃集法:在離心管內裝蒸餾水半管,加血液10~12滴,再加生理鹽水混勻,離心沉澱3分鐘,取沉渣檢查。或取靜脈血1ml,置於盛有3.8%枸櫞酸鈉0.1ml的試管中,搖勻,加水9ml,俟紅細胞溶化後,離心(3000rpm/min)2分鐘,倒去上液,加水再離心,取沉渣鏡檢。
(三)排泄物與分泌物等的檢查
1.痰液 痰中可能查見肺吸蟲卵、溶組織內阿米巴滋養體、棘球蚴的原頭蚴、糞類圓線蟲幼蟲、蛔蚴、鉤蚴、塵蟎等;卡氏肺孢子蟲的包囊也可出現於痰中,但檢出率很低。
⑴肺吸蟲卵檢查:可先用直接塗片法檢查,如為陰性,改用濃集法集卵,以提高檢出率。
直接塗片法:在潔淨載玻片上先加1~2滴生理鹽水,挑取痰液少許,最好選帶鐵鏽色的痰,塗成痰膜,加蓋片鏡檢。如未發現肺吸蟲卵,但見有夏科-雷登晶體,提示可能是肺吸蟲患者,多次塗片檢查為陰性者,可改用濃集法。
濃集法:收集24小時痰液,置於玻璃杯中,加入等量10%NaOH溶液,用玻棒攪勻後,放入37℃溫箱內,數後痰液消化成稀液狀。分裝於數個離心管內,以1500rpm/min離心5~10分鐘,充去上清液,取沉渣滴塗片檢查。
⑵溶組織內阿米巴大滋養體檢查:取新鮮痰液作塗片。天冷時應注意鏡台載玻片保溫。高倍鏡觀察。如為阿米巴滋養體,可見其伸出偽足並作定向運動。
⑶上述其他的蠕蟲幼蟲及蟎類等宜用濃集法檢查。
2.十二指腸液和膽汁 用十二指腸引流管抽取十二指腸液及膽汁,以直接塗片法鏡檢;也可經離心濃集後,吸取沉渣鏡檢。可檢查藍氏賈第鞭毛蟲滋養體、華支睾吸蟲卵、肝片形吸血卵和布氏薑片蟲卵等;急性阿米巴肝膿腫患者偶在膽汁中發現大滋養體。
檢查方法:可將各部分指腸引流液滴於載玻片上,加蓋片後直接鏡檢。為提高寄生蟲檢出率,常將各部分引流加生理鹽水稀釋攪抖後,分裝離心管,以2000rpm/min,離心5~10分鐘,吸取沉渣塗片鏡檢。如引流液過於粘稠,應先加10%NaOH消化後再離心。引流中的賈第蟲滋養體常附著在粘液小塊上,或蟲體聚集成絮片狀物。肝片形吸蟲卵與薑片蟲卵不易鑒別,但前者可出現於膽汁;而後者只見於十二指腸液中。
3.尿 一般先離心,後取沉渣鏡檢。但乳糜尿需加等量乙醚,用力振蕩,使脂肪溶於乙醚。然後吸去脂肪層,離心,取沉渣鏡檢。
4.鞘膜積液 主要檢查班氏微絲蚴。陰囊皮膚經碘酒精消毒後,用注射器抽取鞘膜積液作直接塗片檢查,也可加適量生理鹽水稀釋離心,取沉渣鏡檢。
直接塗片法:用消毒棉簽在受檢查者陰道後穹窿、子宮頸及陰道壁上取分泌物,然後在有1~2滴生理鹽水的載玻片上作塗片鏡檢,可發現活動的蟲體。天氣寒冷時,應注意保溫。
懸滴法:取陰道分泌物置於周緣塗抹一薄層凡士林蓋片上的生理鹽水中,翻轉蓋片小心覆蓋在具凹孔的載玻片上,稍加壓使兩片粘合,液滴懸於蓋片下面,鏡檢。
(四)其它器官組織檢查
1.骨髓穿刺 主要檢查杜氏利什曼原蟲無鞭毛體。一般常作髂骨穿刺,患者側臥,露出髂骨部位。視年齡大小,選用17~20號帶有針芯的乾燥無菌穿刺針,從髂骨前上刺後約1cm處刺入皮下,當針尖觸及骨面時,再慢慢地鑽入骨內約0.5~1.0cm,即可拔出針芯,接上2ml的乾燥注射器,抽取骨髓液。取少許骨髓液作塗片;甲醇固定,同薄血膜染色法染色,油鏡檢。
2.淋巴結穿刺
⑴利什曼原蟲:檢出率低於骨髓穿刺,但方法簡便、安全,且患者經治療後,淋巴結內原蟲消失較慢,故仍有一定價值。一般選腹股溝部,先將局部皮膚消毒,用左手拇指和食指捏住一個較大的淋結,右手取乾燥無菌的6號針頭刺入淋巴結,此時淋巴結組織液自能進入針內。稍待片刻,拔出針頭,將針頭內少量的淋巴結組織液注於載玻片上,作塗片染色檢查。也可用摘除的淋巴結的切面做塗片,染色後鏡檢。
⑵絲蟲成蟲:可用注射器從可疑的淋巴結節中抽取成蟲,或剖檢摘除的結節尋找成蟲,也可作病理組織切片檢查。
3.肌肉活檢
⑴旋毛蟲幼蟲:用外科手術從患者的腓腸肌或肱或股二頭肌取米粒大小的肌肉一塊,置於載玻片上,加50%甘油滴,蓋上另一載玻片,均勻用力壓緊,低倍鏡下觀察。取下肌肉須立即檢查,否則幼蟲變得模糊,不易檢查。
⑵豬囊尾蚴:摘取肌肉內的結節,剝除外層纖維被膜,在2張載玻片間壓平、鏡檢。也可經組織固定後作切片染色檢查。
4.皮膚 檢查疥蟎,蠕形蟎,利什曼原蟲等。
⑴疥蟎:參看「疥蟎和疥瘡」!一節。
⑵蠕形蟎:參看「蠕形蟎和蠕形蟎病」一節。
⑶利什曼原蟲:在皮膚上出現丘疹和結節等疑似皮膚型黑熱病患者,可選擇皮損較明顯之處,作局部消毒,用乾燥滅菌的注射器,刺破皮損處,抽取組織液作塗片;或用消毒的鋒利小剪,從皮損表面剪取一小片皮膚組織,以切面作塗片;也可用無菌解剖刀切一小口,刮取皮膚組織作塗片。以上塗片均用瑞氏或姬氏染液染色。如塗片未見原蟲,可割取小丘疹或結節,固定後,作組織切片染色檢查。
5.直腸粘膜 用直腸鏡從直腸粘膜病變組織內可查見日本血吸蟲卵及溶組織阿米巴滋養體。
日本血吸蟲卵:用直腸鏡自直腸取米粒大小的粘膜一塊,經水洗後,放在2載玻片間,輕輕壓平,鏡檢。蟲卵鑒別見表21。-3。
表21-3 粘膜內血吸蟲卵未染色之鑒別
| 活卵 | 近期變性卵 | 死卵(鈣化卵) | |
| 顏色 | 淡黃至黃褐色 | 灰白至略黃色 | 灰褐色至棕紅 |
| 卵殼 | 較薄 | 薄或不均勻 | 厚而不均勻 |
| 胚膜 | 清楚 | 清楚 | 不清楚 |
| 內含物 | 卵黃細胞或胚團或毛蚴 | 淺灰色或黑色小點或折光均勻的顆粒或萎縮的毛蚴 | 兩極可有密集的黑點含網狀結構或塊狀物 |
溶組織阿米巴:用乙狀結腸鏡觀察潰瘍形狀,自潰瘍邊緣或深層刮取潰瘍組織,置於載玻片上,加少量生理鹽水,蓋上蓋片,輕輕壓平,立即鏡檢。也可取出一小塊病變的粘膜組織,固定切片,染色檢查。
6.肺組織 檢查卡氏肺孢子蟲包囊。取一小塊肺組織作塗片,自然乾燥後甲醇固定,用改良銀染色法進行染色。
改良銀染色法染色步驟:
1.將肺塗片置於5%鉻酸,氧化15分鐘,溫度為20℃。氧化後的標本均從流水沖洗數秒。
2.1%亞硫酸氫鈉經1分鐘,自來水沖洗後,蒸餾水洗滌3~4次。
3.放入四胺銀工作液內,並在60℃孵育約90分鐘,至標本轉至黃褐色為止。流水、蒸餾水各洗5分鐘。
4.0.1%氯化金2~5分鐘,蒸餾水洗4~5次。
5.2%硫代硫酸鈉5分鐘,流水至少洗10分鐘。
6.亮緣復染45秒。
7.95%,99%,100%乙醇逐級脫水。
8.二甲苯透明3次,樹膠封片。
染色結果顯示,卡氏肺孢子蟲包囊呈圓形、卵圓形或不規則的多角形,囊壁為淡褐色或深褐色。紅細胞為淡黃色,其餘背景呈淡綠色。
二、免疫論斷及新技術應用
(一)皮內試驗
利用宿主的速髮型變態反應,將特異抗原液注入皮內,觀測皮丘及紅暈反應以判斷有無特異抗體(IgE)的存在稱皮內試驗(intradermal test,IDT)。
皮內試驗用於多種寄生蟲病的檢測,如血吸蟲病、肺吸蟲病等。最常用於血吸蟲病的調查,操作簡單,並且可即時觀察結果,適宜現場應用。大多用粗製可溶性血吸蟲蟲卵抗原(稀釋度為1:4000)或成蟲冷浸抗原(稀釋度為1:8000)敏感性高,其陽性率在93%~97%,但有部分假陽性反應(2.1%~3.5%),並且對其他寄生蟲病交叉反應較高。皮內試驗可用作①過篩方法,先作皮試,陽性者再作進一步追查;②臨床輔助診斷;③考核預防效果,用作檢查新感染的方法,特別對兒童。
(二)染色試驗
染色試驗(dye test,DT)是比較獨特的免疫反應,是目前診斷弓形蟲病較好的方法,已廣泛用於該病的臨床診斷和流行病學調查。
新鮮弓形蟲滋養體和正常血清混合,在37℃作用1小時或室溫數小時後,大部分弓形蟲失去原來的新月形,而變為圓形或橢圓形,用鹼性美藍染色時著色很深。但新鮮弓形蟲和免疫血清混合時,蟲體仍保持原有形態,用鹼性美藍染色時,著色很淺或不著色。其原因可能是由於弓形蟲受到特異體抗體和輔助因子協同作用後,蟲體細胞變性,結果蟲體對鹼性美藍不易著色。
材料和試劑以弓形蟲速殖子為抗原;採用正常人血清為致活因子。鹼性美藍溶液,取美藍10g加入95%酒精100ml,製成飽和酒精溶液,過濾後取3ml加pH11,要求臨用時新鮮配製。待檢血清經56℃30分鐘滅活,冰箱保存備用。
方法將待檢血清用生理鹽水倍比稀釋,每孔0.1ml,加上述稀釋的弓形蟲速殖子0.1ml,置37℃水浴1小時,加鹼性美藍溶液0.02ml/孔,37℃水浴15分鐘,以每孔聚懸液1滴於載玻片上,加蓋玻片,高倍顯微鏡檢查,計數100個弓形蟲速殖子,統計著色和不著色速殖子比例數。
結果判定以能使50%弓形蟲不著色的血清最高稀釋度為該血清染色試驗陽性效價。陽性血清稀釋度1:8為隱性感染;1:256為活動性感染;1:1024為急性感染。
(三)環卵沉澱試驗
環卵沉澱試驗(circumoval precipitin test,COPT)是以血吸蟲整卵為抗原的特異免疫血清學試驗,卵內毛蚴或胚胎分泌排泄的抗原物質經卵殼微孔滲出與檢測血清內的特異抗體結合,可在蟲卵周圍形成特殊的複合物沉澱,在光鏡下判讀反應強度並計數反應卵的百分率稱環沉率。
1.常規法用載玻片或凹玻片進行,加樣本血清後,挑取適量鮮卵或干卵(約100~150個,從感染動物肝分離),覆蓋24×24mm蓋片,四周用石蠟密封,37℃保溫48小時後,低倍鏡觀察結果,必要時需觀察72小時的反應結果。典型的陽性反應為泡狀、指狀、片狀或細長捲曲狀的折光性沉澱物,邊緣整齊,與卵殼牢固粘連。陰性反應必須觀察全片;陽性者觀察100個成熟卵,計環沉率及反應強度比例。環沉率是指100個成熟蟲卵中出現沉澱物的蟲卵數。凡環沉率≥5%者可報告為陽性,(在基本消滅和消滅血吸蟲病地區環沉率≥3%者可判為陽性),1%~4%者為弱陽性。環沉率在治療上具有參考意義。
2.分級強度判定
「-」折光淡,與蟲卵似連非連;「影狀」物(外形不甚規則,低倍鏡下有折光,高倍鏡下為顆粒狀)及出現直徑小於10μm的泡狀沉澱物者,皆為陰性。
「+」蟲卵外周出現泡狀沉澱物(>10μm),累計面積小於蟲卵面積的1/2;或呈指狀的細長捲曲樣沉澱物,不超過蟲卵的長徑。
「++」蟲卵外周出現泡狀沉澱物的面積大於蟲卵面積的1/2;或細長捲曲樣沉澱相當或超過蟲卵的長徑。
「+++」蟲卵外周出現泡狀沉澱物的面積大於蟲卵本身面積;或細長捲曲樣沉澱物相當或超過蟲卵長徑的2倍。
3.近年來對COPT的方法作了一些改進如①雙面膠紙條法:將雙面膠紙條制特定的式樣作COPT,可省略蠟封片法的繁瑣步驟,具有操作簡易,方法規範,提高工效和避免空氣污染的優點。雙面膠紙條法COPT(DGS-COPT)已在現場擴大應用,今後若能將該法配套干卵,則更能提高它的應用價值;②血吸蟲干卵抗原片(或膜片)環卵沉澱試驗,利用環卵抗原活性物質的耐熱特性,將分離的純卵超聲和熱處理,定量滴加,烤乾固定於載玻片或預製的聚乙稀薄膜上。此種干卵膜片,保存時間較長(4℃半年),已有市售商品。試驗時只需加入血清試樣,濕盒孵育,判讀結果與常規法相同。干卵膜片法還具有簡化操作規程,提高卵抗原的規範要求,並可長期保存等優點。
COPT可作為診斷血吸蟲病的血清學方法之一,及臨床治療病人的依據;可用作考核治療和防治效果的方法;並且用於血清流行病學調查及監測疫情的方法。
(四)間接血凝試驗
間接血凝試驗(indirect haemagglutination test,IHA)是以紅細胞作免疫配體的載體,並以紅細胞凝集讀數的血清學方法。最常用的紅細胞為綿羊或人(O型)紅細胞,來源方便。目前均用醛化紅細胞,可保存半年而不失其免疫吸附性能。
操作步驟如下:
1.紅細胞鞣化和致敏 ①取醛化紅細胞用0.15mol/L,pH7.2PBS離心洗滌2次,並用PBS配成2.5%懸液;②加等量1:2000鞣酸溶液(鞣酸不同批號,質量相差較大必須預試測定適宜濃度)37℃孵育20分鐘,經常搖動;③離心去上清,PBS洗1次,再用0.15mol/L,pH6.4PBS配成10%懸液;④每份懸液加等量適當稀釋的抗原液,置於37℃水浴箱中30分鐘(每5分鐘振動一次),離心去上清,pH7.2PBS洗2次,再用含1%正常兔血清(NRS)10%蔗糖緩衝液配成5%細胞懸液。加1‰疊氮鈉防腐,存4℃或減壓凍干備用,每批致敏細胞均需用已知陽性和陰性血清滴定靈敏度或特異性。陽性滴度在1:640以上,陰性血清不出現反應者可用。
2.微量血凝試驗 在U型(或V型)微量血凝板上,將被試血清用1%NRS或BSA生理鹽水作倍比系列稀釋,每孔含稀釋血清0.05ml。每孔加0.01ml致敏紅細胞懸液(可用標定過的OT針頭滴加),充分振蕩搖勻,加蓋於室溫靜置1~2小時讀取結果。
3.根據紅細胞在孔底的沉積類型而定。「-」,紅細胞沉於管底,呈圓點形,外周光滑;「±」,紅細胞沉於管底,周圍不光滑或中心有白色小點;「+」,紅細胞沉積範圍很小,呈較明顯的環形圈;「++」,紅細胞沉積範圍較小,其中可出現淡淡的環形圈;「+++」,紅細胞布滿管底呈毛玻璃狀;「++++」,紅細胞呈片狀凝集或邊緣捲曲。呈明顯陽性反應(+)的最高稀釋度為該血清的滴度或效價。
目前對血吸蟲病應用純化蟲卵抗原間接血凝試驗。採用經SephadexG-100柱層析純化的血吸蟲卵抗原致敏紅細胞作IHA,提高了方法的敏感性,特異性和重現性,為在疫區擴大應用提供了條件。
IHA操作簡便,敏感性高,適於現場使用,可作為輔助論斷病人,流行病學調查及綜合查病方法。先後在多種寄生蟲感染中應用,如血吸蟲,瘧疾、豬囊蟲,旋毛蟲,肺吸蟲,阿米巴,弓形蟲,肝吸蟲等。有些已製成商品診斷藥盒。不足之處是不能提供檢測抗體的亞型類別,和容易發生異常的非特異凝集。另外抗原的標準化,操作方法規範化急待解決,以提高其診斷效果和可比性。
(五)免疫熒光法
免疫熒光法(immunofluorescent method,IF)是借抗原抗體反應進行特異熒光染色的診斷技術。最常用的熒光素為異硫氰基熒光素(fluorescein isothiocynate,FITC)。常用於寄生蟲感染的熒光抗體染色有直接法與間接法。
1.直接法 用於檢測抗原,其缺點是每查一種抗原必須製備與其相應的熒游標記的抗體。目前很少應用。
2.間接法 也稱間接熒光抗體法(indirect fluorescent antibody method,IFA)。將抗原與未標記的特異性抗體(如患者血清)結合,然後使之與熒游標記的抗免疫球蛋白抗體(抗抗體)結合,三者的複合物可發出熒光。本法的優點是製備一種熒游標記的抗體,可以用於多種抗原,抗體系統的檢查,即可用以測定抗原,也可用來測定抗體。IFA的抗原可用蟲體或含蟲體的組織切片或塗片,經充分乾燥後低溫長期保存備用。一張載片可等距置放多個抗原位點用以同時檢測多個樣本或確定滴度。
IFA的操作步驟如下:①抗原標本:用記號筆或蠟筆將各個抗原位點圍圈隔離;②在每個抗原位置滴加已稀釋的血清樣本或樣本稀釋系列,使樣本液充滿圈內,置濕匣37℃孵育30分鐘;③用pH8.00.01mol/L PBS沖後再置同樣PBS液中浸泡5分鐘,不時搖動,如此2遍,然後取出吹乾;④在抗原位點滴加經pH8.0PBS適當稀釋的羊抗人IgG熒光抗體(每批結合物的工作濃度需經滴定),使完全覆蓋抗原膜,置濕盒37℃孵育30分鐘;⑤經洗滌(同③)後用0.1‰伊文思藍液復染10分鐘,然後以PBS流水沖洗0.5~1分鐘,風乾;⑥用pH8.5或pH8.0碳酸(或磷酸)緩衝甘油封片,也可加一小滴PBS(pH8.0)覆以蓋片鏡檢。鏡檢應及時進行以免疫光衰變。可使用熒光光源或輕便熒光光源,配以適合的激發濾片和吸收濾片,在低倍或高倍鏡下檢查。以見有符合被檢物形態結構的黃綠色清晰熒光發適合的激發濾片和吸收濾片,在低倍或高倍鏡下檢查。以見有符合被檢物形態結構的黃綠色清晰熒光發光體、而陰性對照不可見者為陽性反應。根據熒光亮度及被檢物形態輪廓的清晰度把反應強度按5級區別(+++,++,+,±,-)。+以上的熒光強度為陽性。
該法具有較高的敏感性、特異性和重現性,應用抗原經濟。國內外廣泛應用於寄生蟲病的血清學診斷方法,血清流行病學調查和監測疫情的方法,如主要用於診斷瘧疾、絲蟲病及血吸蟲病,也有用於肺吸蟲病、華支睾吸蟲病、包蟲病及弓形蟲病的血清學診斷。
近10年來,國內學者對IFA進行了很多改進。李允鶴等(1984,1988)通過深入研究,確定了感染鼠肝細胞內蟲卵冰凍切片為IFA較為理想的診斷抗原。該法需用熒光顯微鏡判斷結果,限制了它的應用範圍。但是應用該法時必須具備的熒光抗體,目前國內已有商品供應,這為IFA的擴大應用,提供了條件。
(六)對流免疫電泳試驗
對流免疫電泳試驗(counter-immunao electrophoretic assay,CIE)以瓊脂或瓊脂糖凝膠為基質的一種快速,敏感的電泳技術。
對流電泳較簡單的擴散法和常規免疫電泳法至少敏感10~20倍,省時,省料,可用已知抗原檢測抗體或相反,反應結果特異,陽性反應的可信度高,適用範圍廣。近年來本法的改進已試用酶或放射標記的反應配體,如酶標記抗原對流免疫電泳(ELACIE)、放射對流免疫電泳自顯影術(RCIEA)等。以克服電泳技術本身不夠靈敏的弱點,國內在血吸蟲病、肺吸蟲病免疫診斷已獲良好結果。國外報導應用於阿米巴病、錐蟲病、棘球蚴病、旋毛蚴病、血吸蟲病等血清學診斷。
(七)酶聯免疫吸附試驗
酶聯免疫吸附試驗(enzyme-linked immunosorbent assay.ELISA)簡稱酶聯試驗,已廣泛用於多種寄生蟲感染的宿主體液(血清,腦脊液等)以及排泄分泌物(尿,乳,糞便等)內特異抗體或抗原微粒的檢測。根據檢測要求,試驗可分多種類型,常用者有:用於檢測抗體的間接法;檢測IgM的雙夾心法;檢測抗原的雙抗體夾心法;以固相抗體檢測抗原的競爭法以及競爭抑製法等(圖21-8)。
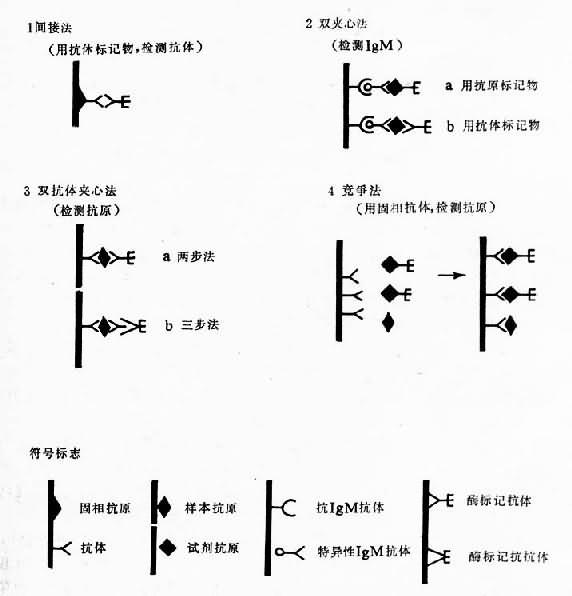
圖21-8 酶聯免疫吸附試驗常用方法示意圖
酶聯試驗的方法根據所用載體、酶底物系統、觀察反應結果等不同而有很大差別。目前最常用的固相載體為聚苯乙稀微量滴定板,具有需樣少,敏感,重演性好,使用方便等優點。酶底物系統也有多種,常用的有辣根過氧化物酶-鄰苯二胺(HRP-OPD)、鹼性磷酸酯酶-硝酚磷酸鹽(AKP-PNP)等,具有較好的生物放大效應。其中HRP由於價廉、易得而被廣泛應用。
酶聯試驗的基本操作過程可分為:①固相包被;②溫育洗滌;③加樣;④酶結合物反應;⑤底物顯色;⑥終止反應讀取結果等若干步驟。溫育和洗滌需貫穿在每二步驟之間,用以去除多餘的反應物。以下為臨床上最常用的間接法(檢測抗體)和雙抗體夾心法(檢測抗原)的操作程序:
⑴間接法:
1)以包被液(碳酸鈉-碳酸氫鈉緩衝液0.05mol/L,pH9.6)稀釋抗原(常用5~10µg/ml),每孔0.1(或0.2)ml包被反應板,37℃濕盒溫育2~3小時或4℃過夜;
2)棄去包被液,反應板用去離子水或PBS-Tween液(0.005mol/LPBS含0.05%Tween-20)沖洗3次,甩干;
3)用樣本稀釋液(0.05mol/L PBS含0.05%Tween-20)稀釋樣本(起始濃度≥100-1),用樣本稀釋液(每孔0.1(或0.2)ml,溫育1小時;
4)棄去樣液,如上沖洗,甩干加稀釋結合物(市售品常稀釋至100-1,用樣本稀釋液),每孔0.1(或0.2)ml,溫育1~2小時;
5)如上沖洗甩干後即刻加入新鮮配製的底物系統,每孔0.1(或0.2)ml,置暗盒室溫15分鐘;
6)終止反應:HRP-OPD系統每孔加1mol/LH2SO450µl;
⑵雙抗體夾心法:
1)以包被液稀釋抗體(如兔抗血吸蟲蟲卵可溶性抗原的抗體,抗SEA-IgG)包被反應板(1~1000µg/ml),方法同間接法包被抗原;
2)沖洗,甩干,加樣溫育同前(起始濃度≥5-1);
3)加結合物(例如抗SEA-IgG-HRP),適宜工作濃度需先經方陣滴定確定;
4)以下各步同間接法。
若包被抗體與第二抗體來自不同種的供體則可應用市售抗免疫球蛋白結合物。例如包被抗體為羊抗SEA,二抗用兔抗SEA則在未標記的二抗溫育洗滌後加羊抗兔IgG結合物(GAP-HRP)。
[附]酶標記物製備:應用抗原或抗體與酶分子的交聯技術,交聯物亦稱酶結合物(conjugate)。根據酶與抗體(抗原)的激活順序,交聯反應可分一步法、二步法及三步法不等。其中以二步法中的過碘酸鈉法多用,戊二醛一步法反應率較低,較適用於交聯AKP。免疫球蛋白標記辣根過氧化物酶(過碘酸鈉法)與免疫球蛋白標記鹼性磷酸脂酶(戊二醛一步法),按常規方法製備。
抗IgG型抗體酶結合物也可用金黃色葡萄球菌A-蛋白酶結合物替代,稱A-蛋白酶聯試驗(SPA-ELISA)。A-蛋白辣根過氧化物酶結合物(PA-HRP)已有市售標準品,其敏感度稍遜於抗體酶結合物。
底物配製:不同的酶要求選擇相應底物,以下為分別適用於比色和肉眼讀取結果的兩種HRP常用底物配製。
鄰苯二胺(OPD):經HRP催化後生成橘紅色產物。40mgOPD溶於檸檬酸磷酸緩衝液(pH5.0)100ml(含24.3ml 0.1mol/L檸檬酸,25.7ml0.02mol/LNa2HPO4加水50ml),臨用前加30%H2O20.15ml,溫育15分鐘後用2mol/l H2SO4終止反應,492nm讀數。本底物具高度敏感性,顯色梯度良好,生成可溶性產物,有利於比色讀數,但為光敏感,反應時應置暗盒內;也具致突變作用。
5-氨基水楊酸(5AS):經HRP催化生成棕色產物。8mg5AS溶於10ml50℃溫熱蒸餾水中,置4℃暗處不超過3天,臨用前以1nNaOH調pH至6.0,加0.05%H2O21ml。37℃經30~60分鐘溫浴後用1n NaOH終止反應,肉眼或449nm比色。本底物無致突變作用,生成棕褐色不全溶解的產物有利於肉眼判讀結果。
酶聯試驗為高靈敏檢測技術,結果可定量表示,可檢測抗體、抗原或特異性免疫複合物,微量滴定板法消耗樣本試劑少,能供全自動操作,適用批量樣本檢測,因此在寄生蟲感染的研究和診斷領域乃至血清流行病學均被廣泛應用。國內外有多種寄生蟲感染的酶聯藥籍出售,包括有血吸蟲病、弓形蟲病、阿米巴病、絲蟲病、蛔蟲病、旋毛蟲病和犬蛔蟲病等,ELISA可用作輔助診斷病人,血清流行病學調查和監測疫情的方法。酶聯試驗操作程序的簡單快速不如IHA,但方法具有很大所改良潛力和適應範圍。判斷結果需用分光光度計,限制了擴大應用;另外,應用抗原及酶結合物尚需進一步標準化,操作方法也應規範化。
近年來已有多種改進的酶聯免疫吸附試驗如①快速-ELISA:改進特點為用PVC薄膜代替聚苯乙烯微量反應板作載體;將1%可溶性血吸蟲卵抗原與尿素溶解性血吸蟲卵抗原等量相混合預吸附於薄膜上;用抗人IggMcAb代替羊抗人IgG製備酶結合物;用底物TMB代替OPD。該法主要以目視法判斷結果,整個操作流程僅需20min左右。②硫酸銨沉澱抗原-ELISA:可溶性血吸蟲卵抗原經飽和硫酸銨沉澱後用作ELISA診斷抗原;在系列實驗基礎上,使操作方法達到規範化;用質量控制圖控制檢測差異,並以標準曲線單位判斷結果;縮短檢測時間,節省檢測時間,節省試液用量,提高了敏感性,特異性和重現性。
(八)斑點ELISA
斑點ELISA(dot-ELISA)是近年新發展的一種ELISA技術,選用對蛋白質有很強吸附能力的硝酸纖維素薄膜作固相載體,底物經酶促反應後形成有色沉澱物使薄膜著色,然後目測或用光密度掃描儀定量。dot-ELISA可用來檢測抗體,也可用來檢測抗原,由於該法檢測抗原時操作較其他免疫學試驗簡便,故目前多用於抗原檢測。
操作方法將待檢血清作1:1~1:20稀釋,用微量加樣器將1µl血清點滴於硝酸纖維素膜(NC)上,置於70℃經1h,將NC浸於1%BSA-PBS中,室溫搖蕩1小時,洗滌2次,加1:1000稀釋的McAb酶標記物,室溫搖蕩2小時,洗滌3次後,加底物3,3'二氨基聯苯胺或4氯-1-乙萘酚,15分鐘後,流水終止反應,以目視法判斷結果。凡顯示棕色斑點者為陽性,否則為陰性。以產生棕色斑點反應的最高稀釋度為抗原滴度。
該法簡易,快速,適合於現場應用,有廣闊的應用前景。現有的資料初步證明具有診斷病人和考核治療效果,國內已用於血吸蟲病,瘧疾,絲蟲病,棘球蚴病的診斷。國內學者曾比較斑點ELISA和雙抗體夾心ELISA用於檢測班氏絲蟲病人循環抗原。採用相同的單株抗體和病人血清進行兩種方法對比試驗。結果顯示兩種方法檢測的特異性均大於95%,但是它們的敏感性有明顯不同,斑點ELISA能檢測出血清中0.055ng/ml微絲蚴抗原,而雙抗體夾心ELISA僅能測出≥10ng/ml抗原;並且前者不需要特殊的設備,適用於絲蟲病流行區。另有報告用單株抗體-抗原斑點試驗(McAb-AsT)檢測血清抗原診斷黑熱病,效果較為滿意,方法上進一步簡化,加樣以原濃度血清反應,效果最佳。國外還用於旋毛蟲病、絲蟲病、弓形蟲病以及肺孢子蟲病的血清學診斷方法。
(九)免疫酶染色試驗
免疫酶染色試驗(immunoenzymic staining test,IEST)是以含寄生蟲病原的組織切片,印片或培養物塗片用作抗原進行過氧化物酶特異免疫染色後在光鏡下檢示樣本中的特異性抗體。在蠕蟲和原蟲感染中均有多種應用。
操作過程抗原組織作冰凍(5~10µm)或石蠟連續切片(4~8µm)排列於載玻片,經丙酮固定貯存於-20℃備用。原蟲純培養亦可製成分隔塗片,方法均同熒光染色法抗原製片。試驗時先將抗原片在稀釋的過氧化氫溶液浸泡15分鐘,除去可能存在於組織中的內源性過氧化物酶;抗原片用PBS沖洗後經Tris緩衝液(PBS,pH7.6)10倍稀釋的正常兔或羊血清培育10分鐘,迅速以PBS洗滌後加檢測樣本(單個或系列稀釋度),置濕盒室溫(20~25℃)或37℃培育30分鐘;PBS洗滌3次,每次5分鐘,然後加兔或羊抗人過氧化物酶結合物(參照ELISA法),結合物中可加入所用抗原組織片供體動物血清約1/25~1/3體積,用以阻斷可能交叉反應,降低背景色度;抗原片以PBS洗滌3次後加聯苯胺(DAB)底物溶液(飽和聯苯胺液加等量pH7.6硼酸緩衝液,用前按9:1體積加入0.1%H2O2液),室溫顯色10~15分鐘後在光鏡下觀察反應結果。
反應標準:「-」,組織內抗原部位不呈現棕紅色;「+」,組織內抗原部位(如血吸蟲肝卵切片中的蟲卵)呈現棕紅色;「++」,局部呈現清晰的棕紅色;「+++」,呈現非常清晰的棕紅色。
該法簡單,節省抗原;判斷結果不需要特殊儀器;適合於現場應用。IEST可用作輔助診斷病人,考核療效,血清流行病學調查及監測疫情的方法。目前主要應用於血吸蟲病、絲蟲病及囊蟲病診斷,也可用來診斷華支囊吸蟲病、肺吸蟲病、包蟲病和弓形蟲病。
目前對該方法改進有:①用感染鼠肝組織內蟲卵製成7µm厚度冰凍切片(或石蠟切片)作為診斷用固相抗原代替可溶性血吸蟲卵抗原作IEST,具有取材容易和應用抗原經濟的優點。②將冰凍切片置於載玻片上,可以反覆使用載玻片,較一次性用的PVC薄膜/苯氯乙烯反應板價廉,顯著地降低了檢測費用。③判斷結果時,應用普通光鏡即可。染色標本不必即時檢查。可保存很長時間,便於複查。④陽性血清作最高滴度,可定量抗體水平,用作考核療效有及防治效果的指標。⑤IEST的反應基本原理與COPT相似,但前者應用切片蟲卵代替了COPT的整個干卵,前法的反應快速(約1.5~2小時)而後法較緩慢(需48~72小時)。為此,IEST彌補了COPT診斷時,漏檢病人和取得結果不快速的缺陷。病鼠肝組織內蟲卵冰凍切片抗原IEST,目前已在疫區擴大應用。現已研製成試劑盒,批量生產,供應現場需用。
(十)免疫印漬試驗
免疫印漬試驗(immunoblot或Western blot)是由十二烷基硫酸鈉聚丙烯醯胺凝膠電泳(SDS-PAGE),電泳轉印及標記免疫試驗三項技術結合而成的一種新型的免疫探針技術(immuno-probing technique),是用於分析蛋白抗原和鑒別生物學活性抗原組分的有效方法,近年已應用於檢測寄生蟲感染宿主體液內針對某分子量抗原的相應循環抗體成分或譜型。是為一項高敏感和高特異的診斷方法,具有很大發展潛力。用於診斷的免疫印漬試驗以採用酶標記的探針(即二抗及其標記結合物)為安全方便,稱酶免疫轉移印漬試驗(enzyme immuno-transfer blotting,EITB)。
1.操作程序(以血吸蟲EITB為例)
⑴樣本分離:
1)取日本血吸蟲新鮮成蟲按5~10對/1.5ml比例加樣本緩衝液,勻漿,置沸水浴2分鐘,離心(10000g,30分鐘),取上清液備用。
2)上述成蟲抗原樣本進行單梳SDS-PAGE電泳分離。左側梳孔加標準分子量蛋白,梳孔右側樣槽加抗原液,電壓控制在160~180V之間。
⑵電泳轉印:
1)從電泳板中取出已完成電泳的凝膠片浸泡於盛有轉印緩衝液(TB)的搪瓷盤 內。
2)在TB液內組成轉印夾心板層:取相應大小的硝酸纖維(NC)薄膜,徐徐浸泡在TB液,將凝膠片與薄膜光面緊貼。兩面各放置浸濕濾紙兩層而後海綿墊(厚0.5~1cm)一層,做好方位標記,最後夾於二層有孔塑料襯板之間,絕對避免各層之間留有氣泡。
3)將TB倒入轉印槽中,然後插入轉印板,使凝膠片位於陰極側,NC薄膜位於陽極側。
4)置轉印槽於4℃冰箱內,通電轉印數小時或過夜,電流控制在250mA上下(約40~50V)。
⑶探針檢測:
1)取出轉印好的NC薄膜,水平地放入猝滅劑中,室溫搖動1小時以封閉未吸附蛋白質的區域,然後用洗滌緩衝液選2~3次,每次30分鐘以除去亦性劑,使蛋白質的天然狀態和生物學特性得以恢復。
2)平置NC薄膜於浸有Tris-緩衝鹽水(TBS)的濾紙上,用刀片將薄膜按電泳方向分割為寬約0.5cm的直條,用鉛筆做好上端標記。
3)取其中一個細條,並同標準蛋白條帶一起作氨基黑染色(也可用考馬斯亮藍染或銀染)測試分離效果並確定分子量位置。其餘細條晾乾後置4℃作印漬試驗備用(抗原活性可保持3個月以上)。
⑷印漬試驗:
1)置上述抗原條於分格反應板的反應槽內,正面向上,每槽一條,預先用0.05%TBS-Tween液浸濕(TBS-T);
2)被檢血清用TBS-T液稀釋(常用1:150),加入反應槽中,以浸沒膜條為限。通常需0.5~1.5ml,相當於10µl血樣量(每槽加液量下同);
3)室溫(20~25℃)振蕩60分鐘,以後用TBS-T洗6次,每次3分鐘;
4)加已稀釋的羊抗人酶結合物,溫育1.5小時,洗滌如上;
5)加入新鮮配製的底物溶液(TBS50ml+0.3%萘酚甲醇液3ml+30%H2O210µl;或二氨基聯苯胺,DAB,5mg/ml 0.05mol/L檸檬酸磷酸緩衝液,pH5.0,每60ml加3%H2O220ul和1%COCl20.2ul 和1%COC120.6ml);
6)15分鐘後用蒸餾水沖洗數次以終止反應,薄膜條取出置玻板自然乾燥;
7)陽性反應可見藍黑色(4氯1萘酚底物)或棕褐色(DAB)條帶。
2.主要試劑
⑴樣本緩衝液:含甘油10ml,2-巰基乙醇5ml,10%SDS30ml。
⑵轉印緩衝液(TB):Tris 3g,甘氨酸14g,甲醇250ml,水加至1000ml。
⑶Tris緩衝鹽水(TBS):10mmol/L,Tris含0.9%NaCl,用1N HC1調pH至7.4。
⑷TBS-T液:TBS液內含0.05%Tween-20於TBS液。
⑸猝滅劑:1%~5%BSA或0.1%~0.3%Tween-20於TBS液。
⑹氨基黑染液:0.1%W/V氨基黑(C. I. 20470),45%V/V甲醇,10%V/V冰醋酸。
脫色液:90%V/V甲醇,2%冰醋酸。
EITB用作鑒定寄生蟲抗原的特定組分蛋白及診斷寄生蟲病的方法。在國外已成功地用於愛滋病的常規診斷,並且在瘧原蟲、弓形蟲、血吸蟲、肺吸蟲、包蟲等的研究分析方面有很多報導。國內用於檢測包蟲病患者血清抗體也獲良好結果,初步應用於血吸蟲感染現場調查,用上述抗原及操作程序可檢示特異的抗腸相關31/32kD診斷蛋白抗體的條帶,呈現特異和敏感的特性。用本法對感染宿主不同病期抗體譜型的研究,可望獲得有效化療後早期隱退的特異條帶。批量製備抗原分離的薄膜條帶,有可能成為適用於現場查病的特異性診斷藥盒,不鐵為一項具有診斷潛能的新技術。
(十一)雜交瘤技術製備單株抗體
經十多年的研究,單株抗體(McAb)廣泛用於寄生蟲病臨床與實驗研究。如寄生蟲蟲種與蟲株的分型和鑒定;建立以檢測循環抗原為主的免疫診斷方法;分析和純化抗原製備靶抗原;以及寄生蟲感染免疫,保護性免疫和蟲苗製備等方面,目前,國內外有報告,McAb用於瘧疾、弓形蟲病、血吸蟲病、肺吸蟲病、棘球蚴病、絲蟲病等方面。有關McAb在瘧疾中的應用,如對蟲種,蟲株的鑒定與分型,通過採用McAb對環孢蛋白(circumsporozoite protein,CSP)抗原及裂殖體糖蛋白研究,為瘧原蟲分型鑒定提供了新的依據;單株抗體的應用又為提高臨床免疫診斷價值提供了極好的工具,近年來,國內已有報告採用McAb雙夾心斑點金銀染色法和雙夾心斑點酶聯免疫吸附試驗以檢測瘧原蟲循環抗原,陽性率分別達90%~93.3%和85%~86.7%,具有較高的特異性和重複性,另外發現某些抗子孢子、裂殖體(子)和配子體的單株抗體具有保護作用。保護性McAb的發現不僅為製備蟲苗的靶抗原提供了條件,而且為進行被動免疫開闢了途徑。
在血吸蟲病方面,單株抗體已應用於血吸蟲抗原分析,免疫學診斷和保護性免疫研究,國內外均已報導採用檢測血吸蟲循環抗原,如Sj23,Sm38,Sj70等抗原,其陽性率在90%~97%,交叉反應低且有良好的療效考核價值,有關保護性免疫研究方面,主要集中在分子量分別為28kD和38kD的抗原,現有資料初步表明以McAb提純的28kD抗原免疫大白鼠後,可獲得70%的保護率。
在絲蟲病方面,應用雜交瘤技術已製備出識別馬來微絲蚴表面分子量分別為70kD、75kD、110kD等抗原的McAb,某些McAb能介導巨噬細胞粘附於微絲蚴表面,引起蟲體死亡。將這些McAb被動轉移給受體動物,在體內能降低微絲蚴血症。
(十二)DNA探針技術
DNA技術(probe)技術,又稱核酸分子雜交(molecular hybridization)技術,最近幾年迅速發展起來的一種敏感性高,特異性強,應用面廣的研究手段。在寄生蟲病診斷中,探針是病原體的特異核酸序列,可用來檢測出病原體是否存在,其關鍵環節在於獲得特異的核酸探針。近10年來應用特異的核酸探針鑒定寄生蟲和診斷寄生蟲病的研究報導較多,現有資料表明,DNA探針檢測,其特異性和敏感性高;並且DNA探針是直接檢測寄生蟲的基因,故比血清學方法可靠;又因探針DNA較穩定,在合適條件下可較長期保存;在試驗條件不變時試驗結果的重演性較好。在寄生蟲病的診斷、現場調查、寄生蟲種的鑒定及分類等方面的研究中均已使用了DNA探針技術,內容包括原蟲、吸蟲、線蟲、絛蟲、昆蟲的鑒定和致病的診斷。另外,核酸探針已成功地用於許多傳播媒介體內寄生蟲的鑒定。但是一般尚在實驗階段。可望能用作高效和準確的寄生蟲病血清學方法,用以製備經濟和理想的診斷抗原。
(十三)PCR技術
檢測病原體遺傳物質用以診斷寄生蟲病的方法,除分子雜交技術外,新近發展的更靈敏、快速,並且不需要同位素標記的基因擴增技術,如聚合酶鏈反應(polymerase chain reaction,PCR)是一種體外擴增特異性DNA技術。
現已使用PCR技術於寄生蟲病診斷,如錐蟲病、利什曼病、肺孢子蟲病、腸球蟲病、賈第蟲病、弓形蟲病等,在一些疾病中,有時原蟲數量極少,用一般方法無法檢測,經用PCR擴增DNA模板,提供了一條解決診斷的途徑。如在檢測錐蟲時,PCR擴增純化DNA可使探針檢測到血樣中1個蟲體;國內建立了弓形蟲病PCR診斷方法,具有高度特異、敏感且快速的優點。今後在寄生蟲學領域中將會更廣泛深入地開展PCR技術的應用。
| 關於「寄生蟲學/寄生蟲學實驗診斷技術」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |