高碘酸
| A+醫學百科 >> 高碘酸 |
中文名稱: 高碘酸
英文名稱: periodic acid
CAS No.: 10450-60-9
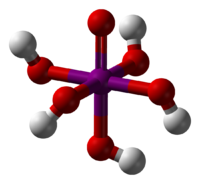
分子式: HIO4.2H2O 碘
分子量: 227.94
理化特性
主要成分: 純品
外觀與性狀: 無色或白色結晶,無臭。有潮解性。
熔點(℃): 122
沸點(℃): 140(分解)
相對蒸氣密度(空氣=1): 7.9
主要用途: 用作氧化劑。
需要注意一點的是,雖然碘和溴、氯都屬於鹵族元素,而且高溴酸(HBrO4)、高氯酸(HCLO4)都是強酸,但高碘酸是弱酸。
製備方法
偏高碘酸也可以由五氧化二碘、氧氣和水在加熱條件下化合製得:I2O5+ H2O+O2====2HIO4(反應會放出大量的熱,所以只需要一開始加熱就行了,之後反應所需的熱量完全能有之前反應放出的熱提供)。
性質
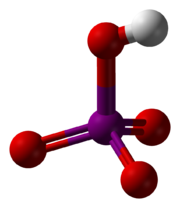
正高碘酸脫水得到偏高碘酸HIO4,進一步脫水則生成七氧化二碘(無色粘稠液體),七氧化二碘分解得到五氧化二碘(I2O5)和氧氣。
純淨的偏高碘酸不存在。偏高碘酸水溶液的最高濃度為86%。偏高碘酸是無機酸中氧化性最強的,能將金屬錳氧化為七氧化二錳或高錳酸。並且酸性只比高氯酸和不穩定的氫砹酸弱,比硫酸還強。在無機酸中酸性排第三。
86%偏高碘酸如果和有機物接觸,先會使其脫水碳化,之後甚至會著起火來。偏高碘酸為難揮發性酸。如皮膚上佔到偏高碘酸,應先用清水沖洗,再有硼酸二氫鈉溶液中和。必要時需到醫院就醫。
正高碘酸和偏高碘酸可分別生成鹽類,稱為「正高碘酸鹽」及「偏高碘酸鹽」。偏高碘酸鹽的溶解度和化學性質與同族鹵素的高氯酸鹽類似,但陰離子半徑更大,氧化性較弱,不過酸性條件下氧化性極強,和偏高碘酸類似。。
有機化學中,高碘酸可氧化偕二醇並使碳-碳鍵斷裂,生成兩個醛,用於確定糖類的結構。
注意事項
健康危害: 具有強烈刺激和腐蝕性。皮膚和眼接觸有強烈刺激性或造成灼傷。口服引起口腔及消化道灼傷。
燃爆危險: 本品助燃,具強腐蝕性、強刺激性,可致人體灼傷。
危險特性: 無機氧化劑。遇易燃物、有機物會引起爆炸。受熱分解,放出氧氣。
| 關於「高碘酸」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |