鎂
| A+醫學百科 >> 鎂 |
元素名稱:鎂(měi)
元素類型:金屬
相對原子質量:24.3050(6)
發現者:戴維
發現年代:1808年
化學式:Mg
核內質子數:12
核外電子數:12
核電荷數:12
電子層數:3
原子體積:(立方厘米/摩爾)
13.97
元素在太陽中的含量:(ppm)
700
元素在海水中的含量:(ppm)
1200
地殼中含量:(ppm)
23000
電負性:1.31
氧化態:
Main
Mg+2
Other
電離能 (kJ/ mol)
M - M+ 737.7
M+ - M2+ 1450.7
M2+ - M3+ 7732.6
M3+ - M4+ 10540
M4+ - M5+ 13630
M5+ - M6+ 17995
M6+ - M7+ 21703
M7+ - M8+ 25656
M8+ - M9+ 31642
M9+ - M10+ 35461
外圍電子排布:3s2 核外電子排布: 2,8,2
晶體結構:晶胞為六方晶胞.。
晶胞參數:
a = 320.94 pm
b = 320.94 pm
c = 521.08 pm
α = 90°
β = 90°
γ = 120°
莫氏硬度:2.5
同位素及放射線: Mg-24 Mg-25 Mg-26 Mg-27[9.45m] Mg-28[21h]
電子親合和能: -21 KJ.mol-1
第一電離能:738 KJ.mol-1 第二電離能:1451 KJ.mol-1 第三電離能:7733 KJ.mol-1
單質密度:1.738 g/cm3 單質熔點:650.0 ℃ 單質沸點:1170.0 ℃
原子半徑:1.72 埃 離子半徑:0.66(+2) 埃 共價半徑:1.36 埃
熱導率: W/(m.K)
156
目錄 |
發現過程
1808年,英國的戴維,用鉀還原白鎂氧(即氧化鎂MgO),最早製得少量的鎂。
物理性質:銀白色的金屬,密度1.738克/厘米3,熔點648.9℃。沸點1090℃。化合價+2,電離能7.646電子伏特,是輕金屬之一,具有延展性,金屬鎂無磁性,且有良好的熱消散性。
化學性質
具有比較強的還原性,能與熱水反應放出氫氣,燃燒時能產生眩目的白光,鎂與氟化物、氫氟酸和鉻酸不發生作用,也不受苛性鹼侵蝕,但極易溶解於有機和無機酸中,鎂能直接與氮、硫和鹵素等化合,包括烴、醛、醇、酚、胺、脂和大多數油類在內的有機化學藥品與鎂僅僅輕微地或者根本不起作用。鎂能在能和二氧化碳發生燃燒反應,因此鎂燃燒不能用二氧化碳滅火器滅火。
1.與非金屬單質的反應: 2Mg+O2=2MgO 3Mg+N2=Mg3N2 (點燃)
2.與水的反應: Mg+2H2O=Mg(OH)2+H2↑(加熱)
3.與酸的反應:Mg+2HCl=MgCl2+H2 ↑ Mg+H2SO4=MgSO4+H2 ↑
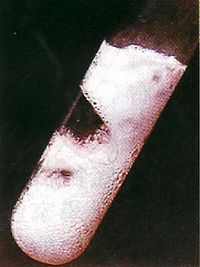
4.與氧化物的反應:2Mg+CO2=2MgO+C(點燃)
5.與空氣反應:2Mg+O2=2MgO(點燃)
- 2Mg+CO2=2MgO+C(點燃)
3Mg+N2=Mg3N2(點燃)
- 註:該反應在氧氣充足時一般不發生或發生後又有 C+O2=CO2(點燃),因為在反應後不見有黑色固體生成。
工業製法
鎂存在於菱鎂礦(碳酸鎂)MgCO3、白雲石(碳酸鎂鈣)CaMg(CO3)2、光鹵石(水合氯化鎂鉀)KCl.MgCl2.H2O中。工業上利用電解熔融氯化鎂或在電爐中用硅鐵等使其還原而製得金屬鎂,前者叫做熔鹽電解法,後者叫做硅熱還原法。氯化鎂可以從海水中提取,每立方英里水含有約120億磅鎂。
Mg在海水中的提取
① CaCO3(s)= (高溫)CaO(s)+CO2(g)↑
CaO(s)+H2O(l)=Ca(OH)2(s)
② Ca(OH)2(aq)+MgCl2(aq)=Mg(OH)2(s)↓+CaCl2(aq)
③ Mg(OH)2(s)+2HCl(l)+6H2O(l)=MgCl2.6H2O(s)+2H2O(l)
④ MgCl2.6H2O(s)=(HCl) MgCl2(s) +6H2O(l)
⑤ MgCl2(l)==通電== Mg(s)+Cl2(g)↑
元素用途
常用做還原劑,去置換鈦、鋯、鈾、鈹等金屬。主要用於製造輕金屬合金、球墨鑄鐵、科學儀器脫硫劑脫氫和格氏試劑,也能用於制煙火、閃光粉、鎂鹽等。結構特性類似於鋁,具有輕金屬的各種用途,可作為飛機、導彈的合金材料。但是鎂在汽油燃點可燃,這限制了它的應用。
日常用途:體操運動員常塗鎂粉來增加摩擦力. (是MgCO3)
醫療用途:治療缺鎂和痙攣。
體育用途:在緊張運動幾小時前注射,或在緊張運動後注射以彌補鎂的流失。
金屬鎂能與大多數非金屬和酸反應;在高壓下能與氫直接合成氫化鎂;鎂能與鹵化烴或鹵化芳烴作用合成格利雅試劑,廣泛應用於有機合成。鎂具有生成配位化合物的明顯傾向。
鎂是航空工業的重要材料,鎂合金用於製造飛機機身、發動機零件等;鎂還用來製造照相和光學儀器等;鎂及其合金的非結構應用也很廣;鎂作為一種強還原劑,還用於鈦、鋯、鈹、鈾和鉿的生產中。
純鎂的強度小,但鎂合金是良好的輕型結構材料,廣泛用於空間技術、航空、汽車和儀錶等工業部門。一架超音速飛機約有5%的鎂合金構件,一枚導彈一般消耗100~200公斤鎂合金。鎂是其他合金(特別是鋁合金)的主要組元,它與其他元素配合能使鋁合金熱處理強化;球墨鑄鐵用鎂作球化劑;而有些金屬(如鈦和鋯)生產又用鎂作還原劑;鎂是燃燒彈彈和照明彈不能缺少的組成物;鎂粉是節日煙花必需的原料;鎂是核工業上的結構材料或包裝材料;鎂肥能促使植物對磷的吸收利用,缺鎂植物則生長趨於停滯。鎂在人民生活中佔有重要地位的一種基礎材料。
鎂在其他方面的應用
鎂是最輕的結構金屬材料之一,又具有比強度和比剛度高、阻尼性和切削性好、易於回收等優點。國內外將鎂合金應用於汽車行業,以減重、節能、降低污染,改善環境。發達國家汽車百公里耗油最終將實現3L目標,歐洲汽車用鎂占鎂總消耗量的14%,預計今後將以15-20%的速度遞增,2005年將達到20萬噸。我國東風、長安等汽車已開始用鎂合金,不久、重慶,成都等地將成為我國汽車用鎂合金研究與開發應用生產基地。
與塑料相比,鎂合金具有重量輕、比強度高、減振性好、熱疲勞性能好、不易老化,又有良好的導熱性、電磁屏蔽能力強、非常好的壓鑄工藝性能,尤其易於回收等優點,是替代鋼鐵、鋁合金和工程塑
料的新一代高性能結構材料。為適應電子、通訊器件高度集成化和輕薄小型化的發展趨勢,鎂合金是交通、電子信息、通訊、計算機、聲像器材、手提工具、電機、林業、紡織、核動力裝置等產品外殼的理想材料。發達國家非常重視鎂合金開發與應用,尤其在汽車零部件、筆記本電腦等便攜電子產品的應用,每年以20%的速度增長,非常引人注目,發展趨勢驚人。我國青島作為家電城,先後投資2.1億及3.5億人民幣,生產製造手機外殼、數碼相機、手提電腦、掌上電腦外殼,高級視聽器材外殼等產品,年產1600萬件鑄件產品,第一個鎂合金開發應用產業化基地將落戶青島。
金屬鎂是鋁合金中的主要合金元素,世界年需求量在15萬噸左右,2000年我國鋁合金生產290萬噸,用鎂作合金元素,每年約需1.01萬噸。
隨著汽車工業、石油、天然氣管線、海洋鑽井平台,橋樑建築等領域用高強度低硫鋼的需求不斷增加,近幾年,我國鞍鋼、寶鋼、武鋼、本鋼、包鋼、攀鋼、首鋼等鋼廠已經用鎂粉深脫硫,獲得優質鋼,取得良好效果。鎂粉用於鋼鐵脫硫具有潛在市場。此外,鎂粉還用於製造化工產品、藥品、煙火、信號、照明彈等材料、金屬還原劑、油漆塗料、焊絲以及供球墨鑄鐵用球化劑等。
鎂犧牲陽極作為有效的防止金屬腐蝕的方法之一,可廣泛用在地下鐵制管道、石油管道、儲罐、海上設施、裝備、民用等。
現代戰爭需要軍隊具有遠程快速部署運動的能力,要求武器裝備輕量化,在手持式武器、裝甲戰車、運輸車、航空制導武器上將大量採用輕金屬材料。輕量化是提高武器裝備作戰性能的重要方向。鎂所具有的輕質特性決定了鎂合金是生產航天器、軍用飛機、導彈、高機動性能戰車、船舶的必不可少的結構材料,因此,大力開發鎂合金應
用範圍是國防現代化的需要。
哪些食物富含鎂?
據測定:紫菜含鎂量最高,每100克紫菜中含鎂460毫克,居各種食物之冠,被喻為「鎂元素的寶庫」。其餘含鎂食物有:穀類如小米、玉米、蕎麥面、高粱面,燕麥,通心粉,烤馬鈴薯;豆類如黃豆、黑豆、蠶豆、豌豆、豇豆、豆腐;蔬菜如冬菜、莧菜、辣椒、蘑菇;水果如楊桃、桂圓、核桃仁;其他如蝦米、花生、芝麻,海產品等。鎂有助於調節人的心臟活動,降低血壓,預防心臟病,提高男士的生育能力。建議男士早餐應吃2碗牛奶燕麥粥和一隻香蕉。
建議攝取量:中國營養學會建議,成年男性每天約需鎂350毫克,成年女性約為300毫克,孕婦以及餵奶期女性約為450毫克(每星期可吃2~3次花生,每次~8粒便能滿足對鎂的需求量)。
鎂是哺乳動物和人類所必需的微量元素,它是細胞內重要的陽離子,參與蛋白質的合成和肌肉的收縮作用。
鎂缺乏在臨床上主要表現為情緒不安、易激動、手足抽搐、反射亢進等,正常情況下,由於腎的調節作用,口服過量的鎂一般不會發生鎂中毒。當腎功能不全時,大量口服鎂可引起鎂中毒,表現為腹痛、腹瀉、嘔吐、煩渴、疲乏無力,嚴重者出現呼吸困難、紫紺、瞳孔散大等。
鎂廣泛分布於植物中,肌肉和臟器中較多,乳製品中較少。動物性食品中鎂的利用率較高,達30%~40%,植物性食品中鎂的利用率較低。鎂的需要量2~3歲為150毫克,3~6歲為200毫克
抽筋」多吃含鎂食物
很多人容易在夜裡睡眠時發生腿部「抽筋」,這在醫學上稱作「抽搐病」,尤以夜裡受涼為甚。不少人將其歸咎於缺鈣,但從人體對礦物質及微量元素的需求來說,缺鎂時也會發生這種癥狀。
鎂在人體運動功能活動中扮演著十分重要的角色。人之所以活著,全靠人體內一系列複雜的生物化學反應維持著生命活動,而催化這些生化反應則需要上千種促酶(生物催化劑)。國外科學家研究發現,鎂可激活325個酶系統,把鎂稱為生命活動的激活劑是當之無愧的。近年來,國外科學家研究指出,人到中年以後要 「鎂」食。即要多食含鎂豐富的食物。心血管疾病,如冠心病、高血壓、高血脂、心肌梗塞、糖尿病等多在人到中年之後發生,這與體內鎂含量降低有關。
鎂是人體中僅次於鉀的細胞內正離子,它參與體內一系列新陳代謝過程,包括骨及細胞的形成,與神經肌肉和心臟功能有密切關係。一般成年人每日對鎂的需求量,男性為350毫克,女性為300毫克,如果缺鎂,可導致肌肉無力,耐久力降低。由於運動,特別是長時間高強度運動大量消耗體內的鎂,從而降低肌肉的活動功能,甚至還會發生抽搐、痙攣等。
專家認為,在正常攝入食物的情況下,一般不存在缺鎂和補鎂的問題。若出現缺鎂癥狀時,應多選用含鎂豐富的食物:穀類、豆類、綠色蔬菜、蛋黃、牛肉、豬肉、河鮮產品、花生、芝麻、香蕉等。豆腐中也含有較高的鎂成分,經常吃些鹵水豆腐,可解決由於缺鎂引起的「抽搐病」。
相關信息
鎂是在自然界中分布最廣的十個元素之一,但由於它不易從化合物中還原成單質狀態,所以遲遲未被發現。
長時期里,化學家們將從含碳酸鎂的菱鎂礦焙燒獲得的鎂的氧化物苦土當作是不可再分割的物質。在1789年拉瓦錫發表的元素表中就列有它。1808年,戴維在成功製得鈣以後,使用同樣的辦法又成功的製得了金屬鎂。從此鎂被確定為元素,並被命名為magnesium,元素符號是Mg。Magnesium來自希臘城市美格里西亞Magnesia,因為在這個城市附近出產氧化鎂,被稱為magnesia alba,即白色氧化鎂。不過鎂的名稱magnesium很容易和錳的名字manganum混淆,雖然有人提出更改,卻一直沿用下來。
鎂是一種參與生物體正常生命活動及新陳代謝過程必不可少的元素。鎂影響細胞的多種生物功能:影響鉀離子和鈣離子的轉運,調控信號的傳遞,參與能量代謝、蛋白質和核酸的合成;可以通過絡合負電荷基團,尤其核苷酸中的磷酸基團來發揮維持物質的結構和功能;催化酶的激活和抑制及對細胞周期、細胞增殖及細胞分化的調控;鎂還參與維持基因組的穩定性,並且還與機體氧化應激和腫瘤發生有關。
鎂的吸收代謝:成人身體總鎂含量約25g,其中60%~65%存在於骨、齒,27%分布於軟組織。食物中的鎂在整個腸道均可被吸收,但主要是在空腸末端與迴腸部位吸收,吸收率一般約為30%。膳食中促進鎂吸收的成分主要有氨基酸、乳糖等;抑制鎂吸收的主要成分有過多的磷、草酸、植酸和膳食纖維等。成人從膳食中攝入的鎂大量從膽汁、胰液和腸液分泌到腸道,其中60%~70%隨糞便排出,部分從汗和脫落的皮膚細胞丟失。
鎂離子是生物機體中含量較多的一種正離子,其量在整體中僅次於鈣、鈉、鉀而居第四位;鎂離子在細胞內的含量則僅次於鉀離子而居第二位。整粒的種子、未經碾磨的穀物、青葉蔬菜、豆類和堅果是日糧鎂最為豐富的來源;魚、肉、奶和水果中鎂含量較低;經過加工的食物,在加工過程中鎂幾乎全部損失。肌酸六磷酸、粗纖維、乙醇、過量的磷酸鹽和鈣離子削弱了鎂的吸收,這可能是因為降低了內腔鎂的濃度。
鎂可以有效促進鈣的吸收.在細胞中有一個特殊的鈣的通路,其形成的主要元素是鎂.所以人體缺鎂會影響鈣的代謝.
鎂缺乏症
鎂的簡介
鎂是人體細胞內的主要陽離子,濃集於腺粒體中,僅次於鉀和磷,在細胞外液僅次於鈉和鈣居第三位,是體內多種細胞基本生化反應的必需物質。鎂的原子序為12,原子量為24.3,是典型的二價金屬,具有金屬的共有特性。由於鎂的氧化物性質與鈣一樣介於「鹼性」和「土性」之間,故稱為鹼金屬元素。正常成人身體總鎂含量約25g,其中60%-65%存在於骨、齒,27%分布於軟組織。鎂主要分布於細胞內,細胞外液的鎂不超過1%。在鈣、維生素C、磷、鈉、鉀等的代謝上,鎂是必要的物質,在神經肌肉的機能正常運作、血糖轉化等過程中扮演著重要角色。
鎂的發現
許多世紀以前,古羅馬人認為「magnesia」(希臘Magnesia地區出產的一種白色鎂鹽,鎂元素即因此得名)能治療多種疾病。直到1808年,英國化學家戴維採用電解苦土(含鎂)的方法分離出元素鎂。上世界30年代初MoCollum,E.V及其同事首次用鼠和狗作為實驗動物,系統地觀察了鎂缺乏的反應。1934年首次發表了少數人在不同疾病的基礎上發生鎂缺乏的臨床報道。證實鎂是人體的必需元素。Flink及其同事在上世紀50年代初曾報告因酗酒和接受無鎂靜脈輸液而發生鎂耗竭的病例。健康人一般不會發生鎂缺乏,但已發現越來越多的臨床疾病與鎂耗竭有關。
食物來源
鎂普遍存在於食物中,由於葉綠素是鎂卟啉的鰲合物,所以綠葉蔬菜是富含鎂的。食物中諸如糙糧、堅果也含有豐富的鎂,而肉類、澱粉類食物及牛奶中的鎂含量屬中等。除了食物之外,從飲水中也可以獲得少量鎂。但飲水中鎂的含量差異很大。如硬水中含有較高的鎂鹽,軟水中含量相對較低。
代謝吸收
食物中的鎂在整個腸道均可被吸收,但主要是在空腸末端與迴腸部位吸收,吸收率一般約為30%。可通過被動擴散和耗能的主動吸收兩種機制吸收。健康成人從食物中攝入的鎂大量從膽汁、胰液和腸液分泌到腸道,其中60%-70%隨糞便排出,部分從汗和脫落的皮膚細胞丟失,其餘從尿中排出,每天約排出50-120mg,約佔攝入量的1/3~1/2。
生理功能
1.激活多種酶的活性 鎂作為多種酶的激活劑,參與300多餘種酶促反應。
2.抑制鉀、鈣通道。
需要人群
酒精中毒的人通常有缺鎂的現象,常喝酒、喝濃茶和喝濃咖啡的人最好多攝取鎂。
生理需要
成人的適宜攝入量(AI)定為350mg/d,可耐受最高攝入量(UL)定為700mg/d。
缺乏表現
鎂缺乏可致血清鈣下降,神經肌肉興奮性亢進;對血管功能可能有潛在的影響,有人報告低鎂血症患者可有房室性早搏、房顫以及室速與室顫,半數有血壓升高;鎂對骨礦物質的內穩態有重要作用,鎂缺乏可能是絕經後骨質疏鬆症的一種危險因素;少數研究表明鎂耗竭可以導致胰島素抵抗。
治療措施
輕度缺鎂時,可由飲食或口服補充鎂劑,可給予氧化鎂或用氫氧化鎂,為避免腹瀉可與氫氧化鋁膠聯用。口服不能耐受或不能吸收時,可採用肌肉注射鎂劑,一般採用20%~50%硫酸鎂。
若低鎂血症嚴重,出現手足搐搦、痙攣發作或心律失常等,應給予靜脈注射。靜脈給鎂時需注意急性鎂中毒的發生,以免引起心搏驟停。故避免給鎂過多、過速,如遇鎂中毒,應給注射葡萄糖酸鈣或氯化鈣對抗之。
過量表現
過量鎂攝入,血清鎂在1.5-2.5mmol/L時,常伴有噁心、胃腸痙攣等胃腸道反應;當血清鎂增高到2.5-3.5mmol/L時則出現嗜睡、肌無力、膝腱反射弱、肌麻痹;但血清鎂增至5mmol/L時,深腱反射消失;血清鎂超過5mmol/L時可發生隨意肌或呼吸肌麻痹;血清鎂7.5mmol/L或更高時可以發生心臟完全傳導阻滯或心搏停止。
高鎂血症可引起低血鈣,其部分機制可能是由於甲狀旁腺素分泌降低或靶器官對激素的反應性降低。高鎂血症可影響骨和血液凝固。在尿毒症時,骨中鎂含量顯著增高。更重要的是鎂過多可致骨異常。鎂過多可干擾血小板粘附和凝血酶原生成時間。尿毒症時凝血障礙部分原因可能是由於慢性高鎂血症所致。
治療措施
鈣和鎂之間有顯著拮抗作用,可先從靜脈輸給10%葡萄糖酸鈣10%氯化鈣,以對抗鎂對心臟和肌肉的抑制,同時要積極糾正酸中毒和缺水。如血清鎂仍無下降或癥狀不減輕時,應及早採用腹膜透析或血液透析。
鎂與鈣磷攝入量之比
有很多營養素之間是有關聯的,如鉀與鈉,β-胡蘿卜素與維生素A等等。其中,鎂是與鈣磷有關聯的。鈣、磷、鎂攝入量之比為5:3:1。如果其中一樣攝入過多或過少,其他營養素就會受影響,就會影響健康。
參看
|
||||||||||||||||||||||||||
|
||||||||||||||||
| 關於「鎂」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |


