肝纖維化
| A+醫學百科 >> 肝纖維化 |
肝纖維化(hepatic fibrosis)是指肝臟內瀰漫性細胞外基質(特別是膠原)過度沉積。它不是一個獨立的疾病,多種慢性肝臟疾病均可引起肝纖維化。
目錄 |
病因及發病機制
病因
肝纖維化(hepatic fibrosis)是指肝臟內瀰漫性細胞外基質(特別是膠原)過度沉積。它不是一個獨立的疾病,而是許多慢性肝臟疾病均可引起肝纖維化,其病因大致可分為感染性(慢性乙型、丙型和丁型病毒性肝炎,血汲蟲病等),先天性代謝缺陷(肝豆狀核變性、血色病、α1-抗胰蛋白酶缺乏症等)及化學代謝缺陷(慢性酒精性肝病、慢性藥物性肝病)及自身免疫性肝炎、原發性肝汁性肝硬化和原發性硬化性膽管炎等。
發病機制
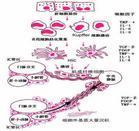
在正常肝組織中,各種細胞及細胞外基質萬分有精確的相對比例和特定的相對空間位置,通過細胞之間、細胞與細胞外基質之間的信號傳遞精確地調控著結構、功能和代謝狀態,成為一個相對穩定的微生態系統。從動態的觀點來看,纖維增生是指各種細胞外基質合成增加,而纖維分解則是指細胞外基質的降解過程;肝纖維化的發生、發展和轉歸取決於二者的「淨效應」。急性肝損害所致肝臟纖維增生是機體對於肝實質損傷的一種修復反應,一旦病因去除則過多的細胞外基質被降解,肝組織內細胞內細胞與基質萬分恢復正常,因而不產生肝臟纖維化。但慢性肝病所致的持續或反覆的肝實質炎症壞死可引起纖維結締組織大量增生、而其降解活性相對或絕對不足,因此大量細胞外基質沉積下來形成肝纖維化。如果肝纖維化同時伴有肝小葉結構的破壞(肝再生結節),則稱為肝硬化。但是,在臨床上難以將兩者截然分開,因為慢性肝病由肝纖維化到肝硬化是一個連續的發展過程。近年的基礎和臨床研究表明,如果能給予有效的病因治療,或能直接抑制細胞外基質的合成和/或促進其降解,則已經形成的肝纖維化甚至早期肝硬化也是可以逆轉的。
病理改變
表現為肝臟細胞外基質合成增多,降解減少。
臨床特徵
(2) 肝纖維化臨床表現食慾減退,往往是最早症状,有時伴噁心,嘔吐.
(3) 慢性消化不良症状,腹脹氣,便秘或腹瀉,肝區隱痛等,臨床上部分患者無明顯的慢性肝病史,肝纖維化臨床表現原因不明出現上述消化不良症状,對症治療效果不佳.經進一步檢查才發現.
(4) 慢性胃炎,許多慢性肝炎患者出現反酸,噯氣,呃逆,上腹部隱痛及上腹飽脹等胃區症状.
(5) 肝纖維化臨床表現出血,慢性肝炎由於肝功能減退影響凝血酶原及其他凝血因子的合成,肝纖維化臨床表現常出現蜘蛛痣、鼻衄,牙齦出血,皮膚和粘膜有紫斑或出血點,女性常有月經過多.
伴發疾病
一般而言,慢性肝病因肝臟持續性損傷,多會伴有肝纖維化。我國慢性肝病中以慢性B型肝炎最多,慢性C型肝炎也不少見。這兩類肝炎都因肝炎病毒複製,刺激了人體的免疫系統,造成免疫淋巴細胞在清除病毒時,「誤傷」肝細胞,產生肝臟內炎症,誘導了纖維組織增生,致使肝纖維化。隨著人民生活水平的提高,我國酒精性肝病和非酒精性肝病的發病率不斷上升。這兩種肝病中較重的病變是脂肪性肝炎,如不積極治療,損傷的肝細胞也可刺激肝內纖維組織的大量增生,由肝纖維化發展到肝硬化。肝癌是各種肝病中最為兇險的疾病,常常同時伴有肝硬化。其他如藥物性肝病、代謝性肝病、自身免疫性肝病或血吸蟲病等,也與肝纖維化有染。由於每個患者體質情況和發病情況不一樣,纖維化的程度與病情的程度或病程的長短可能不成正比關係。
肝纖維化的臨床診斷
a、肝活檢病理學檢查:仍是診斷肝纖維化的金標準,是明確診斷、衡量炎症活動度、纖維化程度以及判定藥物療效的重要依據[1]。目前一般採用半定量計分系統。但是,由於肝纖維化在肝內分布不均勻,而且肝穿刺組織僅佔全肝的五萬分,可造成診斷誤差。因此強調肝活檢標本至少15 mm,並包含6個以上匯管區。Bedossa等[2]研究表明:按METAVIR計分系統標準,如肝穿組織為15 mm,肝纖維化診斷符合率為65%,如肝穿組織為25 mm,符合率為75%,因此主張不少於25 mm。另外肝活檢是一種創傷性檢查,穿刺後疼痛(24.6%)以及其他併發症使半數左右患者不願接受該項檢查。因此探索以非創傷性檢查替代肝穿刺活檢成為當務之急。
b、生化學檢測:血清HA、 LN、 PCIII、CIV可反映肝纖維化程度,特別是HA和PCIII對早期肝纖維化的價值最高,同時也受肝臟炎症程度的影響。但有認為慢性C肝患者HA水平與纖維化分級呈正相關,與肝臟炎症活動關係不大。也有認為CIV水平和肝纖維化及門脈高壓程度關係較大,而與肝臟炎症活動關係較小。蔡衛民等[3]利用ROC曲線,對60例慢性B肝患者肝活檢病理組織學檢查結果與血小板衍生生長因子BB(PDGFBB)、轉化生長因子β1(TGFβ1)、基質金屬蛋白酶抑制劑1(TIMP1)、基質金屬蛋白酶1(MMP1)、 HA、 PCIII、CIV、LN和外周血單核細胞(PBMC)進行比較,結果表明:HA、 PCIII、 CIV、 LN有一定價值,血清PDGFBB的診斷價值最大。在篩選肝纖維化患者時,以血清PDGFBB和TIMPl mRNA聯合檢測最佳。另外國內外學者提出YKL40(人類軟骨蛋白39)可用於評價肝纖維化程度[4]。 近年來推出的Fibrotest (FT)和ActiTest (AT)系統提供了評價肝纖維化的簡便、非創傷性的檢查方法,FT通過檢測血中載脂蛋白A1、α2巨球蛋白、觸珠蛋白和總膽紅素,能簡便、快速、準確定量評價肝纖維化的程度(FT值為0.00~1.00),而ActiTest (AT)系統,通過檢測ALT和GGT,能定量評價肝臟的炎症壞死的程度(AT值也是0.00~100)[5-7]。Naveau等[6]對攝入酒精>50 g/d(平均100 g/d)的221例患者同時行肝穿刺活檢、FT和HA檢測。肝穿刺活檢按METAVIR系統分級,其中明顯肝纖維化(F2~F4)佔63%。 FT的平均值:F0=0.29;F1=0.29;F2=0.40;F3=0.53;F4=0.88(除F0和F1之外,其餘各組之間P值均<0.05)。而HA對F2和F1以及F2和F0之間無統計學上差異。 對F4的診斷,FT和HA的UROC (area under the ROC curves)都非常高,分別為0.95和093。Myers等[8]對209例HBV患者進行研究,其中61例(29%)纖維化分期為F2~F4,FT能正確作出評價(AUROC為0.78±0.04)。 FT積分在≤0.20和>0.80之間者,對肝纖維化的陽性和陰性預測值都是92%。因此認為只需要對FT>0.20和≤0.80之間的患者進行肝穿刺,以明確肝纖維化及其程度。Poynard複習了16篇文獻後指出:對慢性HCV患者來說,FT和AT可以取代肝穿刺對肝纖維化和炎症壞死狀況作出評價,肝穿刺應作為第二線,僅適用於對FT和AT結果有高度懷疑者[9]。
c、影像學檢查:B超對肝臟表面、肝臟回聲、肝靜脈、肝邊緣和脾臟面積5項參數與肝纖維化分期有很好的相關性,但對1~3期較難區分。也有人認為門靜脈主幹、門靜脈每分鐘血流量參數、脾厚度、脾靜脈寬度及肝右葉最大斜徑等參數的改變與肝纖維化的程度有較好的相關性。
彩色都卜勒超聲有助於評價肝纖維化的程度,因為肝纖維化時,肝動脈血流速度增加,門靜脈血流速度減慢,因此二者(A/V)的比值能更全面地反映肝纖維化的血流動力學變化,優於單純測定門靜脈流速或肝靜脈頻譜改變的檢測。Fibroscan(FS)是近年來推出的單維瞬變彈性圖,是以超聲(5 MHz )和低頻彈性波(50 Hz )結合的測量組織硬度的儀器。由於肝臟的硬度與肝纖維化相關,因此反射波kPa越高,肝纖維化程度越重。Sandrin等[10]報導:FS的反射波≤5.1 kPa者,93%患者纖維化程度屬於F0或F1,如反射波≥7.6 kPa,94%患者纖維化程度≥F2。Zio1等[11]報導:5例反射波≤3 kPa者,都是F1,而將反射波8.74 kPa、 9.56 kPa和14.52 kPa作為F≥2, F≥3和F=4的閾值,對肝纖維化有較高的敏感性和特異性。因此對反射波≥8.74kPa的患者需要治療,無需進行肝穿刺。FS的局限性是不適用於腹水患者、肋間隙狹窄以及肥胖者。Castera等.[7].對183例慢性C肝患者,同時檢測FS、FT和ARPI,並和肝穿刺活檢作對照。
按METAVIR分級F1=47; F2=53; F3=37; F4=46。FS值:F≥2 =7.1 kPa; F≥3=95 kPa;
F=4=12.5 kPa。結果顯示:FS是檢測肝纖維化的簡單而有效的方法;同時檢測FS和FT並與肝穿刺結果作比較,F≥2符合率為84%, F≥3為95%, F=4為94%。因此對大多數肝纖維化患者來說可避免肝穿刺。總之FS的優點是無創傷,患者無痛苦、無併發症,操作簡便、快速(<5 min ),可在門診或床邊進行,由於量化,結果客觀而可靠、重複性好。有望取代肝穿刺以診斷和監測肝纖維化的進程。
治療
抗肝纖維化的藥物治療主要包括:
(1)針對原發病去除致病因素,如抗B型肝炎、C型肝炎病毒治療、抗血吸蟲治療、戒酒等。
(2)針對肝纖維化本身的治療,如通過抑制炎症或脂質過氧化,或者抑制肝星狀細胞的增生活化,以及促進膠原降解等。目前已發現了具有抗纖維化作用的藥物,其中很多僅在各種動物模型中驗證了效果並且探討了機制。在這裡我們重點討論的是已經在各種臨床慢性肝病中應用過的抗纖維化藥物,特別是探討了近5年來進行的臨床試驗中這些藥物的療效。
1、皮質類固醇激素:皮質類固醇常被用做各種肝病時的抗炎症藥物,但是目前僅在兩類慢性肝病時證實有效。一類是自身免疫性肝炎,2004年Czaja等報導87例自身免疫性肝炎患者應用皮質類固醇平均治療5年的結果,通過對325個肝活組織樣本分析提示,53%患者的纖維化積分改善,26%患者纖維化無進展。與以前報導的臨床療效一致。另一類是重症酒精性肝炎特別是對有腦病症状的患者,類固醇短期治療者存活期延長,但2006年Phillips等報導認為這種對生存率的提高在1年後變得不再顯著。
2、秋水仙鹼:是一種植物鹼類,其機制是通過抑制膠原分泌過程中的微管聚合達到抑制纖維化的目的。從1986年開始報導對原發性膽汁性肝硬化患者的許多生物化學指標有改善,但是沒有減輕纖維化。然而1988年Kershenobich等報導了秋水仙鹼治療酒精性肝炎和其他多種肝病纖維化患者的隨機雙盲臨床試驗,對100例患者隨訪了14年,結果表明秋水仙鹼不僅可以改善纖維化,還可以顯著提高患者生存率。但是此項研究被質疑方法學有問題而沒有常規應用於臨床。隨後進行的多項薈萃分析和2005年Morgan等用秋水仙鹼治療酒精性肝硬化的隨機雙盲臨床試驗中,秋水仙鹼對於纖維化和生存率均沒有明顯改善。
3、水飛薊素:水飛薊素是植物乳薊的活性成分,可以有抗脂質過氧化和纖維形成的作用。所有臨床研究證實其使用是安全的,但是對抗纖維化的結果不一致。Ferenci等報導在酒精性肝硬化中,水飛薊素可以降低病死率,早期肝硬化緩解。但Parés等報導200例肝活組織檢查或腹腔鏡證實有酒精性肝硬化的患者,進行隨機雙盲安慰劑對照試驗,結果卻不支持水飛薊素可以改善酒精性肝硬化患者的生存率。2002年Lucena等其他小樣本研究也發現6個月的短期臨床治療僅有抗脂質過氧化等作用。
肝纖維化4.干擾素(干擾素α和干擾素γ):Poynard等報導四個臨床試驗的3010例初治的C型肝炎纖維化患者用干擾素α聯合利巴韋林治療24周,以METAVIR積分減輕最少1期為標準,大多患者的纖維化都比治療前有所減輕。入組時有肝硬化的患者中,49%有肝硬化逆轉。纖維化的減輕與開始的纖維化程度、對病毒應答率、病毒水平與年齡和體重均有關。干擾素γ雖然抗病毒的效果弱於干擾素α,但是可以通過抑制星狀細胞的細胞外基質合成等機制產生抗肝纖維化效果。Muir等報導對20例干擾素α治療無效或不能耐受的C型肝炎患者,用干擾素γ治療24周,治療前後做肝穿刺檢查。結果提示應用干擾素γ是安全的,有30%的患者有纖維化改善。Weng等用干擾素γ治療99例B型肝炎肝纖維化患者,療程9個月,通過肝活組織檢查,治療組有63%,對照組有21%的患者肝纖維化有改善。
5、熊去氧膽酸:熊去氧膽酸可以通過穩定細胞膜的細胞保護作用減輕炎症和纖維形成。Poupon等對367例原發性膽汁性肝硬化患者用熊去氧膽酸治療2年,隨機對照研究提示可以減輕纖維化,特別是在開始階段Ⅰ/Ⅱ期的早期的患者,可以顯著改善纖維化的進展。除了原發性膽汁性肝硬化以外,熊去氧膽酸可以減輕兒童的家族性肝內膽汁淤積和囊性纖維化的纖維化形成。Lindor等報導166例非酒精性脂肪性肝炎患者的隨機、安慰劑對照研究,隨訪2年的配對肝活組織檢查,提示熊去氧膽酸對肝纖維化,甚至對脂肪肝和炎症壞死均沒有改善。Dufour等應用熊去氧膽酸和維生素E聯合治療非酒精性脂肪性肝炎患者的研究,結果提示2年的治療僅可以改善實驗室生物化學指標和脂肪肝程度。
6、多不飽和磷脂醯膽鹼:對肝臟炎症和纖維形成中的氧化應激過程進行有效的抗氧化作用。Lieber等報導對789例酒精性肝病患者的隨機、雙盲、安慰劑對照試驗中,觀察持續2年時間後,由於沒有料想到入選患者的平均每日飲酒量從224g乙醇減少至35g乙醇,結果顯示多不飽和磷脂醯膽鹼沒有比安慰劑更顯著地改善纖維化,但是對一些亞組患者多不飽和磷脂醯膽鹼可以降低轉氨酶和膽紅素。
7、白細胞介素(IL)-10:IL-10是抗炎和免疫抑制的細胞因子,通過減少炎症前細胞因子腫瘤壞死因子α和IL-1等減輕炎症反應,並使T細胞向Th2轉化。Nelson等報導IL-10治療抗病毒無效的30例C型肝炎肝纖維化患者的1年試驗中,IL-10可以減輕肝內炎症和纖維化,但是HCV-RNA從治療開始的12.3mEq/ml增加到38mEq/ml。這使得病毒性肝炎患者長期應用IL-10受到了質疑。
8、氯沙坦:腎素-血管緊張素-醛固酮系統在纖維化形成中有重要作用。其主要的效應因子血管緊張素Ⅱ可以通過誘導轉化生長因子β1表達刺激膠原沉積。應用血管緊張素轉換酶抑制劑氯沙坦可以觀察到肝組織纖維化程度減輕。Yokohama等觀察了7例非酒精性脂肪性肝炎合併高血壓的患者,口服氯沙坦48周後有4例肝組織學纖維化改善,與C型肝炎肝硬化後肝移植患者的回顧性試驗研究結果相似。
9、吡非尼酮(Pirfenidone):2005年Azuma報導包括107例肺間質纖維化患者的隨機、雙盲、安慰劑對照的臨床研究,結果提示患者的氧和能力顯著改善,肺功能急性加重頻率顯著降低,治療組生存率顯著提高。隨後在多種肝纖維化動物模型中證實了吡非尼酮可阻斷纖維化,表現為病理纖維化評分改善、組織膠原含量降低、α-平滑肌肌動蛋白陽性細胞減少等,同時伴有轉化生長因子β1表達下降、促進膠原降解的基質金屬蛋白酶表達上調等。2006年Armenda'riz-Borunda等報導應用吡非尼酮(1200mg/d)治療C型肝炎肝硬化患者15例的小樣本臨床研究,療程12周,治療前後肝活組織檢查比較,53%患者肝臟炎症指數改善,30%Ishak肝纖維化分期降低,60%患者脂肪變性好轉。
10、復方牛胎肝提取物:蔡衛民等做了復方牛胎肝提取物片治療大鼠肝纖維化的實驗研究,結果顯示:治療組大鼠死亡數和肝纖維化組織學半定量計分,明顯低於對照組。李謙等採用多中心、自身對照研究,觀察復方牛胎肝提取物片治療115例肝纖維化患者的效果,患者口服復方牛胎肝提取物片2片/次,3次/d,治療24周,治療前均做肝活組織檢查,其中有38例患者在治療後再次做肝活體組織檢查。結果顯示:血清肝纖維化標誌物透明質酸、層黏連蛋白、Ⅳ型膠原蛋白,治療後24周和36周,較治療前(0周)比較顯著降低,差異有統計學意義。肝活組織病理檢查顯示,治療後肝組織纖維化分期比治療前有明顯降低(P<0.01)。
不良後果
如果治療不當主要可通過兩大危害形成肝硬化:一是由於肝組織結構的破壞,使肝內血管受壓扭曲、閉鎖或動脈與靜脈之間出現「短路」吻合,造成門靜脈系統血管阻力增大,形成門靜脈高壓,導致脾腫大、腹水生成和胃底食管靜脈曲張,有上消化道曲張靜脈破裂出血的潛在危險;二是正常肝細胞之間的血液微循環通道因纖維組織成分的沉積而造成循環障礙,影響肝細胞的血液供應,使因炎症受損的肝細胞不易修復甚至加重損傷,直至功能正常的肝細胞愈來愈少,最後導致肝功能衰竭。兩大危害都是致命的。
預防保健
1.情緒穩定:肝臟與精神情志的關係非常密切。情緒不佳,精神抑鬱,暴怒激動均可影響肝的機能,加速病變的發展。樹立堅強意志,心情開朗,振作精神,消除思想負擔,會有益於病情改善。
2.動靜結合:肝纖維化代償功能減退,並發腹水或感染時應絕對臥床休息。在代償功能充沛、病情穩定期可做些輕鬆工作或適當活動,進行有益的體育鍛煉,如散步、做保健操、太極拳、氣功等。活動量以不感覺到疲勞為度。
3.用藥從簡:盲目過多地濫用一般性藥物,會加重肝臟負擔,不利於肝臟恢復。對肝臟有害的藥物如異煙肼、巴比妥類應慎用或忌用。
4.戒煙忌酒:酒能助火動血,長期飲酒,尤其是烈性酒,可導致酒精性肝硬化。因此,飲酒可使肝硬化患者病情加重,並容易引起出血。長期吸煙不利於肝病的穩定和恢復,可加快肝硬化的進程,有促發肝癌的危險。
5.飲食調護:以低脂肪、高蛋白、高維生素和易於消化飲食為宜。做到定時、定量、有節制。早期可多吃豆製品、水果、新鮮蔬菜,適當進食糖類、雞蛋、魚類、瘦肉;當肝功能顯著減退並有肝昏迷先兆時,應對蛋白質攝入適當控制,提倡低鹽飲食或忌鹽飲食。食鹽每日入量不超過1~1.5克,飲水量在2000毫升內,嚴重腹水時,食鹽攝入量應控制在500毫克以內,水攝入量在1000毫升以內。應忌辛辣刺激之品和堅硬生冷食物,不宜進食過熱食物以防並發出血。
6.積極預防:肝硬化是由不同原因引起的肝臟實質性變性而逐漸發展的一個後果。
要重視對各種原發病的防治,積極預防和治療慢性肝炎、血吸蟲病、胃腸道感染,避免接觸和應用對肝臟有毒的物質,減少致病因素。
肝纖四項
肝纖四項即肝纖維化四項檢查,該檢查主要用來檢查診斷慢性肝病患者病情發展狀況和治療效果,衡量炎症活動度、纖維化程度的重要依據。診斷肝纖維化需要進行肝纖四項檢查。肝纖四項主要包括以下四個檢查指標:
1. PCIII (III型前膠原):反映肝內III型膠原合成,血清含量與肝纖程度一致,並與血清γ-球蛋白水平明顯相關。PCIII與肝纖維化形成的活動程度密切相關,但無特異性,其它器官纖維化時,PCIII也升高。持續PCIII升高的慢活肝,提示病情可能會惡化並向肝硬變形成發展,而PCIII降至正常可預示病情緩解,說明PCIII 不僅在肝纖維化早期診斷上有價值,在慢性肝病的預後判斷上也有意義。
血清PCⅢ水平與肝纖維化病變程度呈密切相關,反映肝纖維合成狀況和炎症活動性,早期即顯著升高,而陳舊性肝硬化和部分晚期肝硬變、肝萎縮患者血清PCⅢ不一定增高。
2. IV-C(IV型膠原):為構成基底膜主要成份,反映基底膜膠原更新率,含量增高可較靈敏反映出肝纖過程,是肝纖的早期標誌之一。
(1) 在肝纖維化時出現最早,適合於肝纖維化的早期診斷。
(2) 能反映肝纖維化程度,隨著慢遷肝→慢活肝→肝硬化→肝癌病程演病,Ⅳ-C膠原在血清含量逐步升高。
(3)對重症肝炎和酒精性肝炎也顯高值。
(4)是藥物療效和預後觀察重要依據,血清Ⅳ-C水平與肝組織學的改變完全一致。
(5)在與基底膜相關疾病可出現Ⅳ-C水平的異常,如甲狀腺機能亢進,中晚期糖尿病、硬皮病等。
3. LN(層粘連蛋白):為基底膜中特有的非膠原性結構蛋白,與肝纖維化活動程度及門靜脈壓力呈正相關,慢活肝和肝硬變及原發性肝癌時明顯增高 ,LN也可以反映肝纖維化的進展與嚴重程度。另外,LN水平越高,肝硬變病人的食管靜脈曲張越明顯。
(1) 反映肝纖維化:正常肝臟間質含少量LN,在肝纖維化和肝硬化時, →肌成纖維細胞增多→大量合成和分泌膠原、LN等間質成分→形成完整的基底膜(肝竇毛細血管化)。肝竇毛細血管化是肝硬化的特徵性病理改變, LN與纖維化程度和門脈高壓正相關,纖維化後期升高尤為顯著。
(2) 與腫瘤浸潤、轉移有關:癌症轉移首先要突破基底膜,因此LN與腫瘤浸潤轉移有關。大部分腫瘤患者血清LN水平升高,尤以乳腺癌、肺癌、結腸癌、胃癌顯著。
(3) 與基底膜相關疾病有關:如先兆子癇孕婦血清較正常妊娠者顯著升高,提示可能與腎小球及胎盤螺旋動脈損傷有關。血清LN與糖尿病、腎小球硬化等疾病有關。
4. HA(透明質酸酶):為基質成分之一,由間質細胞合成,可較準確靈敏地反映肝內已生成的纖維量及肝細胞受損狀況,有認為本指標較之肝活檢更能完整反映出病肝全貌,是肝纖維化和肝硬變的敏感指標。
(1) 血清HA在急肝、慢遷肝時輕度升高;慢活肝時顯著升高;肝硬化時極度升高。
(2) 肝硬化病人血清HA極度升高。
(3) HA水平與血清膽紅素、SGPT(Serum glutamic-pyruvic 血清谷丙轉氨酶)、γ-球蛋白呈正相關
(5) 故血清HA水平是反映肝損害嚴重程度、判斷有無活動性肝纖維化的定量指標 。
(6) 對慢遷肝與慢活肝的鑒別診斷,慢遷肝HA濃度與正常人無差別,而慢活肝的升高明顯。
(7) 有助於估價肝病發展趨勢,在急性肝炎→慢活肝→肝硬化發展中,血清HA逐步並優於其他肝硬化診斷指標等。
健康問答網關於肝纖維化的相關提問
| Error: It's not possible to get http://www.wenda120.com/tags/3304/rss... |
| 關於「肝纖維化」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |