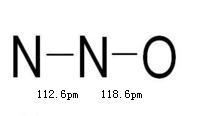一氧化二氮
| A+醫學百科 >> 一氧化二氮 |
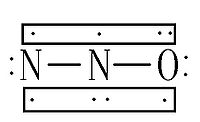
一氧化二氮(Nitrous Oxide)又稱笑氣,無色有甜味氣體,是一種氧化劑,化學式N2O,在一定條件下能支持燃燒(同氧氣,因為笑氣在高溫下能分解成氮氣和氧氣),但在室溫下穩定,有輕微麻醉作用,並能致人發笑。其麻醉作用於1799年由英國化學家漢弗萊.戴維發現。有關理論認為N2O與CO2分子具有相似的結構(包括電子式),則其空間構型是直線型,N2O為極性分子。2009年8月份,美國一項最新研究顯示,這種無色有甜味的氣體已經成為人類排放的首要消耗臭氧層物質。現在主要用於表演。
目錄 |
簡介
一氧化二氮早期被用於牙科手術的麻醉,是人類最早應用於醫療的麻醉劑之一。它可由NH4NO3在微熱條件下分解產生,產物除N2O外還有一種,此反應的化學方程式為 )NH4NO3====N2O↑+2H2O;等電子體理論認為N2O與CO2分子具有相似的結構(包括電子式),則其空間構型是直線型,N2O為極性分子。
基本信息
中文名稱:一氧化二氮。
英文名稱:Dinitrogen oxide;Laughing gas。
別名:氧化亞氮;笑氣。
CAS No.:10028-97-2。
分子式:N2O。
分子量:44.01。
危險標記:5(不燃氣體)。
包裝方法:鋼質氣瓶。
醫學應用
【別名】 笑氣,氧化亞氮,
連二次硝酸酐
【分子結構】一氧化二 氮分子為直線形分子,極性分子。N2O的分子是直線形的(N-N-O),N,O原子採取sp雜化,生成兩個σ鍵,兩個三中心四電子π鍵,N的氧化數為+1。
【英文名稱】Nitrous Oxide 西班牙名稱: Oxido Nitroso
【醫學適應症】 因全麻效果差,目前常與氟烷、甲氧氟烷、乙醚或靜脈全麻藥合用。現已少用。氧化亞氮(N2O)用於麻醉,對呼吸道無刺激,對心、肺、肝、腎等重要臟器功能無損害。在體內不經任何生物轉化或降解,絕大部分仍以原藥隨呼氣排出體外,僅小量由皮膚蒸發,無蓄積作用。吸入體內只需要30s~40s 即產生鎮痛作用,鎮痛作用強而麻醉作用弱,受術者處於清醒狀態(而不是麻醉狀態) ,避免了全身麻醉併發症,術後恢復快。
【醫學上用量用法】 吸入:用量視手術需要和病人情況而定。
【醫學上注意事項】 1.大手術需配合硫噴妥鈉及肌肉鬆弛劑等;吸入氣體中氧氣濃度不應低於20%;麻醉終止後,應吸入純氧10分鐘,以防止缺氧。 2.當病人有低血容量、休克或明顯的心臟病時,可引起嚴重的低血壓。氧化亞氮對有肺血管栓塞症的病人可能也是有害的。
【禁忌症】(1)氣囊腫(2)腸梗阻、腸脹氣(3)氣胸(4)氣腦(5)高頭位開顱手術
【醫學藥品規格】 氣體:用耐壓鐵筒裝。
【貯藏】 置耐壓鋼瓶內,在涼暗處保存。
【作用與用途】吸入純粹本品氣體能迅速引起麻醉狀態和窒息,因此,必須與氧混合使用。誘導時間短。若不補充維持劑量,可迅速蘇醒。本品可用於馬、反芻動物、犬和貓的維持麻醉。
【用法與用量】本品用耐高壓鋼瓶盛裝。用於小動物麻醉:75%氧化亞氮同25%氧混合,通過面罩給予2-3分鐘,然後再加入氟烷,使其在氧化亞氮和氧混合氣體中達3%濃度,直至出現下頜鬆弛等麻醉徵象為止。
物理性質
熔點 -90.8℃
沸點 -88.49℃
臨界溫度 36.5℃
臨界壓力 7.263×10Pa
相對密度 1.977
折光率 1.0005-7265 bar
化學性質
一氧化二氮加熱或撞擊硝酸銨可以生成一氧化二氮和水:NH4NO3=N2O↑+2H2O,工業上對硝酸銨熱分解可製得純度95%的一氧化二氮,一個笑氣分子與六個水分子結合在一起。當水中溶解大量笑氣時,再把水冷卻,舊會有笑氣晶體出現。把晶體加熱,笑氣會逸出。人們利用笑氣這種性質,制高純笑氣。
製取方法
【原理】硝酸銨在169.5℃熔融,在220℃分解成一氧化二氮和水
NH4NO3==加熱==N2O↑+2H2O
【用品】大試管、鐵架台、酒精燈、水槽、集氣瓶、乾燥硝酸銨粉末
【操作】
1.在能適當加熱的乾燥裝置中,在80--100℃的溫度下,使硝酸銨充分乾燥。然後用乾的研缽磨碎,再在80--100℃的溫度下乾燥後,迅速放入瓶里加塞保存備用。
2.取2g上述乾燥的硝酸銨,加入乾燥的試管里,按圖裝配好,加熱(剪短酒精燈的燈蕊,使火焰不太大)後。硝酸銨熔融成液體,以後像水沸騰那樣,氣泡翻滾。用向上排空氣法收集一氧化二氮氣體。
【備註】
1.本實驗加熱的溫度不宜過高。溫度過高,可能分解生成氮氣、一氧化氮和二氧化氮。特別是在高溫下容易引起爆炸。
2.硝酸銨的用量控制在2g左右,以免發生爆炸。
3.試管口應略低於水平。這樣就能避免反應生成的水跟加熱部分接觸,引起試管破裂。
4.2g硝酸銨在常溫、常壓下理論上能收集到610mL一氧化二氮,但由於部分熔融硝酸銨隨生成的水流去,只能收集到300mL氣體,用一隻mL集氣瓶就可以了
其他製取方法:1、30HNO3+8Fe===8Fe(NO3)3+3N2O↑+15H2O
2、4Zn+10HNO3(稀)===4Zn(NO3)2+N2O↑+5H2O
應急處理
處置
吸入:迅速脫離現場至空氣新鮮處。保持呼吸道通暢。如呼吸困難,給予輸氧。如呼吸停止,立即進行人工呼吸。就醫。
呼吸系統防護:一般不需特殊防護。高濃度接觸時可佩戴自吸過濾式防毒面具(半面罩)。
眼睛防護:一般不需特殊防護。
身體防護:穿一般作業工作服。
手防護:戴防化學品手套。
其他防護:避免高濃度吸入。進入罐、限制性空間或其他高濃度區作業,須有人監護。
泄漏應急處理:迅速撤離泄漏污染區人員至上風處,並進行隔離,嚴格限制出入。建議應急處理人員戴自給正壓式呼吸器,穿一般作業工作服。儘可能切斷泄漏源。合理通風,加速擴散。漏氣容器要妥善處理,修復、檢驗後再用。
有害燃燒產物:氧化氮。
滅火方法:本品不燃。消防人員須佩戴防毒面具,穿全身消防服,在上風向滅火。用霧狀水保持火場中容器冷卻。迅速切斷氣源,用水噴淋保護切斷氣源的人員,然後根據著火原因選擇適當滅火劑滅火。
診斷要點
1.刺激反應
出現一過性胸悶,咳嗽,肺部無陽性體征,X線檢查無異常,一般在24 h內症状消失。
出現咳嗽、咳痰、胸悶、胸痛,可伴有頭暈、頭痛、無力、心悸等症状,肺部聽診呼吸音粗糙,可有散在干、濕囉音,X線胸片示肺紋理增多,增粗、邊緣模糊,白細胞總數增高。血氣分析一般無低氧血症。
3.急性化學性肺炎
出現胸悶加重,咳嗽加劇,呼吸困難,咳痰或咳血絲痰,輕度發紺,兩肺呼吸音降低,聞及干、濕性囉音。X線示肺野透亮度降低,肺紋理增多紊亂,呈網狀陰影或兩肺有散在斑片或點狀性實變陰影,多見於中下肺野。血氣分析:在吸低濃度氧(<50%)時,才能維持動脈氧分壓大於8 kPa(60 mmHg)。
4.急性肺水腫
常伴有化學性肺炎,其發病過程可分為三期:
(1)刺激期和症状緩解期:如吸入較高濃度的氮氧化物時,當時即可出現咽部不適,伴隨有刺激性咳嗽,甚至痙攣性陣咳而引起嘔吐。部分病人刺激期後病情繼續發展,經過幾小時到幾十小時的症状緩解期後出現肺水腫。症状緩解期中有頭昏、無力、食慾減退、煩躁、失眠等,也有完全無症状的,胸部X線檢查無異常。症状緩解期的長短與吸入毒物的量有關。
(2)肺水腫期:有胸悶、胸痛和呼吸急促等症状,咳嗽,咳檸檬色或粉紅色痰。呼吸急促,脈搏加快,體溫升高,兩肺聽診早期呼吸音降低而粗糙,以後有濕囉音,可伴有脈搏緩慢,出現外收縮,出汗、皮膚潮紅等,心電圖可見ST段壓低、T波平坦,白細胞計數和中性粒細胞增多,X線胸片表現早期有肺野透亮度降低和紋理紊亂,晚期可出現大小不等、邊緣模糊、密度不等的結節狀或雲絮狀陰影,廣泛散在於兩肺野內,與肺野分界不很清晰。血氣分析常呈重度低氧血症。如搶救不及時,可出現急性呼吸窘迫症候群(ARDS),昏迷或窒息,甚至死亡。
(3)恢復期:在積極有效的治療後,絕大多數病例的病情可以好轉,一般在5 d左右可以基本痊癒。X線胸片表現在一周左右好轉,全身症状約一至兩個月才能完全恢復。
5.遲發性阻塞性細支氣管炎
表現在肺水腫基本恢復後兩周左右,突然又出現咳嗽、胸悶、進行性呼吸困難,明顯發紺,兩肺可聞及干囉音或細濕囉音。X線胸片示兩肺滿布粟粒陰影。
6.併發症
早期可有自發性氣胸、縱隔氣腫與皮下氣腫;晚期可出現細支氣管炎、支氣管肺炎、支氣管擴張、肺不張等,少數患者可發生支氣管哮喘。
處理原則
(1)迅速、安全將患者救離中毒現場,更換污染衣物,保持安靜,保暖,吸氧,給予對症處理,如鎮靜、鎮咳,解除支氣管痙攣,保持呼吸道通暢。
(2)密切觀察:對密切接觸者,需觀察24~72 h,觀察期間,應靜臥休息,注意病情變化,給予適當的檢查和對症治療。
(3)積極防治肺水腫:應早期、足量給予糖皮質激素。注意保持呼吸道暢通。可給予1%二甲基矽油消泡靈霧化吸入,每次約5 min,不要超過30 min。必要時行氣管切開和正壓吸氧。
(4)氧自由基清除應用,如維生素C、維生素E、Q10、β-胡蘿卜素、還原型谷胱甘肽等均可選擇使用。
(6)對突發性阻塞性毛細支氣管炎,應儘早使用大量腎上腺皮質激素。
氮氣加速系統
NOS全稱NITROUS OXIDE SYSTEM,即氮氣加速系統。是由美國HOLLEY公司開發生產的產品。在目前的世界直線加速賽(DRAG RACING)中,為了在瞬間提高大比率馬力,利用的液態氮氧化物系統正是NOS。其實,早在二次世界大戰中德國空軍已開始使用NOS,戰爭結束後才逐漸被用於直線加速賽。
NOS的工作原理是把N2O(一氧化二氮,俗稱笑氣LAUGH GAS)形成高壓的液態後裝入鋼瓶中,然後在發動機內與空氣一道充當助燃劑與燃料混合燃燒(N2O可放出氧氣和氮氣,其中氧氣就是關鍵的助燃氣體,而氮氣又可協助降溫),以此增加燃料燃燒的完整度,提升動力。
由於NOS提供了額外的助燃氧氣,所以安裝NOS後還要相應增加噴油量與之配合。正所謂「要想馬兒跑得快,就要馬兒多吃草」,燃料就是發動機的草,這樣發動機 的動力才得到進一步的提升。
NOS與渦輪增壓和機械增增壓一樣,都是為了增加混合氣中的氧氣含量,提升燃燒效率從而增加功率輸出,不同的是NOS是直接利用氧化物,而增壓則是通過外力增加空氣密度來達到目的的。也許有人會問為什麼不直接使用氧氣而用N2O呢?那是因為用氧氣難以控制發動機的穩定性(高溫和爆發力)。
儲存N2O的專用儲氣罐淨重約6.7kg,充滿N2O後約11kg。按照每次使用1min來算(專家建議NOS系統每次使用時間不可超過1min,一瓶氣用3538次左右。
根據一輛夏利2000的實際升級情況,其1.342L的8A發動機加裝NOS後,其0~100km/h加速時間減少了23%,而功率提升了21kw。
NOS系統使用時間最好不要超過10S。好像目前還沒有引擎能夠承受1min以上的NOS噴射…… 因為長時間使用NOS噴射,可以使發動機內壁磨損嚴重,最終引起俗稱「爆缸」的嚴重後果。一些賽車遊戲中的N2O,也就是指的這個加速裝置。
環境效應
一 氧化二氮(N2O)是一種具有溫室效應的氣體,是《京都議定書》規定的6種溫室氣體之一。N2O在大氣中的存留時間長,並可輸送到平流層,同時,N2O也是導致臭氧層損耗的物質之一。
與二氧化碳相比,雖然N2O在大氣中的含量很低,但其單分子增溫潛勢卻是二氧化碳的310倍;對全球氣候的增溫效應在未來將越來越顯著,N2O濃度的增加,已引起科學家的極大關注。目前,對這一問題的研究,正在深入進行。
|
||||||||
|
|||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
| 關於「一氧化二氮」的留言: | |
給一氧化二氮條目的留言--118.186.209.18 2014年12月30日 (二) 09:47 (CST) 留言:19世紀初,英國開始風行吸入一氧化二氮,或稱笑氣,因為有人發現使用這種氣體會」給人一種高度的快感和刺激「。在隨後的半個世紀里,它成了年輕人使用的一種高檔毒品。有個名叫阿斯克協會的學術團體一度不在致力余別的事情,專場舉辦」笑場晚會「,志願者可以在那裡狠狠吸上一口,提提精神,然後以搖搖擺擺的滑稽姿態逗樂觀眾。直到1846年,才有人有時間為一氧化二氮找到了一條實用圖徑:用做麻醉藥。事情是明擺著的,過去怎麼誰也沒想到,害的天知道有多少萬人在外科醫生的刀下吃了不必要的苦頭。 | |
| 添加留言 | |