醚
| A+醫學百科 >> 醚 |
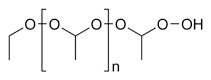
醚(漢語拼音:mí,英語:Ether)是具有醚官能團的一類有機化合物。醚官能團是由一個氧原子連接兩個烷基或芳基所形成,醚的通式為:R–O–R。它還可看作是醇或酚羥基上的氫被烴基所取代的化合物。[1]
醚類中最典型的化合物屬:乙醚,它常用於有機溶劑與醫用麻醉劑。由於其在化學中的常用性(乙醚是最常用的醚類提取溶劑),我們還有時將乙醚直接簡稱為「醚」。醚類化合物的應用常見於有機化學和生物化學,它們還可作為糖類和木質素的連接片段。
目錄 |
結構和化學鍵
醚的結構通式為:R-O-R(R')、Ar-O-R或Ar-O-Ar(Ar')(R=烴基,Ar=芳烴基)。醚的鍵角約為110°,C-O鍵長為140pm,C-O鍵的旋轉能壘的能量很小,而水、醇與醚分子中氧的鍵合能力也與此相似。根據價鍵理論,氧原子的雜化狀態是sp3。
氧原子的電負性比碳更強,因此與氧連接的α氫原子酸性強於碳連接的α氫原子,然而其酸性比不上羰基α氫原子。
分類
醚可以根據醚鍵是否成環分為:直鏈醚和環醚兩大類。 分子中含有多個-O-CH2-CH2-結構單元的大環醚稱為冠醚。冠醚是一種大環多醚,因分子性狀類似王冠而得名。 在直鏈醚中,氧原子所連接的兩個烴基相同則稱為:單醚; 兩個烴基不相同則稱為:混醚;兩個烴基中有一個或兩個是芳基的稱為:芳香醚。
命名
醚的普通命名法是於烴基後加上「醚」字,習慣上對稱醚的「二」字可省略。醚的兩個不同基團排列順序通常是:先小基團後大基團。芳香醚的命名習慣則為:苯基或芳烴基在前。英文命名則按字母順序。冠醚的命名為 x-冠-y,x代表環總原子數,y代表環中氧原子數。
物理性質
醚分子不能互相形成氫鍵,因此它們具有和醇類相比較低的沸點。醚具有微弱的極性,這是由於醚官能團中碳氧碳的鍵角約110度,而碳氧之間的極性差異沒有抵消(不同於二硫化碳之類的線型分子)。醚類極性不如醇、酯與醯胺類化合物,但是強於烯烴的極性。醚氧原子的孤電子對使它有可能與水分子形成氫鍵。
環狀醚類比如四氫呋喃和1,4-二惡烷能與水混溶,這是因為這類醚分子的氧原子比起烷基醚(鏈狀醚)來說更暴露於分子之外,所以極性比起後者更大。
反應
醚類總體來說化學活性都較低,但強於烷烴(環氧化物、酮、縮醛參見各自條目)。
與醚相關的重要反應講解如下:[2]
醚的裂解
雖然醚能不輕易的發生水解反應,但於酸性條件下(如:氫溴酸或氫碘酸),可斷裂為醇。鹽酸條件下,斷裂醚的速度非常慢。 如:甲醚製備溴代甲烷:
- ROCH3 + HBr → CH3Br + ROH
該類反應都是通過鎓中間體進行,如: [RO(H)CH3]+Br-.
有些醚類能於三溴化硼條件中迅速分解,有時還可用更強的路易斯酸如:三氯化鋁反應,製備溴代烷烴。[3] 這些都取決於取代基的不同,還有些醚類可在特定的試劑中發生裂解,如非常強的鹼。
過氧化物
臨近氧原子,含有CH基團的一級醚或二級醚易形成有機過氧化物,如:乙醚過氧化物。該反應需要氧氣(或者空氣)參與,且在光、金屬和醛的催化下加速反應。得到的過氧化物在高溫或高濃度下具爆炸性,因此操作二異丙基醚、四氫呋喃等醚類溶劑大多都不可蒸干,而廠商在分裝醚類試劑也會放入一些穩定劑,防止大量產生過氧化物。
作為路易斯鹼
醚類可作為路易斯鹼及Bronsted鹼。強酸與醚發生反應,可提供給醚氧原子一個質子,從而形成:「鎓離子」,如:乙醚可以與三氟化硼形成絡合物(BF3.OEt2) 。醚還可與二價鎂絡合成格氏試劑。多聚醚都可與鹼金屬離子牢固的結合。
α-鹵代反應
該反應類似於醚的α氫原子發生過氧化的反應,如:單質氯製備α-氯代醚的反應。
== 合成 == 醚在實驗室條件下可通過許多方法合成:
醇的脫水
醇可通過脫水反應製備醚:
- 2 R-OH → R-O-R +H2O(高溫下)
該反應過程需要高溫(通常在125°C)。該反應還需要酸的催化(通常為硫酸)。上述方法對於製備對稱醚來說有效,但對於不對稱醚卻無能為力,如:乙醚易於通過此法製備,環醚也同樣可用此方法製備(分子內脫水)。另外此方法還會引入一定的副產物,如分子內脫水產物:
- R-CH2-CH2(OH) → R-CH=CH2 + H2O
另外此法只能合成一些簡單的醚,對於複雜的分子醚類分子不太試用。對於複雜分子則需要更溫和的條件來合成。
威廉姆遜醚合成
鹵代烴和醇鹽發生親核取代反應:
- R-ONa + R'-X → R-O-R' + NaX
該反應稱作:威廉姆遜合成。該反應通過用強鹼處理醇,形成醇鹽,而後與帶有合適離去基團的烴類分子反應。這裡的離去基團包括:碘、溴等鹵素,或磺酸酯。該方法對於芳香鹵代烴一般不適用(如:溴苯,參見Ullmann縮合)。該方法還只局限於一級鹵代烴才可得到較好的收率,對於二級鹵代烴與三級鹵代烴則由於太易生成E2消除產物而不適用。
在相似的反應中,烷基鹵代烴還可與酚負離子發生親核取代反應。R-X雖不能與醇反應,但酚卻能夠進行該反應(酚酸性遠高於醇),它可通過一個強鹼,如:氫化鈉先形成酚負離子再進行反應。酚可取代鹵代烴中的X離去基團,形成酚醚的結構,該過程為SN2機理。
- C6H5OH + OH- → C6H5-O- + H2O
- C6H5-O- + R-X → C6H5OR
Ullmann二芳醚合成
Ullmann二芳醚合成的反應很類似於威廉姆遜反應,不同之處在於底物是芳香鹵代烴。該反應需要催化劑才能進行,如:銅。
醇對於烯烴的親電加成反應
醇可與活化後的烯烴進行親電加成:
- R2C=CR2+ R-OH → R2CH-C(-O-R)-R2
該反應需要酸催化,三氟醋酸汞(Hg(OCOCF3)2)常可作為這種反應的催化劑,反應生成具有弗拉基米爾·瓦西里耶維奇·馬爾科夫尼科夫(Markovnikov)立體化學的醚類。使用相似的反應條件,四氫吡喃醚(THP)可作為一種醇的保護基。
製備環氧化合物
環氧化合物通常由烯烴氧化製備。在工業生產中,最重要的環氧化合物是:環氧乙烷,它通過乙烯和氧氣製備。其他的過氧化合物還可通過以下方法製備:
重要的醚
參考文獻
- ↑ 國際純粹與應用化學聯合會."ethers".化學術語總目錄 在線版本.
- ↑ Wilhelm Heitmann, Günther Strehlke, Dieter Mayer "Ethers, Aliphatic" in Ullmann's Encyclopedia of Industrial Chemistry" Wiley-VCH, Weinheim, 2002. doi:10.1002/14356007.a10_023
- ↑ J. F. W. McOmie and D. E. West (1973). "3,3'-Dihydroxylbiphenyl". Org. Synth.; Coll. Vol. 5: 412.
外部連結
- ILPI page about ethers.
- An Account of the Extraordinary Medicinal Fluid, called Aether, by M. Turner, circa 1788, from Project Gutenberg
|
||||||||
|
||||||||||||||||||||||||
參考來源
| 關於「醚」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |