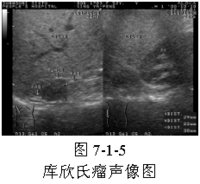
庫欣症候群
| A+醫學百科 >> 庫欣症候群 |
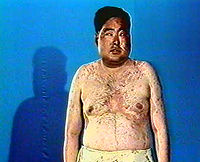
庫欣症候群(Cushing's syndrome)又稱皮質醇增多症(hvpercortisolism)或柯興症候群。1912年,由Harvey Cushing首先報導。本徵是由多種病因引起的以高皮質醇血症為特徵的臨床症候群,典型表現有:臉如滿月,紅潤多脂;軀幹肥胖,四肢瘦小;皮膚菲薄,多有紫紋;高血壓,低血鉀等。常見的病因是垂體分泌過多的促腎上腺皮質激素(ACTH),其次是腎上腺皮質腫瘤和異位ACTH症候群。長期應用較大劑量的糖皮質激素或ACTH可引起類似庫興氏症候群的臨床表現,稱為醫源性庫興氏症候群。飲用大量酒精飲料也可引起類似表現。
男女之比約為1:5。高血壓是常見症状,庫欣症候群約80%的病人有高血壓。收縮壓和舒張壓可達到2級高血壓水平,且為持續性升高。
目錄 |
特點
辨別庫欣症候群其實很容易,患者體型改變極有特點:
1、向心性肥胖,呈現出向心性肥胖,即軀幹肥而四肢瘦;
2、滿月臉,面如滿月,且紅潤多脂;
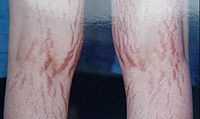
4、紫紋,另外還有紫紋,紫紋多見於腹壁、大腿內外側、臀部的皮膚;
5、性方面,性功能減退,男性陽痿、睾丸變軟,女性月經減少、閉經、不育、多毛;
6、骨骼系統,可見骨質疏鬆,出現腰背痛、脊柱壓縮性骨折,後期可因椎體塌陷而成駝背。
病因
庫欣症候群按其病因和垂體、腎上腺的病理改變不同可分成下列三種:
醫源性皮質醇症
,這在臨床上十分常見。這是由外源性激素造成的,停藥後可逐漸復原。但長期大量應用糖皮質激素可反饋抑制垂體分泌ACTH,造成腎上腺皮質萎縮,一旦急驟停藥,可導致一系列皮質功能不足的表現,甚至發生危象,故應予注意。長期使用ACTH也可出現皮質醇症。
垂體性雙側腎上腺皮質增生
雙側腎上腺皮質增生是由於垂體分泌ACTH過多引起。其原因:①垂體腫瘤。多見嗜鹼細胞瘤,也可見於嫌色細胞瘤;②垂體無明顯腫瘤,但分泌ACTH增多。一般認為是由於下丘腦分泌過量促腎上腺皮質激素釋放因子(CRF)所致。臨床上能查到垂體有腫瘤的僅佔10%左右。這類病例由於垂體分泌ACTH已達一反常的高水平,血漿皮質醇的增高不足以引起正常的反饋抑制,但口服大劑量氟美松仍可有抑制作用。
垂體外病變引起的雙側腎上腺皮質增生 支氣管肺癌(尤其是燕麥細胞癌)、甲狀腺癌、胸腺癌、鼻咽癌及起源於神經嵴組織的腫瘤有時可分泌一種類似ACTH的物質,具有類似ACTH的生物效應,從而引起雙側腎上腺皮質增生,故稱異源性ACTH症候群。這類患者還常有明顯的肌萎縮和低血鉀症。病灶分泌ACTH類物質是自主的,口服大劑量氟美松無抑制作用。病灶切除或治癒後,病症即漸可消退。
腎上腺皮質腫瘤
大多為良性的腎上腺皮質腺瘤,少數為惡性的腺癌。腫瘤的生長和分泌腎上腺皮質激素是自主性的,不受ACTH的控制。由於腫瘤分泌了大量的皮質激素,反饋抑制了垂體的分泌功能,使血漿ACTH濃度降低,從而使非腫瘤部分的正常腎上腺皮質明顯萎縮。此類患者無論是給予ACTH興奮或大劑量氟美松抑制,皮質醇的分泌量不會改變。腎上腺皮質腫瘤尤其是惡性腫瘤時,尿中17酮類固醇常有顯著增高。
腎上腺皮質腫瘤多為單個良性腺瘤,直徑一般小於3~4cm,色棕黃,有完整的包膜。瘤細胞形態和排列與腎上腺皮質細胞相似。腺癌則常較大,魚肉狀,有浸潤或蔓延到周圍臟器,常有淋巴結和遠處轉移。細胞呈惡性細胞特徵。 無內分泌功能的腎上腺皮質腫瘤則不導致皮質醇症。
臨床上發現少數病例腎上腺呈結節狀增生,屬增生與腺瘤的中間型。患者血漿ACTH可呈降低,大劑量氟美松無抑制作用。
臨床上70%的病例為垂體病變所致的雙側腎上腺皮質增生,良性腺瘤佔20~30%,惡性腎上腺腺癌佔5~10%,異位ACTH分泌過多則甚為少見。
臨床表現
脂肪代謝障礙:特徵性表現為向心性肥胖--滿月臉、水牛背、球
形腹,但四肢瘦小。
蛋白質代謝障礙:大量皮質醇促進蛋白質分解,抑制蛋白質合成,形成負氮平衡狀態。病人因蛋白質過度消耗而表現的皮膚菲薄,毛細血管脆性增加,呈現典型的皮膚紫紋。
電解質紊亂:大量皮質醇有瀦鈉,排鉀作用。病人表現為輕度水腫或低鉀血症
心血管病變:高血壓
神經精神障礙:病人易出現不同程度的激動,煩躁,失眠,抑鬱,妄想等神經精神的改變
臨床診斷
庫欣症候群的診斷分三個面:確定疾病診斷、病因診斷和定位診斷。
確定疾病診斷
確定疾病診斷主要依典型的臨床症状和體征。如向心性肥胖、紫紋、毛髮
增多、性功能障礙、疲乏等。加上尿17羥皮質類固醇排出量顯著增高,小劑量氟美松抑制試驗不能被抑制和血11羥皮質類固醇高於正常水平並失去晝夜變化節律即可確診為皮質醇症。早期輕型的病例應與單純性肥胖相鑒別。
小劑量氟美松試驗:服用小劑量氟美松不影響尿中17羥類固醇的測定,但可反饋抑制垂體分泌ACTH。方法是連續6天測定24小時尿中17羥皮質類固醇的排出量,在第3~4天每天口服氟美松0.75mg每8小時1次。將每天測出的值在座標上標出並連成曲線。正常人用藥後2天尿中17羥皮質類固醇的排出量比用藥前明顯減低,如其下降在一半以上則說明有明顯抑制,屬正常。反之降低不明顯或不超過50%,則為皮質醇症。
病因診斷
病因診斷即區別是由腎上腺皮質腺瘤、腺癌、垂體腫瘤引起的皮質增生、非垂體腫瘤或異源性ACTH分泌腫瘤引起的皮質增生。
其它影像學診斷方法
腎上腺正常,部分垂體有占痊
患側腎上腺佔位
患側腎上腺佔位
腎上腺正常,可能發現分泌異源ACTH的病灶
1、蝶鞍的X線學診斷 垂體腫瘤可引起視神經受壓而出現顳側偏盲。在蝶鞍X線點片上可見鞍底、鞍背骨質疏鬆脫鈣,前後突吸收,蝶鞍擴大。分層片或cT則可顯示更小的垂體腫瘤。這種由垂體腫瘤引起繼發性腎上腺皮質增生者約佔皮質醇症的10%。
2、ACTH興奮試驗 腎上腺皮質增生者 對ACTH的刺激仍有明顯反應。其方法同小劑量氟美松試驗,但在第3~4天每天由靜脈滴 入ACTH20u(加入5%葡萄糖液500~1000ml 內,8小時滴完)。腎上腺皮質增生時,注射 ACTH後2天的24小時尿17羥皮質類固醇的排 出量比注射前增高50%以上,血中嗜伊紅細胞計數常同時下降80~90%。腎上腺皮質增生伴有小腺瘤或結節狀皮質增生時,ACTH抑制試驗的反應和增生相似,但有時較弱或不明顯。腎上腺皮質腫瘤時,因正常腎上腺皮質處於萎縮狀態,故不起反應或反應很弱。但病程短,尤其小腺瘤或發展迅速的皮質癌,因腫瘤外的腎上腺皮質尚未萎縮,對此試驗仍有較明顯的反應。異源性ACTH分泌腫瘤因腫瘤大量分泌ACTH,腎上腺皮質已處於持久的高興奮狀態,故對此試驗也不起反應。
3、大劑量氟美松抑制試驗 方法與小劑量氟美松試驗相同,但第3~4天每6小時服氟美松2mg。服藥後尿24小時17羥皮質類固醇排出量比服藥前減少50%以上為陽性反應。異源ACTH分泌腫瘤、皮質腺瘤、皮質腺癌的分泌功能均是自主性的,對此試驗均不起反應。而皮質增生者則可有明顯抑制呈陽性反應。皮質增生伴小腺瘤或結節性增生者儘管ACTH興奮試驗可陽性,但大劑量氟美松卻不能抑制其分泌(即興奮得起,但抑制不下)。此時需作其它試驗來區別是皮質腫瘤還是增生。
4、甲吡酮(雙吡啶異丙酮、甲雙吡丙酮、Su4885)試驗 甲吡酮抑制11β-羥化酶而使11-去氧皮質酮轉變為皮質酮及11-去氧皮質醇轉變成皮質醇的過程受阻,使血漿皮質醇降低,從而反饋抑制減弱,促使垂體分泌大量ACTH。血漿ACTH增高(正常值上午8~10時<100pg/ml),11-去氧皮質醇的合成增多。11-去氧皮質醇包括在17羥及17酮皮質類固醇的測定範圍內,因此尿中17羥及17酮皮質類固醇的排出量也增多。故此試驗可測定垂體分泌ACTH的儲備能力。皮質增生時,甲吡酮試驗呈陽性反應;而皮質腫瘤時,因腫瘤自主地大量分泌皮質醇,抑制了垂體分泌ACTH的能力,甲吡酮的興奮作用不能顯示出來。而垂體腺瘤所致的皮質醇症時,垂體能自主大量分泌ACTH,故也呈陰性反應。
5、加壓素試驗 加壓素有類似CRF的作用,故可用以測定垂體分泌ACTH的儲備功能。皮質增生者呈陽性反應(血ACTH及尿17羥皮質類固醇排多量均增加)。皮質腫瘤者呈陰性反應。加壓素可引起冠狀動脈收縮,故老年、冠心病病人不宜試用。
如ACTH、甲吡酮、加壓素三個試驗均呈無反應,則可能是腎上腺皮質癌;三試驗均為陽性反應時,為皮質增生。
定位診斷
定位診斷主要是腎上腺皮質腫瘤的定位,以利手術切除。但定位的同時,也常解決了病因診斷。
1、X線胸片 可除外肺癌和肺轉移灶。
2、靜脈腎盂造影 了解雙腎情況。較大的腎上腺腫瘤可將患側腎臟向下推移。
3、腹膜後充氣造影 由於腎上腺皮質腺瘤一般不太大,且肥胖病人腹膜後大塊狀脂肪組織常可導致誤診,現已少用。
4、B超 方便有效。對腎上腺皮質腫瘤的定位診斷的正確率可達90%以上。
5、CT對直徑0.5~1cm以上的腎上腺皮質腺瘤大多能正確定位。
6、放射性核素標記碘化膽固醇腎上腺掃描 正常腎上腺顯影較淡且對稱,部分人不顯像。皮質增生時兩側腎上腺顯像對稱但濃集。皮質腺瘤或腺癌則腺瘤側腎上腺放射性濃集,對側不顯像。部分腺癌病例腫瘤顯像;部分腺癌病例腫瘤不顯像,可能是每單位重量的腫瘤組織為低功能性分泌激素,每單位重量的組織攝取膽固醇較少,致使放射性不濃集。本法也適用於手術後殘留腎上腺組織、移植的腎上腺組織的測定和尋找迷走的腎上腺組織。
7、腎上腺血管造影 引起皮質醇症的腎上腺皮質腫瘤一般較小,血供也不豐富,故一般不做腎上腺血管造影和經靜脈導管採取血樣測定皮質醇。但也有用選擇性腎上腺動脈或靜脈造影顯示腎上腺皮質腺瘤的報導。凡其它方法不能定位的腺瘤,尤其是皮質腺癌、可選用腎上腺血管造影的方法明確診斷。
檢查方法
患者血紅蛋白、紅細胞計數略升高,白細胞略增多,中性粒細胞百分數偏高,淋巴細胞偏低,嗜酸細胞直接計數<50/mm3。
部分病例血鈉增高,鉀降低,氯降低並鹼中毒。大部分病例葡萄糖耐量試驗呈糖尿病曲線,部分病例空腹血糖升高或並有糖尿。 血漿皮質醇的分泌有明顯的晝夜變化:於清晨達最高峰(10±2.1μg/dl),以後逐漸下降,下午4時均值約4.7±1.9μg/dl,晚上入睡前至最低水平。若每4小時測定1次血漿皮質醇濃度並標在座標上連成一曲線,應呈V型。而皮質醇症時其血漿濃度可>30μg/dl,並失去V型的變化曲線規律。
尿中17羥皮質醇類固醇均超過正常值(正常值男性5~15mg/24h,女性4~10mg/24h)。 尿中17酮類固醇可正常或略升高。如有顯著增高,甚至>50mg/24h,應注意有癌腫可能(正常值男性6~18mg/24h, 女性4~13mg/24h)。
治療方法
一、手術療法
1、垂體腫瘤摘除 適用於由垂體腫瘤所致的雙側腎上腺皮質增生,尤
其伴有視神經受壓症状的病例更為適宜。但手術常不能徹底切除腫瘤,並可影響垂體其它的內分泌功能。如手術切除不徹底或不能切除者,可作垂體放射治療。如出現垂體功能不足者應補充必要量的激素。由垂體微腺瘤引起的雙側腎上腺皮質增生可通過鼻腔經蝶骨藉助於顯微外科技術作選擇性垂體微腺瘤切除。手術創傷小,不影響垂體功能,而且屬病因治療,故效果好。此法已被廣泛採用。如微腺瘤切除不徹底,則術後病情不緩解;如微腺瘤為下丘腦依賴性的,術後可能會複發。
2、腎上腺皮質腫瘤摘除 適用於腎上腺皮質腺瘤及腎上腺皮質腺癌。如能明確定位,可經患側第11肋間切口進行。如不能明確定位,則需經腹部或背部切口探查雙側腎上腺。腎上腺皮質腺瘤摘除術較簡單,但腎上腺皮質腺癌者常不能達到根治。由於腫瘤以外的正常腎上腺呈萎縮狀態,故術前、術後均應補充皮質激素。術後尚可肌注ACTH20r/d,共2周,以促進萎縮的皮質功能恢復。術後激素的維持需達3個月以上,然後再逐步減量至停服。
3、雙側腎上腺摘除 適用於雙側腎上腺皮質增生病例。其方法有①雙側腎上腺全切除:優點是控制病情迅速,並可避免複發;缺點是術後要終身補充皮質激素,術後易發生Nelson症(垂體腫瘤+色素沉著)。②一側腎上腺全切除,另一側腎上腺次全切除:由於右側腎上腺緊貼下腔靜脈,如有殘留腎上腺增生複發,再次手術十分困難,故一般作右側腎上腺全切除。左側殘留腎上腺應佔全部腎上腺重量的5%左右。殘留過多,則複發率高。殘留過少或殘留腎上腺組織血供損傷,則出現腎上腺皮質功能不全或Nelson症。故術中應注意勿損傷其血供。由於腎上腺血供是呈梳狀通向其邊緣,故殘留的組織應是邊緣的一小片組織。有的作者採用一側腎上腺全切除加垂體放療,但常無效或有複發。
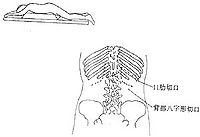
在作腎上腺手術時,應注意以下幾點:①切口的選擇:可經第11肋間切口進行,但術中需更換體位,部分腎上腺皮質腺瘤病人誤診為腎上腺皮質增生時,則發生困難。病人肥胖,經腹部探查雙側腎上腺較困難。比較合適的是病人全麻下取俯臥位,經背部八字切口(Nagamatsu切口(圖1),或經第11肋切口探查。一般先探查右側,如發現右側腎上腺增生(雙側腎上腺增生)或萎縮(左側腎上腺皮質腺瘤),則需再探查左側腎上腺。如發現右側腎上腺皮質腺瘤則可作腺瘤摘除,不需再探查左側。巨大的腎上腺腺癌可選用胸腹連合切口進行手術(圖2)。②皮質激素的補充:皮質醇症患者體內皮質醇分泌處於一高水平,術後皮質醇水平驟降易導致急性腎上腺皮質功能不足所致的危象。其臨床表現為休克、心率快、呼吸急促、紫紺、噁心嘔吐、腹痛、腹瀉、高熱、昏迷甚至死亡。故於術前、術中和術後均應補充皮質激素以預防。一旦危象發生,應快速靜脈補充皮質激素,糾正水電解質紊亂以及對症處理。情緒波動、感染以及某些手術併發症可誘發危象發生,並有時會混淆診斷(如氣胸、出血等),應予注意避免發生。
以上補充的皮質激素量雖已超過正常生理分泌量,但由於術前患者皮質醇分泌處於一很高水平,故部分病例仍可發生危象。由於術後危象大多發生於手術後2天之內,故我院於術日及術後2天再靜脈補充氫化可的松100~200mg/d, 從而使危象的發生大大減少。如疑有危象或有手術併發症,均應加大皮質激素用量。皮質激素的長期維持量是醋酸可的松25~37.5mg/d(為正常生理需要量)。腺瘤患者一般需維持3~6個月後停藥,雙側腎上腺全切除者需終生服藥。如病人有其它疾病、感染及拔牙等手術時,應增大激素用量。如有腹瀉及不能進食時,應改成肌注用藥。病人應隨身攜帶診斷書,隨時供醫生參考。腎上腺腺瘤及腎上腺大部切除患者在病情穩定後可逐步停藥。停藥前如需測定體內皮質醇分泌水平,可停服醋酸可的松,改服氟美松(0.75mg氟美松相當於25mg醋酸可的松)1~2周,再測24小時尿17羥、17酮的排出量。因氟美松不影響尿中17羥、17酮類固醇的測定,故所測得的17羥、17酮類固醇表示體內皮質醇的分泌水平。如已接近正常,則可逐步減量停藥。如水平極低,則仍繼續改服醋酸可的松維持。有作者報導將切除的腎上腺切成小塊,埋植在縫匠肌或腸系膜中治療手術後腎上腺皮質功能低下,獲得一定療效。經放射性核素標記膽固醇掃描證明移植區確有放射性濃集,尿17-羥類固醇排出量也有升高,部分病例可停服或減少皮質激素的維持量。如有皮質功能亢進者,可局部作一較小手術切除之。由於腎上腺動脈細小,帶血管的自體腎上腺移植有一定困難。③Nelson症的處理:腎上腺全切除後,垂體原有的腺瘤或微腺瘤可繼續增大,壓迫視神經,引起視力障礙。垂體分泌的促黑色素激素引起全身皮膚粘膜色素沉著,甚至呈古銅色。垂體腺瘤摘除術可以挽救視力,垂體局部放療可以抑制腫瘤的生長。中醫中藥對緩解色素沉著也有一定療效。
二、非手術療法
1、垂體放射治療 有20%病例可獲持久療效。但大多數病例療效差且易複發,故一般不作首選。垂體放療前必須確定腎上腺無腫瘤。
2、藥物治療 副作用大,療效不肯定。主要適用於無法切除的腎上腺皮質腺癌病例。①二氯二苯二氯乙烷(O,P´DDD,dichlorodiphenyldichloroethane):可使腎上腺皮質網狀帶和束狀帶細胞壞死。適用於已轉移和無法根治的功能性或無功能性的皮質癌。但有嚴重的胃腸道和神經系統的副作用,並可導致急性腎上腺皮質功能不足。治療劑量4~12g/d,從小劑量開始漸增到維持量,並根據病人忍受力和皮質功能情況調節。②甲吡酮(metyrapone,Su4885):是11β-羥化酶抑制劑。可抑制11-去氧皮質醇轉化為皮質醇、11-去氧皮質酮轉化為皮質酮,從而使皮質醇合成減少。副作用小,主要為消化道反應。但作用暫時,只能起緩解症状的作用。一旦皮質醇分泌減少刺激ACTH的分泌,可克服其阻斷作用。③氨基導眠能(aminoglutethimide):可抑制膽固醇合成孕烯醇酮。輕型腎上腺皮質增生症服1~1.5g/d,嚴重者1.5~2g/d可控制症状。但需密切隨訪皮質激素水平,必要時應補充小劑量的糖皮質激素和鹽皮質激素,以免發生腎上腺皮質功能不足現象。④賽庚啶(cyproheptadine):是血清素(serotonin)的競爭劑,而血清素可興奮丘腦-垂體軸而釋放ACTH,故賽庚啶可抑制垂體分泌ACTH。適用於雙側腎上腺增生病例的治療。劑量由8mg/d逐漸增加到24mg/d。在雙側腎上腺全切除或次全切除術後皮質功能不足的情況下,一方面補充皮質激素,一方面服用賽庚啶能減少垂體瘤的發生機會。其它尚報告溴隱亭、腈環氧雄烷(trilostane)等藥物亦有一定療效。
鑒別
一、單純性肥胖及2型糖尿病:可有肥胖、高血壓、糖代謝異常、月經紊亂、皮膚白紋等,血尿皮質醇及其代謝產物增高,但可被小劑量地塞米松所抑制,皮質醇及ACTH節律正常。
二、假性Cushing症候群:酒精性肝臟損害時,不僅各種症状及激素水平類似本病,且對小劑量地塞米松給藥無反應或反應減弱,但戒酒即可恢復。
三、抑鬱症:雖增高的激素及其代謝物不受地塞米松小劑量給藥抑制,但無Chushing症候群的臨床表現。
預防
病情觀察
1、肥胖狀態,高血壓。
2、皮膚乾燥、皮下出血、痤瘡、創傷化膿、四肢末梢紫紺、水腫、多毛、肌力低下、乏力、疲勞感、骨質疏鬆與病理性骨折等。
4、精神症状失眠、不安、抑鬱、興奮。
5、感染症状發熱。
6、女性患者月經異常等。
庫欣症候群是1921年由庫欣發現的,故而得名。英文: Cushing's Syndrome。
為各種病因造成腎上腺分泌過多糖皮質激素(主要是皮質醇)所致病症的總稱,其中最多見者為垂體促腎上腺皮質激素(ACTH)分泌亢進所引起的臨床類型,因此又稱為皮質醇增多症。
男女之比約為1:5。
高血壓是常見症状,庫欣症候群約80%的病人有高血壓。收縮壓和舒張壓可達到2級高血壓水平,且為持續性升高。
特點
辨別庫欣症候群其實很容易,患者體型改變極有特點:
1、向心性肥胖,呈現出向心性肥胖,即軀幹肥而四肢瘦;
2、滿月臉,面如滿月,且紅潤多脂;
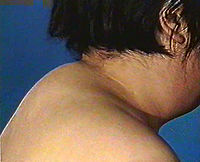
3、水牛背,背部是「水牛背」模樣,腹部懸垂;
4、紫紋,另外還有紫紋,紫紋多見於腹壁、大腿內外側、臀部的皮膚;
5、性方面,性功能減退,男性陽痿、睾丸變軟,女性月經減少、閉經、不育、多毛;
6、骨骼系統,可見骨質疏鬆,出現腰背痛、脊柱壓縮性骨折,後期可因椎體塌陷而成駝背。
病因
庫欣症候群按其病因和垂體、腎上腺的病理改變不同可分成下列三種:
醫源性皮質醇症
長期大量使用糖皮質激素治療某些疾病可出現皮質醇症的臨床表現,這在臨床上十分常見。這是由外源性激素造成的,停藥後可逐漸復原。但長期大量應用糖皮質激素可反饋抑制垂體分泌ACTH,造成腎上腺皮質萎縮,一旦急驟停藥,可導致一系列皮質功能不足的表現,甚至發生危象,故應予注意。長期使用ACTH也可出現皮質醇症。
垂體性雙側腎上腺皮質增生
雙側腎上腺皮質增生是由於垂體分泌ACTH過多引起。其原因:①垂體腫瘤。多見嗜鹼細胞瘤,也可見於嫌色細胞瘤;②垂體無明顯腫瘤,但分泌ACTH增多。一般認為是由於下丘腦分泌過量促腎上腺皮質激素釋放因子(CRF)所致。臨床上能查到垂體有腫瘤的僅佔10%左右。這類病例由於垂體分泌ACTH已達一反常的高水平,血漿皮質醇的增高不足以引起正常的反饋抑制,但口服大劑量氟美松仍可有抑制作用。
垂體外病變引起的雙側腎上腺皮質增生 支氣管肺癌(尤其是燕麥細胞癌)、甲狀腺癌、胸腺癌、鼻咽癌及起源於神經嵴組織的腫瘤有時可分泌一種類似ACTH的物質,具有類似ACTH的生物效應,從而引起雙側腎上腺皮質增生,故稱異源性ACTH症候群。這類患者還常有明顯的肌萎縮和低血鉀症。病灶分泌ACTH類物質是自主的,口服大劑量氟美松無抑制作用。病灶切除或治癒後,病症即漸可消退。
腎上腺皮質腫瘤
大多為良性的腎上腺皮質腺瘤,少數為惡性的腺癌。腫瘤的生長和分泌腎上腺皮質激素是自主性的,不受ACTH的控制。由於腫瘤分泌了大量的皮質激素,反饋抑制了垂體的分泌功能,使血漿ACTH濃度降低,從而使非腫瘤部分的正常腎上腺皮質明顯萎縮。此類患者無論是給予ACTH興奮或大劑量氟美松抑制,皮質醇的分泌量不會改變。腎上腺皮質腫瘤尤其是惡性腫瘤時,尿中17酮類固醇常有顯著增高。
腎上腺皮質腫瘤多為單個良性腺瘤,直徑一般小於3~4cm,色棕黃,有完整的包膜。瘤細胞形態和排列與腎上腺皮質細胞相似。腺癌則常較大,魚肉狀,有浸潤或蔓延到周圍臟器,常有淋巴結和遠處轉移。細胞呈惡性細胞特徵。 無內分泌功能的腎上腺皮質腫瘤則不導致皮質醇症。
臨床上發現少數病例腎上腺呈結節狀增生,屬增生與腺瘤的中間型。患者血漿ACTH可呈降低,大劑量氟美松無抑制作用。
臨床上70%的病例為垂體病變所致的雙側腎上腺皮質增生,良性腺瘤佔20~30%,惡性腎上腺腺癌佔5~10%,異位ACTH分泌過多則甚為少見。
臨床表現
脂肪代謝障礙:特徵性表現為向心性肥胖--滿月臉、水牛背、球形腹,但四肢瘦小。
蛋白質代謝障礙:大量皮質醇促進蛋白質分解,抑制蛋白質合成,形成負氮平衡狀態。病人因蛋白質過度消耗而表現的皮膚菲薄,毛細血管脆性增加,呈現典型的皮膚紫紋。
糖代謝障礙:表現為血糖升高,糖耐量降低。
電解質紊亂:大量皮質醇有瀦鈉,排鉀作用。病人表現為輕度水腫或低鉀血症
心血管病變:高血壓
神經精神障礙:病人易出現不同程度的激動,煩躁,失眠,抑鬱,妄想等神經精神的改變
臨床診斷
庫欣症候群的診斷分三個面:確定疾病診斷、病因診斷和定位診斷。
確定疾病診斷
確定疾病診斷主要依典型的臨床症状和體征。如向心性肥胖、紫紋、毛髮增多、性功能障礙、疲乏等。加上尿17羥皮質類固醇排出量顯著增高,小劑量氟美松抑制試驗不能被抑制和血11羥皮質類固醇高於正常水平並失去晝夜變化節律即可確診為皮質醇症。早期輕型的病例應與單純性肥胖相鑒別。小劑量氟美松試驗:服用小劑量氟美松不影響尿中17羥類固醇的測定,但可反饋抑制垂體分泌ACTH。方法是連續6天測定24小時尿中17羥皮質類固醇的排出量,在第3~4天每天口服氟美松0.75mg每8小時1次。將每天測出的值在座標上標出並連成曲線。正常人用藥後2天尿中17羥皮質類固醇的排出量比用藥前明顯減低,如其下降在一半以上則說明有明顯抑制,屬正常。反之降低不明顯或不超過50%,則為皮質醇症。
病因診斷
病因診斷即區別是由腎上腺皮質腺瘤、腺癌、垂體腫瘤引起的皮質增生、非垂體腫瘤或異源性ACTH分泌腫瘤引起的皮質增生。
其它影像學診斷方法
腎上腺正常,部分垂體有占痊
患側腎上腺佔位
患側腎上腺佔位
腎上腺正常,可能發現分泌異源ACTH的病灶1、蝶鞍的X線學診斷 垂體腫瘤可引起視神經受壓而出現顳側偏盲。在蝶鞍X線點片上可見鞍底、鞍背骨質疏鬆脫鈣,前後突吸收,蝶鞍擴大。分層片或cT則可顯示更小的垂體腫瘤。這種由垂體腫瘤引起繼發性腎上腺皮質增生者約佔皮質醇症的10%。
2、ACTH興奮試驗 腎上腺皮質增生者 對ACTH的刺激仍有明顯反應。其方法同小劑量氟美松試驗,但在第3~4天每天由靜脈滴 入ACTH20u(加入5%葡萄糖液500~1000ml 內,8小時滴完)。腎上腺皮質增生時,注射 ACTH後2天的24小時尿17羥皮質類固醇的排 出量比注射前增高50%以上,血中嗜伊紅細胞計數常同時下降80~90%。腎上腺皮質增生伴有小腺瘤或結節狀皮質增生時,ACTH抑制試驗的反應和增生相似,但有時較弱或不明顯。腎上腺皮質腫瘤時,因正常腎上腺皮質處於萎縮狀態,故不起反應或反應很弱。但病程短,尤其小腺瘤或發展迅速的皮質癌,因腫瘤外的腎上腺皮質尚未萎縮,對此試驗仍有較明顯的反應。異源性ACTH分泌腫瘤因腫瘤大量分泌ACTH,腎上腺皮質已處於持久的高興奮狀態,故對此試驗也不起反應。
3、大劑量氟美松抑制試驗 方法與小劑量氟美松試驗相同,但第3~4天每6小時服氟美松2mg。服藥後尿24小時17羥皮質類固醇排出量比服藥前減少50%以上為陽性反應。異源ACTH分泌腫瘤、皮質腺瘤、皮質腺癌的分泌功能均是自主性的,對此試驗均不起反應。而皮質增生者則可有明顯抑制呈陽性反應。皮質增生伴小腺瘤或結節性增生者儘管ACTH興奮試驗可陽性,但大劑量氟美松卻不能抑制其分泌(即興奮得起,但抑制不下)。此時需作其它試驗來區別是皮質腫瘤還是增生。
4、甲吡酮(雙吡啶異丙酮、甲雙吡丙酮、Su4885)試驗 甲吡酮抑制11β-羥化酶而使11-去氧皮質酮轉變為皮質酮及11-去氧皮質醇轉變成皮質醇的過程受阻,使血漿皮質醇降低,從而反饋抑制減弱,促使垂體分泌大量ACTH。血漿ACTH增高(正常值上午8~10時<100pg/ml),11-去氧皮質醇的合成增多。11-去氧皮質醇包括在17羥及17酮皮質類固醇的測定範圍內,因此尿中17羥及17酮皮質類固醇的排出量也增多。故此試驗可測定垂體分泌ACTH的儲備能力。皮質增生時,甲吡酮試驗呈陽性反應;而皮質腫瘤時,因腫瘤自主地大量分泌皮質醇,抑制了垂體分泌ACTH的能力,甲吡酮的興奮作用不能顯示出來。而垂體腺瘤所致的皮質醇症時,垂體能自主大量分泌ACTH,故也呈陰性反應。
5、加壓素試驗 加壓素有類似CRF的作用,故可用以測定垂體分泌ACTH的儲備功能。皮質增生者呈陽性反應(血ACTH及尿17羥皮質類固醇排多量均增加)。皮質腫瘤者呈陰性反應。加壓素可引起冠狀動脈收縮,故老年、冠心病病人不宜試用。
如ACTH、甲吡酮、加壓素三個試驗均呈無反應,則可能是腎上腺皮質癌;三試驗均為陽性反應時,為皮質增生。
定位診斷
定位診斷主要是腎上腺皮質腫瘤的定位,以利手術切除。但定位的同時,也常解決了病因診斷。1、X線胸片 可除外肺癌和肺轉移灶。
2、靜脈腎盂造影 了解雙腎情況。較大的腎上腺腫瘤可將患側腎臟向下推移。
3、腹膜後充氣造影 由於腎上腺皮質腺瘤一般不太大,且肥胖病人腹膜後大塊狀脂肪組織常可導致誤診,現已少用。
4、B超 方便有效。對腎上腺皮質腫瘤的定位診斷的正確率可達90%以上。
5、CT對直徑0.5~1cm以上的腎上腺皮質腺瘤大多能正確定位。
6、放射性核素標記碘化膽固醇腎上腺掃描 正常腎上腺顯影較淡且對稱,部分人不顯像。皮質增生時兩側腎上腺顯像對稱但濃集。皮質腺瘤或腺癌則腺瘤側腎上腺放射性濃集,對側不顯像。部分腺癌病例腫瘤顯像;部分腺癌病例腫瘤不顯像,可能是每單位重量的腫瘤組織為低功能性分泌激素,每單位重量的組織攝取膽固醇較少,致使放射性不濃集。本法也適用於手術後殘留腎上腺組織、移植的腎上腺組織的測定和尋找迷走的腎上腺組織。
7、腎上腺血管造影 引起皮質醇症的腎上腺皮質腫瘤一般較小,血供也不豐富,故一般不做腎上腺血管造影和經靜脈導管採取血樣測定皮質醇。但也有用選擇性腎上腺動脈或靜脈造影顯示腎上腺皮質腺瘤的報導。凡其它方法不能定位的腺瘤,尤其是皮質腺癌、可選用腎上腺血管造影的方法明確診斷。
檢查方法
患者血紅蛋白、紅細胞計數略升高,白細胞略增多,中性粒細胞百分數偏高,淋巴細胞偏低,嗜酸細胞直接計數<50/mm3。 部分病例血鈉增高,鉀降低,氯降低並鹼中毒。大部分病例葡萄糖耐量試驗呈糖尿病曲線,部分病例空腹血糖升高或並有糖尿。 血漿皮質醇的分泌有明顯的晝夜變化:於清晨達最高峰(10±2.1μg/dl),以後逐漸下降,下午4時均值約4.7±1.9μg/dl,晚上入睡前至最低水平。若每4小時測定1次血漿皮質醇濃度並標在座標上連成一曲線,應呈V型。而皮質醇症時其血漿濃度可>30μg/dl,並失去V型的變化曲線規律。
尿中17羥皮質醇類固醇均超過正常值(正常值男性5~15mg/24h,女性4~10mg/24h)。 尿中17酮類固醇可正常或略升高。如有顯著增高,甚至>50mg/24h,應注意有癌腫可能(正常值男性6~18mg/24h, 女性4~13mg/24h)。
治療方法
一、手術療法
1、垂體腫瘤摘除 適用於由垂體腫瘤所致的雙側腎上腺皮質增生,尤其伴有視神經受壓症状的病例更為適宜。但手術常不能徹底切除腫瘤,並可影響垂體其它的內分泌功能。如手術切除不徹底或不能切除者,可作垂體放射治療。如出現垂體功能不足者應補充必要量的激素。由垂體微腺瘤引起的雙側腎上腺皮質增生可通過鼻腔經蝶骨藉助於顯微外科技術作選擇性垂體微腺瘤切除。手術創傷小,不影響垂體功能,而且屬病因治療,故效果好。此法已被廣泛採用。如微腺瘤切除不徹底,則術後病情不緩解;如微腺瘤為下丘腦依賴性的,術後可能會複發。
2、腎上腺皮質腫瘤摘除 適用於腎上腺皮質腺瘤及腎上腺皮質腺癌。如能明確定位,可經患側第11肋間切口進行。如不能明確定位,則需經腹部或背部切口探查雙側腎上腺。腎上腺皮質腺瘤摘除術較簡單,但腎上腺皮質腺癌者常不能達到根治。由於腫瘤以外的正常腎上腺呈萎縮狀態,故術前、術後均應補充皮質激素。術後尚可肌注ACTH20r/d,共2周,以促進萎縮的皮質功能恢復。術後激素的維持需達3個月以上,然後再逐步減量至停服。
3、雙側腎上腺摘除 適用於雙側腎上腺皮質增生病例。其方法有①雙側腎上腺全切除:優點是控制病情迅速,並可避免複發;缺點是術後要終身補充皮質激素,術後易發生Nelson症(垂體腫瘤+色素沉著)。②一側腎上腺全切除,另一側腎上腺次全切除:由於右側腎上腺緊貼下腔靜脈,如有殘留腎上腺增生複發,再次手術十分困難,故一般作右側腎上腺全切除。左側殘留腎上腺應佔全部腎上腺重量的5%左右。殘留過多,則複發率高。殘留過少或殘留腎上腺組織血供損傷,則出現腎上腺皮質功能不全或Nelson症。故術中應注意勿損傷其血供。由於腎上腺血供是呈梳狀通向其邊緣,故殘留的組織應是邊緣的一小片組織。有的作者採用一側腎上腺全切除加垂體放療,但常無效或有複發。
在作腎上腺手術時,應注意以下幾點:①切口的選擇:可經第11肋間切口進行,但術中需更換體位,部分腎上腺皮質腺瘤病人誤診為腎上腺皮質增生時,則發生困難。病人肥胖,經腹部探查雙側腎上腺較困難。比較合適的是病人全麻下取俯臥位,經背部八字切口(Nagamatsu切口(圖1),或經第11肋切口探查。一般先探查右側,如發現右側腎上腺增生(雙側腎上腺增生)或萎縮(左側腎上腺皮質腺瘤),則需再探查左側腎上腺。如發現右側腎上腺皮質腺瘤則可作腺瘤摘除,不需再探查左側。巨大的腎上腺腺癌可選用胸腹連合切口進行手術(圖2)。②皮質激素的補充:皮質醇症患者體內皮質醇分泌處於一高水平,術後皮質醇水平驟降易導致急性腎上腺皮質功能不足所致的危象。其臨床表現為休克、心率快、呼吸急促、紫紺、噁心嘔吐、腹痛、腹瀉、高熱、昏迷甚至死亡。故於術前、術中和術後均應補充皮質激素以預防。一旦危象發生,應快速靜脈補充皮質激素,糾正水電解質紊亂以及對症處理。情緒波動、感染以及某些手術併發症可誘發危象發生,並有時會混淆診斷(如氣胸、出血等),應予注意避免發生。
以上補充的皮質激素量雖已超過正常生理分泌量,但由於術前患者皮質醇分泌處於一很高水平,故部分病例仍可發生危象。由於術後危象大多發生於手術後2天之內,故我院於術日及術後2天再靜脈補充氫化可的松100~200mg/d, 從而使危象的發生大大減少。如疑有危象或有手術併發症,均應加大皮質激素用量。皮質激素的長期維持量是醋酸可的松25~37.5mg/d(為正常生理需要量)。腺瘤患者一般需維持3~6個月後停藥,雙側腎上腺全切除者需終生服藥。如病人有其它疾病、感染及拔牙等手術時,應增大激素用量。如有腹瀉及不能進食時,應改成肌注用藥。病人應隨身攜帶診斷書,隨時供醫生參考。腎上腺腺瘤及腎上腺大部切除患者在病情穩定後可逐步停藥。停藥前如需測定體內皮質醇分泌水平,可停服醋酸可的松,改服氟美松(0.75mg氟美松相當於25mg醋酸可的松)1~2周,再測24小時尿17羥、17酮的排出量。因氟美松不影響尿中17羥、17酮類固醇的測定,故所測得的17羥、17酮類固醇表示體內皮質醇的分泌水平。如已接近正常,則可逐步減量停藥。如水平極低,則仍繼續改服醋酸可的松維持。有作者報導將切除的腎上腺切成小塊,埋植在縫匠肌或腸系膜中治療手術後腎上腺皮質功能低下,獲得一定療效。經放射性核素標記膽固醇掃描證明移植區確有放射性濃集,尿17-羥類固醇排出量也有升高,部分病例可停服或減少皮質激素的維持量。如有皮質功能亢進者,可局部作一較小手術切除之。由於腎上腺動脈細小,帶血管的自體腎上腺移植有一定困難。③Nelson症的處理:腎上腺全切除後,垂體原有的腺瘤或微腺瘤可繼續增大,壓迫視神經,引起視力障礙。垂體分泌的促黑色素激素引起全身皮膚粘膜色素沉著,甚至呈古銅色。垂體腺瘤摘除術可以挽救視力,垂體局部放療可以抑制腫瘤的生長。中醫中藥對緩解色素沉著也有一定療效。
二、非手術療法
1、垂體放射治療 有20%病例可獲持久療效。但大多數病例療效差且易複發,故一般不作首選。垂體放療前必須確定腎上腺無腫瘤。
2、藥物治療 副作用大,療效不肯定。主要適用於無法切除的腎上腺皮質腺癌病例。①二氯二苯二氯乙烷(O,P´DDD,dichlorodiphenyldichloroethane):可使腎上腺皮質網狀帶和束狀帶細胞壞死。適用於已轉移和無法根治的功能性或無功能性的皮質癌。但有嚴重的胃腸道和神經系統的副作用,並可導致急性腎上腺皮質功能不足。治療劑量4~12g/d,從小劑量開始漸增到維持量,並根據病人忍受力和皮質功能情況調節。②甲吡酮(metyrapone,Su4885):是11β-羥化酶抑制劑。可抑制11-去氧皮質醇轉化為皮質醇、11-去氧皮質酮轉化為皮質酮,從而使皮質醇合成減少。副作用小,主要為消化道反應。但作用暫時,只能起緩解症状的作用。一旦皮質醇分泌減少刺激ACTH的分泌,可克服其阻斷作用。③氨基導眠能(aminoglutethimide):可抑制膽固醇合成孕烯醇酮。輕型腎上腺皮質增生症服1~1.5g/d,嚴重者1.5~2g/d可控制症状。但需密切隨訪皮質激素水平,必要時應補充小劑量的糖皮質激素和鹽皮質激素,以免發生腎上腺皮質功能不足現象。④賽庚啶(cyproheptadine):是血清素(serotonin)的競爭劑,而血清素可興奮丘腦-垂體軸而釋放ACTH,故賽庚啶可抑制垂體分泌ACTH。適用於雙側腎上腺增生病例的治療。劑量由8mg/d逐漸增加到24mg/d。在雙側腎上腺全切除或次全切除術後皮質功能不足的情況下,一方面補充皮質激素,一方面服用賽庚啶能減少垂體瘤的發生機會。其它尚報告溴隱亭、腈環氧雄烷(trilostane)等藥物亦有一定療效。
鑒別
一、單純性肥胖及2型糖尿病:可有肥胖、高血壓、糖代謝異常、月經紊亂、皮膚白紋等,血尿皮質醇及其代謝產物增高,但可被小劑量地塞米松所抑制,皮質醇及ACTH節律正常。
二、假性Cushing症候群:酒精性肝臟損害時,不僅各種症状及激素水平類似本病,且對小劑量地塞米松給藥無反應或反應減弱,但戒酒即可恢復。
三、抑鬱症:雖增高的激素及其代謝物不受地塞米松小劑量給藥抑制,但無Chushing症候群的臨床表現。
預防
病情觀察
1、肥胖狀態,高血壓。
2、皮膚乾燥、皮下出血、痤瘡、創傷化膿、四肢末梢紫紺、水腫、多毛、肌力低下、乏力、疲勞感、骨質疏鬆與病理性骨折等。
3、尿量,尿性狀血尿、蛋白尿、尿糖。
4、精神症状失眠、不安、抑鬱、興奮。
5、感染症状發熱。
6、女性患者月經異常等。
對症護理
1、預防感染,保持皮膚清潔,勤沐浴,換衣褲,保持床單位的平整清潔。做好口腔、會陰護理。
2、觀察精神症状與防止發生事故。患者煩躁不安,異常興奮或抑鬱狀態時,要注意嚴加看護,防止墜床,用床檔或用約束帶保護患者,不宜在患者身邊放置危險品,避免刺激性言行,耐心仔細,應多關心照顧。
3、腎上腺癌化療的患者觀察有無噁心、嘔吐、嗜睡、運動失調和記憶減退。
4、每周測量身高、體重,預防脊柱突發性壓縮性骨折。
5、正確無誤做好各項試驗,及時送驗。
一般護理
1、臥床休息,輕者可適當活動。
2、飲食宜給予高蛋白、高維生素、低脂、低鈉、高鉀的食物,每餐不宜過多或過少,要均勻進餐。
健康指導
1、指導患者在日常生活中,要注意預防感染,皮膚保持清潔,防止外傷,骨折。
2、指導患者正確地攝取營養平衡的飲食,給予低鈉、高鉀、高蛋白的食物。
3、遵醫囑服用藥,不擅自減藥或停藥。
4、定期門診隨訪。
參看
| 關於「庫欣症候群」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |