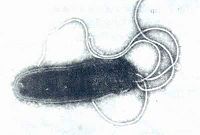
幽門螺桿菌
| A+醫學百科 >> 幽門螺桿菌 |
幽門螺桿菌,Helicobacter pylori,簡稱Hp。首先由巴里.馬歇爾(Barry J. Marshall)和羅賓.沃倫(J. Robin Warren)二人發現,此二人因此獲得2005年的諾貝爾生理學或醫學獎
目錄 |
特徵
形態學特徵
幽門螺桿菌是一種單極、多鞭毛、末端鈍圓、螺旋形彎曲的細菌。長2.5~4.0μm,寬0.5~1.0μm。革蘭染色陰性。有動力。在胃粘膜上皮細胞表面常呈典型的螺旋狀或弧形。在固體培養基上生長時,除典型的形態外,有時可出現桿狀或圓球狀。
電子顯微鏡下,菌體的一端可伸出2~6條帶鞘的鞭毛。在分裂時,兩端均可見鞭毛。鞭毛長約為菌體1~1.5倍。粗約為30nm。鞭毛的頂端有時可見一球狀物,實為鞘的延伸物。每一鞭毛根部均可見一個圓球狀根基伸入菌體頂端細胞壁內側。在其內側尚有一電子密度降低區域。。鞭毛在運動中起推進器作用,在定居過程中起拋錨作用。
生理學和分子生物學特徵
幽門螺桿菌是微需氧菌,環境氧要求5~8%,在大氣或絕對厭氧環境下不能生長。許多固體培養基可作幽門螺桿菌分離培養的基礎培養基,布氏瓊脂使用較多,但需加用適量全血或胎牛血清作為補充物方能生長。常以萬古黴素、TMP、兩性黴素B等組成抑菌劑防止雜菌生長。
幽門螺桿菌對臨床微生物實驗中常用於鑒定腸道細菌的大多數經典生化實驗不起反應。而氧化酶、觸酶、尿素酶、鹼性磷酸酶、r-谷氨醯轉肽酶、亮氨酸肽酶這七種酶反應是作為幽門螺桿菌生化鑒定的依據。
幽門螺桿菌的全基因序列已經測出,其中尿素酶基因有四個開放性讀框,分別是UreA、 UreB、 UreC 和UreD。UreA和UreB編碼的多肽與尿素酶結構的兩個亞單位結構相當。幽門螺桿菌的尿素酶極為豐富,約含菌體蛋白的15%,活性相當於變形桿菌的400倍。尿素酶催化尿素水解形成氨雲保護細菌在高酸環境下生存。此外,尚有VacA基因和CagA基因,分別編碼空泡毒素和細胞毒素相關蛋白。根據這兩種基因的表達情況,又將幽門螺桿菌菌株分成兩種主要類型:Ⅰ型含有CagA和VacA基因並表達兩種蛋白,Ⅱ型不含CagA基因,不表達兩種蛋白,尚有一些為中間表達型,即表達其中一種毒力因子。現在多認為Ⅰ型與胃疾病關係較為密切。
培養
用於培養的胃粘膜活檢標本應置於生理鹽水、營養肉湯或20%葡萄糖中,然後立即轉送到細菌室培養。如果標本不能在4個小時內培養,就應放在4。C保存,但不宜超過24小時。長期保存用於培養的活檢標本的唯一方法是將其置於-70。C或液氮之中。
培養幽門螺桿菌的培養基包括非選擇性及選擇性兩種。常用的非選擇性培養基基礎為腦心浸液瓊脂、哥倫比亞瓊脂、胰蛋白腖大豆瓊脂以及Wilkins-Chalgren瓊脂。培養基中需加7%-10%的去纖維蛋白馬血。羊血、人血、馬血清、氯化血紅素、澱粉、膽固醇或環糊精(cyclodextrins) 也可代替馬血。選擇培養基則是在上述 培養基中添加一定的抗菌藥物,如萬古黴素、啶酸、二性黴素B、多粘菌素B以及甲氧苄氨嘧啶(TMP)。常用的有Skirrow 配方及Dent 配方。前者原用於彎麴菌的培養,亦可用於幽門螺桿菌培養。後者為前者的改良,即將多粘菌素用頭孢磺啶取代,因為少數(5%左右)幽門螺桿菌菌株對多粘菌素敏感。Drnt配方為萬古黴素(10mg/L)、頭孢磺啶(5mg/L)、TMP(5mg/L)以及二性黴素B(5mg/L)。有報導指出,部分菌株對啶酸敏感,因而培養基中應盡量避免作用該抗生素。
感染與致病機理
幽門螺桿菌感染是慢性活動性胃炎、消化性潰瘍、胃黏膜相關淋巴組織(MALT) 淋巴瘤和胃癌的主要致病因素。1994年世界衛生組織/國際癌症研究機構 (WHO/IARC) 將幽門螺桿菌定為Ⅰ類致癌原。
幽門螺桿菌感染
幽門螺桿菌進入胃後,藉助菌體一側的鞭毛提供動力穿過黏液層。研究表明,幽門螺桿菌在粘稠的環境下具有極強的運動能力,強動力性是幽門螺桿菌致病的重要因素。幽門螺桿菌到達上皮表面後,通過粘附素,牢牢地與上皮細胞連接在一起,避免隨食物一起被胃排空。並分泌過氧化物歧化酶(SOD)和過氧化氫酶,以保護其不受中性粒細胞的殺傷作用。幽門螺桿菌富含尿素酶,通過尿素酶水解尿素產生氨,在菌體周圍形成「氨雲」保護層,以抵抗胃酸的殺滅作用。
幽門螺桿菌與胃炎
正常情況下,胃壁有一系列完善的自我保護機制(胃酸、蛋白酶的分泌功能,不溶性與可溶性粘液層的保護作用,有規律的運動等),能抵禦經口而入的千百種微生物的侵襲。自從在胃粘膜上皮細胞表面發現了幽門螺桿菌以後,才認識到幽門螺桿菌幾乎是能夠突破這一天然屏障的唯一元凶。goodwin把幽門螺桿菌對胃粘膜屏障在破壞作用比喻作對「屋頂」的破壞給屋內造成災難那樣的後果,故稱為「屋漏」學說。目前對幽門螺桿菌感染的研究能歸入這一學說的資料最多。主要包括:①使幽門螺桿菌穿透粘液層在胃上皮細胞表面定居的因素;②對胃上皮細胞等起破壞作用的毒素因子;③各種炎症細胞及炎症介質;④免疫反應物質等。
這些因素構成幽門螺桿菌感染的基本病理變化,即各種類型的急、慢性胃炎。其中近年來得到最重要關注的是空泡毒素vaca、細胞毒素相關蛋白質caga,和尿素酶等的作用及其分子生物學研究。
幽門螺桿菌與消化性潰瘍
幽門螺桿菌感染明顯地增加了發生十二指腸和胃潰瘍的危險性。大約1/6 幽門螺桿菌感染者可能發生消化性潰瘍病。治療幽門螺桿菌感染可加速潰瘍的癒合和大大降低潰瘍的複發率。不用抑酸劑,單用抗幽門螺桿菌藥物治療,表明也能有效地治癒胃和十二指腸潰瘍。幽門螺桿菌感染已經與一些引起潰瘍病的原因找到了聯繫。例如:胃酸增加、十二指腸胃化生、粘膜屏障性質的改變、胃竇粘膜產生炎症代謝產物等。這些患者中的發現已在動物實驗中得到初步證明。實際上消化性潰瘍涉及幾個複雜的相互作用的機制。如細菌的毒力因素(vaca和caga等),宿主的反應性(例:如易感性的遺傳、十二指腸上皮的胃化生、粘膜屏障和炎症的相互作用、泌酸反應、神經調節作用)和環境因素(例如飲食、獲得感染的年齡)的綜合作用導致潰瘍的最後結果。過去臨床上對潰瘍的發生有一句諺語,叫「no acid,no ulcer」。現在,從現代理論來看,「no hp,no ulcer」應得到更多地強調。
消化性潰瘍(包括胃潰瘍和十二指腸球部潰瘍)病因,長期以來認為與遺傳、胃酸過多、膽汁返流、吸煙等多種因素有關,其中尤以胃酸被認為是發病的主要因素。近80年來,胃酸一直被認為是胃潰瘍形成的原因,所以,有了「無酸無潰瘍」的傳統說法。
消化性潰瘍的傳統治療方法是中和胃酸或抑制胃酸分泌。過去沿用鹼性藥物,目前常用Hz受體抑制劑或其他胃酸分泌抑制劑。應用這些抗酸抑酸藥物,確實有利於潰瘍的癒合,但是這些藥物有一共同缺點,一旦停藥,不久潰瘍便又複發。因此,有些病人要間斷性服藥,有的則需長期服用維持劑量。還有不少病人潰瘍病卻屢愈屢發。
通過胃液分析發現,十二指腸潰瘍病人,胃酸分泌過高;而胃潰瘍病人中胃酸分泌增加者僅16%,而許多病人胃酸分泌正常,有的甚至低於正常。由此可見胃酸分泌的多少,並非是胃潰瘍發病的重要因素,而胃粘膜防禦能力降低,使胃酸等攻擊作用相對增加,可能是形成胃潰瘍的主要原因。
幽門螺桿菌與胃癌
從近年來對幽門螺桿菌感染的大量研究中提出了許多幽門螺桿菌致胃癌的可能機制:①細菌的代謝產物直接轉化粘膜;②類同於病毒的致病機制,hp dna的某些片段轉移入宿主細胞,引起轉化;③幽門螺桿菌引起炎症反應,其本身具有基因毒性作用。在這些機制中,後者似乎與最廣泛的資料是一致的。
流行病學
流行病學研究表明幽門螺桿菌感染了世界範圍內一半以上的人口,其發病率各個國家不同,甚至同一國家的各個地區也不相同。目前已知發病率的高低與社會經濟水平,人口密集程度,公共衛生條件以及水源供應有較密切的關係。也有報導指出,幽門螺桿菌的感染有明顯的季節分布特徵,以7~8月份為高峰。在亞洲地區,中國內地、中國香港、越南、印度等少年幽門螺桿菌的感染率分別60%、50%、40%、70%。慢性胃炎患者的胃粘膜活檢標本中幽門螺桿菌檢出率可達80%~90%,而消化性潰瘍患者更高,可達95%以上,甚至接近100%。胃癌由於局部上皮細胞已發生異化,因此檢出率高低報導不一。在自然人群中初出生的新生兒血清中抗幽門螺桿菌-IgG水平很高,接近成人水平,可能從母體獲得被動免疫抗體之故。半年後迅速下降。在我國及大多數發展中國家中陽性率待降至10%~20%後又迅速回升。大約在10歲以後即迅速上升達到或接近成人陽性檢出率水平。
我國及大多數發展中國家人群幽門螺桿菌感染因地區有所不同。低達20%,高達90%,人群中總感染率高於已開發國家。這些基本資料說明了如下幾個問題:1、胃病患者中幽門螺桿菌檢出率遠高於人群中總的檢出率,這說明幽門螺桿菌感染者並不都得胃病。這可能還蘊藏著與致病有關的其他因素,特別是遺傳因素(宿主的易感性和菌株的型別差異等);2、人群中的幽門螺桿菌感染率與胃病的發生率,發展中國家高於已開發國家。這又與社會經濟、衛生狀況有關。特別是現已證明胃癌高發區不僅與該地區人群中幽門螺桿菌感染率高有關外,還與人群中幽門螺桿菌的早發感染有關;3、人類一旦感染幽門螺桿菌後,若不進行治療,幾乎終身處於持續感染中。因此感染率總的講來隨著年齡增長而增長。
目前多數學者認為「人-人」「糞-口」是主要的傳播方式和途徑,亦可通過內鏡傳播,而且幽門螺桿菌感染在家庭內有明顯的聚集現象。父母感染了幽門螺桿菌其子女的感染機會比其它家庭高得多。對感染幽門螺桿菌的家庭調查提示,有幽門螺桿菌感染者家庭中的「健康人」,幽門螺桿菌抗體陽性率為64%,明顯高於同年齡組無幽門螺桿菌感染患者家庭的「健康人」(13%)。
診斷方法
自1983年通過胃鏡取活檢標本分離培養成功以來,對幽門螺桿菌感染的診斷已發展出了許多方法,包括有細菌學、病理學、血清學、同位素示蹤、分子生物學等。但總的講來,從標本採集角度看,可以分為侵襲性和非侵襲性兩大類。
侵襲性方法主要指必需通過胃鏡取活檢標本檢查的方法,是目前消化病學科的常規方法。它包括細菌的分離培養和直接塗片、快速尿素酶試驗,藥敏試驗。
非侵襲性方法主要指不通過胃鏡取活檢標本診斷幽門螺桿菌標本感染的方法。這類方法包括血清學和同位素蹤兩大類。
最新檢查手段:
診斷工具:C-14呼氣檢測儀+呼氣檢測口袋。
只需要吹氣5分鐘外,無其他任何不適。
該方法使眾多高血壓、心臟病及對胃鏡過敏的患者避免了做胃鏡的不適感,是目前理想的檢測方法之一。
治療方法
幽門螺桿菌感染現在主要靠抗幽門螺桿菌藥物進行治療。儘管幽門螺桿菌在體外對許多抗菌藥物都很敏感,但是在體內用藥並不那樣如意。這是因為幽門螺桿菌主要寄生在粘液層下面,胃上皮細胞表面。注射途徑用藥,對它無作用,經口局部又因為胃酸環境.粘液層的屏障及胃的不斷排空作用,使藥效也大大地受到了限制。再加上有些藥長期應用易產生嚴重的副作用或耐藥菌株等問題。因此幽門螺桿菌感染引起的急慢性胃炎.消化性潰瘍等疾病,本來看起來很容易治療的問題,實際上效果並不總是很理想。何況目前缺乏合適的幽門螺桿菌感染的動物模型,可供幫助制訂有效的治療方案。因此目前的治療方案幾乎全憑臨床經驗制訂,有很大的局限性(因地區、人群的差異)。總的講來,目前不提倡用單一的抗菌藥物,因為它的治癒率較低,一般<20%,且易產生耐藥性。
治療方案的選擇原則是:①採用聯合用藥方法;②幽門螺桿菌的根除率>80%,最好在90%以上;③無明顯副作用,病人耐受性好;④病人經濟上可承受性。判斷幽門螺桿菌感染的治療效果應根據幽門螺桿菌的根除率,而不是清除率。根除是指治療終止後至少在一個月後,通過細菌學、病理組織學或同位素示蹤方法證實無細菌生長。
根除幽門螺桿菌前應先注意口腔衛生。可以先更換牙具,使用一段時間漱口水和抑菌牙膏,修復口腔問題如蛀牙,牙垢,牙結石等。
目前國內外常用的抗幽門螺桿菌藥物有羥氨苄青黴素、甲硝唑、克拉黴素、四環素、強力黴素、呋喃唑酮、有機膠態鉍劑(de-nol等)、胃得樂(胃速樂)、樂得胃、西皮氏粉和胃舒平等。潰瘍病患者尚可適當結合應用質子泵抑制劑或h2受體拮抗劑加上兩種抗菌素,或者質子泵抑制劑(如奧美拉唑)加上一種抗菌素。療程一般為兩個星期。由於治療幽門螺桿菌感染抗菌方案的廣泛應用,有可能擴大耐藥性問題的產生。因此,將來替換性的治療或預防策略,如疫苗預防或免疫治療的研究是值得重視的。
發現故事
1979年,病理學醫生Warren在慢性胃炎患者的胃竇黏膜組織切片上觀察到一種彎曲狀細菌,並且發現這種細菌鄰近的胃黏膜總是有炎症存在,因而意識到這種細菌和慢性胃炎可能有密切關係。
1981年,消化科臨床醫生Marshall與Warren合作,他們以100例接受胃鏡檢查及活檢的胃病患者為對象進行研究,證明這種細菌的存在確實與胃炎相關。此外他們還發現,這種細菌還存在於所有十二指腸潰瘍患者、大多數胃潰瘍患者和約一半胃癌患者的胃黏膜中。
經過多次失敗之後,1982年4月,Marshall終於從胃黏膜活檢樣本中成功培養和分離出了這種細菌。為了進一步證實這種細菌就是導致胃炎的罪魁禍首,Marshall和另一位醫生Morris不惜喝下含有這種細菌的培養液,結果大病一場。
基於這些結果,Marshall和Warren提出幽門螺桿菌涉及胃炎和消化性潰瘍的病因學。1984年4月號,他們的成果發表於在世界權威醫學期刊《柳葉刀》(lancet)上。成果一經發表,立刻在國際消化病學界引起了轟動,掀起了全世界的研究熱潮。世界各大藥廠陸續投巨資開發相關藥物,專業刊物《螺桿菌》雜誌應運而生,世界螺桿菌大會定期召開,有關螺桿菌的研究論文不計其數。通過人體試驗、抗生素治療和流行病學等研究,幽門螺桿菌在胃炎和胃潰瘍等疾病中所起的作用逐漸清晰,科學家對該病菌致病機理的認識也不斷深入。
2005年10月3日,瑞典卡羅林斯卡研究院宣布,2005年度諾貝爾生理學或醫學獎授予這兩位科學家以表彰他們發現了幽門螺桿菌以及這種細菌在胃炎和胃潰瘍等疾病中的作用。
發現意義
大量研究表明,超過90%的十二指腸潰瘍和80%左右的胃潰瘍,都是由幽門螺桿菌感染所導致的。目前,消化科醫生已經可以通過內窺鏡檢查和呼氣試驗等診斷幽門螺桿菌感染。抗生素的治療方法已被證明能夠根治胃潰瘍等疾病。幽門螺桿菌及其作用的發現,打破了當時已經流行多年的人們對胃炎和消化性潰瘍發病機理的錯誤認識,被譽為是消化病學研究領域的里程碑式的革命。由於他們的發現,潰瘍病從原先難以治癒反覆發作的慢性病,變成了一種採用短療程的抗生素和抑酸劑就可治癒的疾病,大幅度提高了胃潰瘍等患者獲得徹底治癒的機會,為改善人類生活質量作出了貢獻。
這一發現還啟發人們去研究微生物與其他慢性炎症疾病的關係。人類許多疾病都是慢性炎症性疾病,如局限性迴腸炎、潰瘍性結腸炎、類風濕性關節炎、動脈粥樣硬化。雖然這些研究目前尚沒有明確結論,但正如諾貝爾獎評審委員會所說:「幽門螺桿菌的發現加深了人類對慢性感染、炎症和癌症之間關係的認識。」
慢性胃病的元凶—幽門螺桿菌
慢性胃病是指慢性胃炎(淺表性胃炎和萎縮性胃炎)和潰瘍病(胃潰瘍和十二指腸潰瘍)。胃鏡普查證實,我國人群中慢性胃炎的發病率高達60%以上,潰瘍病的發病率為10%左右。
慢性胃病的發病原因一直不很清楚,故長期無理想的防治方法。1982年,澳大利亞學者馬歇爾觀察到胃粘膜中有一種叫幽門螺桿菌(簡稱HP)的細菌與慢性胃病發病有關。之後,國內外學者對此菌作了大量研究後發現:
(1)胃粘膜正常的志願者,口服HP混懸液可引起胃炎症状和病理改變。
(2)患慢性胃炎時HP檢出率很高,而胃粘膜正常者則不能檢出此菌。
(3)慢性胃炎患者血清中HP抗體明顯增高,胃液中可檢出抗HP免疫球蛋白,這表明HP是有致病性的抗原(病原體)。
(4)針對HP進行治療,可使慢性胃炎患者胃粘膜明顯改善。
(5)60%-80%的胃潰瘍和70%-100%的十二指腸潰瘍患者的胃竇部可檢出HP,血清學檢查證實,這些人血清HP抗體滴度較高。
(6)用傳統抗潰瘍藥物治療無效的難治性潰瘍,改用抗HP藥物治療後,大部分潰瘍能癒合。
(7)採用抗HP藥物治癒的潰瘍病複發率明顯降低。
(8)用HP感染恆河猴,能使之發生慢性胃炎,胃粘膜的病理改變與人類感染相似,即製備HP胃炎動物模型獲得了成功。以上說明,HP與慢性胃病有相關性是確鑿無疑的。
現在醫學界有以下共識:HP肯定是慢性胃炎的致病菌,與潰瘍病和胃癌關係也極為密切。即是說,HP是引發慢性胃病的元凶和罪魁禍首。
因此,對慢性胃病的治療,除使用傳統的藥物外,還應給予抗HP藥物。現認為治療此菌療效較好的藥物有:膠態次枸櫞酸鉍(亦名德諾)、阿莫西林、痢特靈和甲硝唑等。
幽門螺旋桿菌感染有哪些檢測方法
幽門螺旋桿菌感染的檢查方法很多,主要包括細菌的直接檢查、尿毒酶活性測定、免疫學檢測及聚合酶鏈反應等方法。
(1)細菌的直接檢查:是指通過胃鏡檢查鉗取胃粘膜(多為胃竇粘膜)作直接塗片、染色,組織切片染色及細菌培養來檢測幽門螺旋桿菌。其中胃粘膜細菌培養是診斷幽門螺旋桿菌最可靠的方法,可作為驗證其他診斷性試驗的「金標準」,同時又能進行藥敏試驗,指導臨床選用藥物。
(2)尿毒酶檢查:因為幽門螺旋桿菌是人胃內唯一能夠產生大量尿毒酶的細菌,故可通過檢測尿毒酶來診斷幽門螺旋桿菌感染。尿毒酶分解胃內尿毒生成氨和二氧化碳,使尿素濃度降低、氨濃度升高。基於此原理已發展了多種檢測方法:①胃活檢組織尿毒酶試驗;②呼吸試驗;③胃液尿素或尿素氮測定;④15N-尿素試驗。
(3)免疫學檢測:目前已有多種免疫學檢測方法,通過測定血清中的幽門螺旋桿菌抗體來檢測幽門螺旋桿菌感染,包括補體結合試驗、凝集試驗、被動血凝測定、免疫印跡技術和酶聯合吸附測定(ELISA)等。
(4)聚合酶鏈反應技術:正常胃粘膜很少檢出幽門螺旋桿菌(0~6%),慢性胃炎患者幽門螺旋桿菌的檢出率很高,約50%~80%,慢性活動性胃炎患者幽門螺旋桿菌檢出率則更高,達90%以上。
(5)C-14呼氣檢測儀+呼氣檢測口袋。
只需要吹氣5分鐘外,無其他任何不適。
該方法使眾多高血壓、心臟病及對胃鏡過敏的患者避免了做胃鏡的不適感,是目前理想的檢測方法之一。是目前檢測HP的醫學界的金標準.敏感性95%,特異性95%--100%
口氣重可能是感染幽門螺旋桿菌
感染幽門螺旋桿菌後可能導致口氣重,即口腔有異味,嚴重者往往還有一種特殊口腔異味,無論如何清潔,都無法去除。
此外,感染幽門螺旋桿菌後,可能使患胃癌的危險增加2.7至12倍。如果沒有幽門螺旋桿菌感染,至少有相當部分患者的胃癌不會發生。世界衛生組織下屬國際癌症研究所將幽門螺旋桿菌定為人類I類致癌原。而我國是幽門螺旋桿菌感染高發國家之一,作為慢性胃炎、消化性潰瘍和胃癌等主要病因,治療消化性潰瘍、預防胃癌的一個可行措施就是預防並根除幽門螺旋桿菌感染。由於早期胃癌患者大約80%沒有症状,少數患者即使有一些症状也是些非特異性表現,比如:食欲不振、早飽、腹部不適等,極易被當作消化性潰瘍或其他胃腸道疾病而忽視。
| 關於「幽門螺桿菌」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |