醫學微生物學/人類免疫缺陷病毒
| 醫學電子書 >> 《醫學微生物學》 >> 其他病毒 >> 人類免疫缺陷病毒 |
| 醫學微生物學 |
|
|
本病毒為愛滋病人(Aids)的病原體,系引起細胞病變的靈長類逆轉錄病毒之一,屬逆轉錄病科(Retroviridae)慢病毒亞科(Lentivirinae)。它於1983年 Montaginer 等首先從1例淋巴腺病症候群患者分離到,命名為淋巴腺病症候群相關病毒(LymphadenopathyAssociated Virus,LAS) 。隨後1984年國Gallo等從愛滋病人分離到逆轉錄病毒,命名為嗜人類T淋巴細胞病毒Ⅲ型(Human T Cell Lymphotropic Virus Type Ⅲ ,HTLV-Ⅲ),後來證明這二種病毒是一樣的。至1986年國際病毒命名委員統一稱為人類免疫缺陷病毒(Human Immunodificidncy Virus ,HIV) 。HIV主要型別為HIV-1和HIV-2,愛滋病大多由HIV-1引起。
目錄 |
一、生物學診斷
(一)形態結構
病毒呈球形,直徑100~120nm,電鏡下可見一緻密的圓錐狀核心,內含病毒RNA分子和酶(逆轉錄酶、整合酶、蛋白酶),病毒外層囊膜系雙層脂質蛋白膜,其中嵌有gp120和gp41,分別組成刺突和跨膜蛋白。囊膜內面為P17蛋白構成的衣殼,其內有核心蛋白(P24)包裹RNA(圖30-1)。
(二)基因結構及編碼蛋白的功能
HIV基因組長約9.2~9.7kb,含gag、Pol、env、3個結構基因,及至少6個調控基因(Tat Rev、Nef、Vif、VPU、Vpr)並在基因組的5′端和3′端各含長末端序列(圖30-2)。HIVLTR含順式調控序列,它們控制前病毒基因的表達。已證明在LTR有啟動子和增強子並含負調控區。
1.gag基因能編碼約500個胺基酸組成的聚合前體蛋白(P55),經蛋白酶水解形成P17,P24核蛋白,使RNA不受外界核酸酶破壞。
2.Pol基因編碼聚合酶前體蛋白(P34),經切割形成蛋白酶、整合酶、逆轉錄酶、核糖核酸酶H,均為病毒增殖所必需。
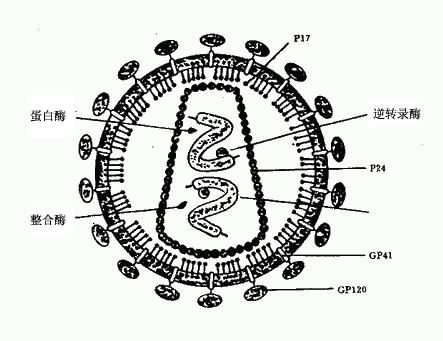
圖30-1 HIV結構示意圖
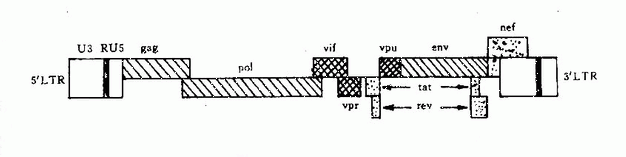
圖30-2 HIV基因組結構
3.env基因編碼約863個胺基酸的前體蛋白並糖基化成gp160,gp120和gp41。gp120含有中和抗原決定簇,已證明HIV中和抗原表位,在gp120 V3環上,V3環區是囊膜蛋白的重要功能區,在病毒與細胞融合中起重要作用。gp120與跨膜蛋白gp41以非共價鍵相連。gp41與靶細胞融合,促使病毒進入細胞內。實驗表明gp41亦有較強抗原性,能誘導產生抗體反應。
4.TaT 基因編碼蛋白(P14)可與LTR結合,以增加病毒所有基因轉錄率,也能在轉錄後促進病毒mRNA的翻譯。
5.Rev基因產物是一種順式激活因子,能對env和gag中順式作用抑制序(Cis-Actingrepression sequance,Crs) 去抑制作用,增強gag和env基因的表達,以合成相應的病毒結構蛋白。
6.Nef基因編碼蛋白P27對HIV基因的表達有負調控作用,以推遲病毒複製。該蛋白作用於HIv cDNA的LTR,抑制整合的病毒轉錄。可能是HIV在體內維持持續感集體所必需。
7.Vif基因對HIV並非必不可少,但可能影響游離HIV感染性、病毒體的產生和體內傳播。
8.VPU基因為HIV-1所特有,對HIV的有效複製及病毒體的裝配與成熟不可少。
9.Vpr基因編碼蛋白是一種弱的轉錄激活物,在體內繁殖周期中起一定作用。
HIV-2基因結構與HIV-1有差別:它不含VPU基因,但有一功能不明VPX基因。核酸雜交法檢查HIV-1與HIV-2的核苷酸序列,僅40%相同。env基因表達產物激發機體產生的抗體無交叉反應。
(三)培養特性
將病人自身外周或骨髓中淋巴細胞經PHA刺激48~72小時作體外培養(培養液中加IL2)1~2周後,病毒增殖可釋放至細胞外,並使細胞融合成多核巨細胞,最後細胞破潰死亡。亦可用傳代淋巴細胞系如HT-H9、Molt-4細胞作分離及傳代。
HIV動物感染範圍窄,僅黑猩猩和長劈猿,一般多用黑猩猩做實驗。用感染HIV細胞或無細胞的HIV濾液感染黑猩猩,或將感染HIV黑猩猩血液輸給正常黑猩猩都感染成功,邊續8個月在血液和淋巴液中可持續分離到HIV,在3~5周後查出HIV特異性抗體,並繼續維持一定水平。但無論黑猩猩或長臂猿感染後都不發生疾病。
(四)抵抗力
HIV對熱敏感。56℃30min滅活,但在室溫保存7天,仍保持活性。不加穩定劑病毒-70℃冰凍失去活性,而35%山梨醇或50%胎牛血清中-70℃冰凍3個月仍保持活性。對消毒劑和去污劑亦敏感,0.2%次氯酸鈉0.1%漂白粉,70%乙醇,35%異丙醇、50%乙醚、0.3%H2O20.5%來蘇爾處理5′能滅活病毒,1%NP-40和0.5%triton-X-100能滅活病毒而保留抗原性。外紫外線、γ射線有較強抵抗力。
二、病毒性與免疫性
HIV感染者是傳染源,曾從血液、精液、陰道分泌液、眼淚、乳汁等分離得HIV。傳播途徑有:
1.性傳播:通過男性同性戀之間及異性間的性接觸感染。
2.血液傳播:通過輸血、血液製品或沒有消毒好的注射器傳播,靜脈嗜毒者共享不經消毒的注射器和針頭造成嚴重感染,據我國雲南邊鏡靜脈嗜毒者感染率達60%。
(二)致病機制
HIV選擇性地侵犯帶有CD4分子的,主要有T4淋巴細胞、單核巨噬細胞、樹突狀細胞等。細胞表面CD4分子是HIV受體,通過HIV囊膜蛋白gp120與細胞膜上CD4結合後由gp41介導使毒穿入易感細胞內,造成細胞破壞。其機制尚未完全清楚,可能通過以下方式起作用:
1.由於HIV包膜蛋白插入細胞或病毒出芽釋放導致細胞膜通透性增加,產生滲透性溶解。
2.受染細胞內CD-gp120複合物與細胞器(如高爾基氏體等)的膜融合,使之溶解,導致感染細胞迅速死亡。
3.HIV感染時未整合的DNA積累,或對細胞蛋白的抑制,導致HIV殺傷細胞作用。
4.HIV感染細胞表達的gp120能與未感染細胞膜上的CD4結合,在gp41作用下融合形成多核巨細胞而溶解死亡。
5.HIV感染細胞膜病毒抗原與特異性抗體結合,通過激活補體或介導ADCC效應將細胞裂解。
6.HIV誘導自身免疫,如gp41與T4細胞膜上MHCⅡ類分子有一同源區,由抗gp41抗體可與這類淋巴細胞起交叉反應,導致細胞破壞。
7.細胞程序化死亡(programmedcell death ):在愛滋病發病時可激活細胞凋亡 (Apoptosis) 。如HIV的gp120與CD4受體結合;直接激活受感染的細胞凋亡。甚至感染HIV的T細胞表達的囊膜抗原也可啟動正常T細胞,通過細胞表面CD4分子交聯間接地引起凋亡CD+4細胞的大量破壞,結果造成以T4細胞缺損為中心的嚴重免疫缺陷,患者主要表現:外周淋巴細胞減少,T4/T8比例配置,對植物血凝素和某些抗原的反應消失,遲髮型變態反應下降,NK細胞、巨噬細胞活性減弱,IL2、γ干擾素等細胞因子合成減少。病程早期由於B細胞處於多克隆活化狀態,患者血清中lg水平往往增高,隨著疾病的進展,B細胞對各種抗原產生抗體的功能也直接和間接地受到影響。
愛滋病人由於免疫功能嚴重缺損,常合併嚴重的機會感染,常見的有細胞(鳥分枝桿菌)、原蟲(卡氏肺囊蟲、弓形體)、真菌(白色念珠菌、新型隱球菌)、病毒(巨細胞病毒、單純皰疹病毒,B型肝炎病毒),最後導致無法控制而死亡,另一些病例可發生Kaposis肉瘤或惡性淋巴瘤。此外,感染單核巨噬細胞中HIV呈低度增殖,不引起病變,但損害其免疫功能,可將病毒傳播全身,引起間質肺炎和亞急性腦炎。
HIV感染人體後,往往經歷很長潛伏期(3~5年或更長至8年)才發病,表明HIV在感染機體中,以潛伏或低水平的慢性感染方式持續存在。當HIV潛伏細胞受到某些因素刺激,使潛伏的HIV激活大量增殖而致病,多數患者於1-3年內為死亡。
(三)免疫性
HIV感染後可刺激機體生產囊膜蛋白(Gp120,Gp41)抗體和核心蛋白(P24)抗體。在HIV攜帶者、愛滋病病人血清中測出低水平的抗病毒中和抗體,其中愛滋病病人水平最低,健康同性戀者最高,說明該抗體在體內有保護作用。但抗體不能與單核巨噬細胞內存留的病毒接觸,且HIV囊膜蛋白易發生抗原性變異,原有抗體失去作用,使中和抗體不能發的應有的作用。在潛伏感染階段,HIV前病毒整合入宿主細胞基因組中,不被免疫系統識別,逃避免疫清除。這些都與HIV引起持續感染有關。
三、微生物學診斷
檢測HIV感染者體液中病毒抗原和抗體的方法,操作方便,易於普及應用,其中抗體檢測尤普通。但HIv P24抗原和病毒基因的測定,在HIV感染檢測中的地位和重要性也日益受到重視。
(一)抗體檢測
主要有酶聯免疫吸附試驗(ELISA)和免疫熒光試驗(IFA)。ELISA用去污劑裂解HIV或感染細胞液提取物作抗原,IFA用感染細胞塗片作抗原進行抗體檢測,如果發現陽性標本應重複一次。為防止假陽性,可做Westernblot (WB,蛋白印跡法)進一步確證。
WB法是用聚丙烯醯胺凝膠電泳將HIV蛋白進行分離,再經傳移電泳將不同蛋白條帶轉移於硝酸纖維膜上,加入病人血清孵育後,用抗人球蛋白酶標抗體染色,就能測出針對不同結構蛋白抗體,如抗gp120、gp41、P24抗體,特異性較高。
(二)抗原檢測
用ELISA檢測P24抗原,在HIV感染早期尚未出現抗體時,血中就有該抗原存在.由於P24量太少,陽性率通常較低。現有用解離免疫複合物法或濃縮P24抗原,來提高敏感性。
(三)核酸檢測
用PCR法檢測HIV基因,具有快速、高效、敏感和特異等優點,目前該法已被應用於HIV感染早期診斷及愛滋病的研究中。
(四)病毒分離
常用方法為共培養法,即用正常人外周血液分離單個核細胞,加PHA刺激並培養後,加入病人單個核細胞診斷及愛滋病的研究中。
四、防治原則
自1981年發現愛滋病,隨後在世界各地迅速蔓延,據WHO報告,至1995年1月1日全球累積的HIV感染得為2590萬例,愛滋病人850萬例,死亡病人700萬例,其中非洲流行最嚴重,居首位,其次是東南亞地區。我國於1984年使用美國Ameur公司Ⅷ因子,首次傳入,逐年增加,從1985年至1995年底累HIV感染者3341例,其中117例為愛滋病人,地理分布去最高,佔80%左右,以嗜毒者為主。
由於愛滋病驚人的蔓延速度和高度的致死率,已引起WHO和許多國家的重視,普遍採用了一系列綜合措施,主要包括:
(一)廣泛地開展宣傳教育,普及防治知識,認識本病傳染源、傳播方式及悲慘結局。
(二)建立HIV感染和愛滋病的監測系統,掌握流行動態。對高危人群實行監測,嚴格管理愛滋病人及HIV感染者。
(三)對供血者進行HIV抗體檢測,確保輸血和血液製品安全。
(四)加強國境檢疫,防止本病傳入。
特異預防,迄今尚缺理想疫苗。減毒活疫苗和滅活全病毒疫苗,由於難以保證疫苗安全,不宜人體應用。目前選擇基因工程方法研製疫苗,如克隆囊膜蛋白基因、核心蛋白基因,在細胞和動物細胞中表達多肽作亞單位疫苗,或囊膜基因插入病毒或腺病毒中製備重組疫苗。最大問題是囊膜蛋白高度易變性,不同毒株HIVgp120有明顯差別,使疫苗的使用受到了限制。現已證明包膜蛋白gp120的肽鍵中有一些區段的胺基酸序列比較保守恆定,用該保守恆定片段製備,將能解決問題。
目前用於治療愛滋病的藥物有疊氮脫氧胸苷(AZT)、蘇攔明(Suramin)、雙脫氧胞苷(ddc)、雙脫氧面苷(ddl )等。AZT能干擾病毒DNA合成,從而抑制HIV在體內增殖,緩解症状,延長病人生存期。蘇拉明對HIV的逆轉錄酶活性有抑制作用。ddc是最有效的HIV抑制劑,能明顯減少HIV的複製和改善病人免疫功能。ddl抗病毒的範圍比AZT和ddc 窄一些,但毒性較低,半衰期較長。
此外,發現許多抑制蛋白酶、阻止HIV與靶細胞結合或融合的藥物,能分別作用於細胞感染的不同階段,以達到抗HIV的效果,均尚處於研究階段。
中草藥中發現括蔞蛋白、貝母苷、甘草甜素、及地丁、空心莧、紫草等抽提物有抑HIV的作用。中藥方制治療愛滋病人也能緩解症状,都在研究和總結中。
參看
| 關於「醫學微生物學/人類免疫缺陷病毒」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |