醫院藥學/製劑中藥物的化學分解與穩定方法
| 醫學電子書 >> 《醫院藥學》 >> 藥物製劑的稱定性 >> 製劑中藥物的化學分解與穩定方法 |
| 醫院藥學 |
|
|
|
藥物在製劑中的化學分解有氧化,水解異構化、脫羧、裂環或環重排,聚合等分解途徑,其中以氧化和水解最為常見。
(一)水解反應引起的藥物穩定性水解反應可分為離子型水解和分子型水解兩大類,離了型水解是強酸一弱鹼型鹽或強鹼一弱酸鹽等具有離子鍵的藥物與水的瞬時反應速度一般比較緩慢,在H+或OH-催化下,反慶加速並趨於完全。分子型水引起分子結構的斷裂,可使藥物失效或減效。例如(用通式表示)
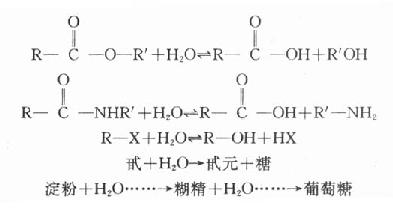
1.酯類藥物的分解;很多含有酯的藥物,在溶液中容易被水解生成有機羧酸和醇的混俁物。這種水解主要是碳原子和氧原子之間即醯一氧鍵之間的共價鍵的。雖然個別酯類(主要是低分子量的伯醇酯類藥物)在單純的水中也能產生明顯的水解,但大多數酯類藥物需要H、OH或方義的酯一鹼或某種酶(例如水解酶)的催化下才能加速其反慶,使反太進行完全。酯的酸或鹼催化水解的動力學方程式通式:
d[酯]/dt=-k[酯][H+]
d[酯]/dt=-k[酯]O[H-]
故為二級反應。但如[H-]或[OH+]>>[酯],或用緩衝鹽保持[H-]或[OH+]於幾乎不變,則:d[酯]/dt=-k[酯][酯]故為偽一級反應。酯的水解常為一級或偽一級動力學反慶但有時是二級反應。琥珀醯氯化膽鹼較氯化乙醯膽鹼穩定,注射液(PH3-5)可以98-1000,30分鐘滅菌粉劑安瓿為宜。琥珀醯氯化膽鹼溶液在PH3.7左右時最為穩定,在P0.9-8.5不解反應是一級反應,反應速度常數可用嗵式K=1.36×10」exp(-17230/RT)計算。本品水解酸一鹼催化,例如醋酸鹽緩衝液(600,離子強度=0.2,PH=4.69,3.98)分解為二級反應,反應速度數為5×10(升
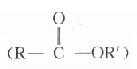
/克分子小時)。故該注射液不應含有緩衝劑;。羧酸酯(R-C-OR)的水解程度與R的結構關係很大,R基愈大或碳上的烷基或其他基團佔據的間愈大,則阻礙H或OH對酯寒攻的作用愈大,故該酯尖藥物愈不易被水解所以溴本辛、普魯本辛就比較穩定,但要製成可以以久使用的水溶液還是困難的,製成片劑時水分也應注意,普魯本辛片劑的水份如果超過3%,貯藏一年以後咕噸酸的含量將超過藥典規定(>2%)。
2.醯胺類藥物的水解本類藥物比相應的酯類藥物可穩定,例如鹽普魯卡因胺比鹽酸普魯卡因要穩定。但有些醯胺藥物,由於結構上的特殊原因。也比較容易被水解。現舉常見的幾種藥物為例子以說明:①青黴素類藥物:青黴素類藥物分屯結構中的B內醯胺環是四節環,內部存在張力,在H、OH影響下易於裂環而失效。例如青黴素G鉀,水溶液室溫貯藏7天,效從下降80%左右,因此只能製成滅粉針安瓿。根據實驗青黴素G鉀在PH6.5時最穩定。用枸椽酸鹽緩衝液(PH6.5)製成的溶液至多也只能用三天。PH2,24℃時的半衰期僅18.5分鐘,故不可口服。②巴比妥類鈉:巴比妥類是六節不的醯胺類藥物,不易水.在溶解度小,通常用鈉鹽作注射液可被空氣中的CO2作巴比妥類分子結構中的亞醯基酸的性比碳酸還弱,故其鈉墁溶液可空氣中的CO2作用生成巴比肝的沉澱,故滅菌粉針宜用無CO2的注射用水溶解。鈉鹽水溶液(灌注於安瓿中,無CO2)在加溫(滅菌時的濕度)或室溫貯藏一個朋,約有22%分解。用60%的丙的二醇為溶劑電的注射泫則甚為穩定,至少可用一年。③氯黴素:氯黴素的化學性質比較,乾燥粉末閉密保存二年,其抗菌效力幾乎不變。溶液(水中溶解度:1:400)煮沸五小時,效價幾首無顯著變化。在顯著鹼性(PH>8)時或酸性時水解較。氯霉在PH=6時最穩定.鹽,枸櫞酸及其緩衝液可促使氯黴素水解(一般酸一鹼催化)。本品滴眼液通常用硼酸一硼酸鈉緩衝液(PH約7),室溫使用期為三個朋,貯藏於2-8中為17個月。氯黴素在PH17的上緩衝液的分解服從一級反應。國內藥廠生產氯黴素滴眼液採用增加設料量的方法,但使用仍不到一年。硼砂可增加氯黴素的溶解度(可能是硼與氯黴素分子中兩個羥基形成了絡合鹽),過去常認為硼砂可增加氯黴素的穩定性,其實不然。
3.延緩藥物水解速度的方法①調節PH:以上許多實例說明藥物的水解速度與溶液的PH直接有關。在較低的PH值範圍內,以H-催化為主,在較高PH範圍時以OH+論為主,在中間的PH範圍,水解反慶能與PH無關或由H-或OH共同催化。為了肯定P具體藥物水解的可以測定幾個P藥物的水解情況,用反應速度常數K的對數對PH作圖,從貢線的最低點(轉折點)可求出該藥物最穩定時的PH值。實驗可在料高的濕度(恆溫)下進行,以但在較短的時間內取得結果。這樣得到轉折點以溫時得到的有些不同但通常不大,可以用酸或鹼緩衝溶液被所用的緩衝鹽所催化(一般酸一鹼催化),則級鹽應保值最低的濃度。②選用適當的溶劑:用介電常數較低的溶劑如乙醇、甘油,丙二醇、聚乙烯二醇、N,N一甲基乙醯等部分或全瓿代替水作為溶劑,可使藥物的水解速度降低。但是對於個別藥物卻是例外,如環乙酸(C-yclamicacid)在水溶液中水解慢,在乙醇液中卻顯著變快。氯黴素在50%二醇溶液的水解速度也稍有增加。因此對具體藥物應通過實驗才能得出符合的結論。③製成維溶性鹽或酯:一般而言,溶液中溶解的那部分藥物才水解反應。將容易水解的藥物製成難溶性的酯類衍生物,其穩定性將顯著增加。水溶性愈低往往愈穩定。例如青素G鉀鹽、在水中溶解的而破壞已如前述,只是普魯卡因青黴素G(水中溶解度為1:250)就7較穩定,其混懸液中鐾光並低於20處貯藏,可以保持效價至少18個月。三乙醯竹桃黴素(Friacetyloleandomycinum)。紅霉素硬脂酸酯等維溶性藥物,不僅化學穩定性優於母體藥物,而且無味、耐胃酸;口服後比母體藥物更好。④形成絡合物:加入一種化合物,使它與藥物形成水中可溶並且對藥物有保護作用的絡合物,這絡合物所以對藥物有保護作用可能有空間障礙和極性效慶二種原因。⑤加入表面活性劑:在脂或醯類藥物[溶液中加入適當表面活性劑,有時可以增加某些藥物的穩定性,例如苯佐卡因含5%月桂酥醇硫酸鈉(陰離子型表面活性劑)的溶液,可使苯佐卡因的半衰期半增中18倍,這可能是月桂醇酸鈉與苯佐卡因形成膠團,苯佐卡因藏在膠團內部,減少了OH-對苯佐卡因分子中酯鍵的攻擊。⑥改變藥物的分子結構在脂類藥物(R-COOR)和醯類藥物(R-COOR)的a一碳原了上引入其它基團或側鏈或增加R或R』碳邏的長度以增加空間效應可極性效應,可以有效地降低這些藥物水解速度。⑦製成固體製劑:將藥物製成固體製劑穩定性可以大大提高。⑧控制溫度:濕度升高,水解反應速度隨之增加。
(二)由於氧化所引起的藥物不穩定氧化反應是藥物分解失效的重要原因之一。維生素C、嗎啡、腎上腺一素、鹽酸硫胺等,都是熟知的例子。
1.容易氧化的藥物藥物氧化分解的結果,使藥物失效、顏色變深、顏色變深、形成沉[淀或產生有毒物質(如新胂凡納明暴露於空氣中,易氧化變質,毒性顯著增加而不能供藥用)。有些注射劑其中藥物雖僅極少一部分氧化,但顏色變深,以致可能成為廢品。藥物的氧化過程比水解不要複雜,往往不易用明反應式完整的表達。本節列舉的某些藥物的氧化反慶,可能是水解過程中主要的反應。①酚類藥物:分子結構中具有酚羥基的藥物如腎上腺素、多巴胺、嗎啡、水嗎啡、水楊酸鈉等,在氯金屬離子、光線、濕度等的下,均易氧化變質。酚類藥物被氧化,大多因為酚羥基變成醌式結構順而呈黃棕等色。維生素C的分子結構不存在酚羥基,但有醇結構,很易氧化生成一系列有色的無效物質。維生素C的氧化分解已有過廣泛、深入的研究,資料累積很大,但它的自氧化反太機理還是很不清楚。在無空氣的情況下,維生素C降解後生成糠醛和二氧化碳。糠醛很易氧化,聚合生成有色物質,此可能是本品晶體表面存在黃色的一個原因。空氯中的氧可氧化維生素C為去氫維生素C,中還原劑存在下,後者仍可轉變為維生素C。去氫維生素C很不穩定,迅速生成2,3一二酮基古羅酸(鈉)等分解物,溶液由於黃色以變為橙紅色、維生素C溶液中如果沒有金屬離子,只在在PH9以上時才不較明顯的氧化反應產生,但如有銅離子在,即使PH=6.5,氧化反應極為迅速。銅對維生素C是極強的氧化催化劑,只要2×10-4M/L的濃度,就能使維生素C一價陰離子的氧化反應速度增大10000倍。鐵、鋁電漿也可使維生素C分解。維生素C溶液最穩定的PH值為5.4。需加焦亞硫酸鈉用抗氧劑。溶液通過二氧化碳比通氮好。氯化鈉、丙二醇、甘油、蔗糖、螯合劑對維生素C都有穩定作用。②芳胺類藥物:如磺胺類鈉鹽、鹽酸普魯卡因胺、對氨基水楊酸鈉等芳午藥物,也比較容易氧化。與酚類藥物一樣,多數芳胺類藥物的氧化反應過程都異常雜,很多還不夠明了。③其他類型藥物:吡唑酮類藥物例如氨基比林、安乃近的水溶液,也比較容易氧化,生成黃色。一般認為是吡唑酮環上的不飽和鍵被氧化。噻類藥物如鹽酸異丙嗪。鹽酸氯丙嗪等,在光、金屬離子、氧等作用下,極易氧化變色,注射注0常用焦亞硫鈉,維生素C、EDTA-Na2等為穩定劑,以減緩氧化。含有不飽和賓藥物,能常也很易氧化例如維生素A、維生素D、油脂,在光線、氧、水份、金屬防子以及微生物等影響下,都能產生氧化拓應而分解。揮髮油中含有的成分萜烯、蒎烯、氧化後有醛、酮形成,所以有特殊味。萜烯和蒎烯等氧化後尚可聚合生成樹脂狀物。鹽酸硫胺可被空氣中的氧氧化生成無效的充色素,但不用亞硫酸為抗氧劑。因後者可使鹽胺安全斷裂、失效。
2.影響物質氧化速度的因素①有機藥物不飽和程度:雙鍵較欽的藥物通常均容易氧化。②游離脂肪酸:有機羧酸或醇類藥物比它們相應的酯容易產生自氧化反應。③與金屬離子:金屬特別是二價以上的金屬離子Cu++、Fe++、Pb++、Ni++等),可以促進反的,是藥物分解的催化劑。④易氧化的藥物的物理狀態:通常固體脂肪要比液體脂肪不易發生自氧化反應。這可能是氧在固化脂肪中不易擴散的緣故。⑤氧的含量:大多數藥物的氧化分解是懈含游離基的自氧化反應。有時僅需痕量的氧就可以引起這種反應。一旦反應進行,氧的含量便不重要了。⑥濕度:一般而言,濕度增加,氧化反應的速度加速。但濕度增加時氧在水中的溶解度減低。
3.延緩藥物氧化分解的方法①除去氧氣;②加入抗氧劑;③調節PH值。
(三)由於其他反應引起的不穩定性
1.異構化異構化分為光異構化和幾何構化二種,前者又分為消旋化和差向異構化。①光學異構化:甲、外消旋化:具有光學活性的藥物在溶液中受H+、OH-或其他催化劑及溫度等的影響下轉變成它的對映體的過程,這個反應過程一直進行到生成等量的二種對映體為止,因此最後得到1/2量的左旋體和1/2量的右旋體混合物,結果這個藥物溶液的旋光度等於零。級大多數藥物的左旋體的生理活性大於右旋體(泛酸鈣和乙胺乙醇例外0,但右旋體往往也有一定的生理活性,故外消旋藥物的生理活性一般超過純粹左旋體的一半些。外消旋反應的與否道德決定於不對稱碳原子上的聯著的基因,不對稱碳原子聯接有度香或具有苄醇的結構,則外消旋反應較易進行。因此左旋明上腺素和左旋莨蓉鹼都容易外消旋化。外消旋反應與OH-、H+等的催化劑、溫度、光線等有關。外消旋反慶的學研究,在方法上與水解反慶相似。一般外消旋反應是按一級反就進行的。乙.差向異構化;某些具有多個不對我碳原子的藥,其中一個不對兒碳原子上的基因發生立體異構化,稱為差向異構化。差向異構化反應達到平衡時,二個差向異構體的是一不盯等,故其光學活性不等於零,這點與外消旋化不同。②幾何異構:含有雙健的有機藥物,順式幾何異柢體與反式向何異構體的生量活性往往是不相同的。維生素A分子中有五個共軛的雙鍵,理論上有16個幾何異構體,各異構體的生理活性互有不同,其中以全反式的異構體為最高。在PH較低的水中,可生成Retro維生素A及支水維生素A,前者的生理活性僅為反式維生素A的12%後者則無生理活性。維生素A棕櫚酸脂與其他維生素製成的複合維生素混懸劑(助懸劑為吐溫-80,PH=5.3),經過一年左右的貯藏以後,除了因氧化而分解外,還有10-―順式和10,15二順式二種異構體生成,這兩種異構體的生理活性很弱。
2.由於聚合作用而產生的藥物變質,二個以上相同的藥物分聚合而使藥物變質的實例不多,比較熟知的是甲醛溶液中加入可10%-15%甲醇可以減緩其聚合。藥物本身由於聚合作用而出現沉澱,變色等現象比較常見。例如葡萄糖注射液熱壓滅後不少量5-羥甲基呋喃甲醛形成,後者聚合生成有顏色的聚合物,因而使注射液微濕黃色。
3.由於脫反應而引起的分解,由於藥物分子結構中的羧基脫裂而引起藥物分解的情況,有時可能遇到。對氨基不楊酸鈉注射液因為對氮基水楊酸分解,脫去羧基生成間氨基苯酚而易使顏色變深。對氨基水楊酸鈉的脫羧反應與溶液的PH很有在系,偏鹼性時比穩定,PH6.3開始明顯產生脫羧,PH2.7時達最高峰。本品20%溶液三個月,約有2.5因脫羧而分解。1150、30分鐘則有15%分解,故本品以製成來菌粉末安瓿為宜。
4.吸收二氧化碳引起的藥物分解有些鹼性藥物,可因吸收空氣中的CO2作用失去相應的碳酸鹽而改變藥物原來的性質。如丙環乙(Propylhexedrinum)是一種有揮發性的液體按類藥物,製成吸入劑吸入鼻腔以收縮局部血管,丙環乙胺能吸收空氣中的CO2生成碳酸鹽而減弱其的揮發性,從而影響其療效。巴比妥類鈉鹽溶液遇CO2可能生成巴比妥類沉澱。
5.藥物之間互相作用將兩種或兩種以上藥物配合使用,如果不了解藥物的理化、藥理等方面的性質,不明白藥物在臨床上的使用要求而盲目的混合使用,往往不但不能達到醫療上的預期目的,而且有時還可能產生不良後果甚至危及患者生命。
| 關於「醫院藥學/製劑中藥物的化學分解與穩定方法」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |