臨床生物化學/糖尿病的生物化學檢測
| 醫學電子書 >> 《臨床生物化學》 >> 糖代謝紊亂 >> 高血糖症與糖尿病 >> 糖尿病的生物化學檢測 |
| 臨床生物化學 |
|
|
|
(一)血糖的測定
血糖的測定是糖尿病生物化學檢測中最常見的方法之一,糖尿病患者均有不同程度的血糖升高。
測定血糖的標本以血漿最為方便,測得結果最可靠。一般情況下全血葡萄糖濃度比血漿低10%-15%,毛細血管血樣與靜脈血樣二者的測定值在空腹時無區別,但餐後1小時血樣,二者血漿血糖水平可相差2.27±0.66mmol/L。測血糖的血漿中取空腹、進食一小時或隨機取血,一般採用空腹血樣本。抗凝劑用草酸鉀氧化鈉(2mg/ml可在24小時內阻止葡萄糖酵解)。正常人空腹血漿葡萄糖濃度的參考範圍為3.9-6.7mmol/L。若空腹靜脈血糖濃度大於8mmol/L,且有臨床症状,可診斷為糖尿病。若小於6mmol/L,則可除外糖尿病;若在6.0-7.0mmol/L之間,應複查做進一步檢查。進餐後1小時,血糖濃度可一時性升高,並伴有胰島素分泌增多。若餐後1小時血糖明顯增高,而血漿胰島素為低水平,則可論斷為糖尿病;若餐後2小時,血漿葡萄糖濃度大於7mmol/L,可懷疑為糖尿病。因為正常人餐後,葡萄糖的來源增加,血中葡萄糖濃度會反應性的一時升高,但多不超過腎糖閾,故尿病試驗為陰性。高糖的刺激使胰島素分泌增加,後者作用的結果,使餐後2小時內血糖濃度恢復到空腹水平。只有在胰島素不足時,餐後血糖才持續升高,且不恢復到空腹水平。如果隨機血樣濃度大於11mmol/L,也可論斷為糖尿病。
測定血糖的方法主要有兩種,即化學法和酶法。化學法具有操作簡便、快速、試劑價廉等優點,但由於干擾較大,所以仍屬不理想的方法。已糖激酶法以其高度特異性,方法靈敏、準確,干擾因素少等優點被公認為參考方法。我國臨床檢驗中心推薦的葡萄糖氧化酶-過氧化物酶比色法(GOD-POD法)目前已廣泛用於臨床。本法分析性能與已糖激酶法相近,且試劑穩定、價格便宜、操作簡便。酶法測血糖還可以標準化、程序化、宜用於自動分析儀。用酶製劑製成的試紙條或膠片,直接用毛細血管進行快速分析,方便了患者根據血糖濃度自行調節胰島素的劑量,以監控糖尿病的胰島素治療。固相酶試片法還提高了酶製劑的穩定性,所以是大有發展前途的。
(二)尿糖的測定
正常人24小時由尿排出的葡萄糖少於0.5g,在常規尿葡萄糖檢測時為陰性。只有當血糖濃度高於8.9-9.9mmol/L(160-180mg/dl),超過腎小管重吸收能力時,尿糖試驗才為陽性。所以將腎對葡萄糖的吸收能力用血糖濃度8.9-9.9mmol/L(160-180mg/dl)表示,即此值為正常腎糖閾。臨床上有些糖尿病是由於受試者腎糖閾值低於正常人,如妊娠婦女由於腎糖閾值降低,可出現暫時性糖尿。而長期患糖尿病的患者其腎糖閾值可高於正常人。
尿糖測定已廣泛用於對糖尿病的初判斷,通常作為過篩程序的一部分。尿糖測定一般不需要準確定量,當尿糖濃度為5.55-11.1mmol/L時,應考慮糖尿病。尿標本以膀胱排空再飲水後30分鐘為宜,這樣更能準確地反映病人的代謝情況。
腎性尿糖是由於慢性腎炎、腎病症候群等疾病引起腎臟對糖的重吸收障礙而出現的尿糖,但病人血糖及糖耐量曲線基本正常,這與糖尿病性尿糖有根本的區別。
(三)口服葡萄糖耐量試驗(oralglucosetolerancetest,OGTT)
OGTT是一種葡萄糖負荷試驗,用以了解機體對葡萄糖的調節能力。當空腹血漿葡萄糖濃度在6-7mmol/L之間而又懷疑為糖尿病時,作此試驗可以幫助明確診斷。
WHO標準化的OGTT是:試驗前3日,每日食物中糖含量應不低於150g,且維持正常活動。影響試驗的藥物(表3-3)應在3日前停用。試驗前病人應10-16小時不進食。坐位取血後5分鐘內飲入250ml含75g無水葡萄糖的糖水,以後每隔30分鐘取血1次,共4次,歷時2小時。整個試驗中不可吸煙、喝咖啡、喝茶或進食。兒童給予葡萄糖量為0.75g/kg體重。於采血的同時,每隔1小時留取尿液做尿糖半定量試驗。必要時可適當延長血標本的收集時間,可長達口服葡萄糖後6小時。
表3-3影響葡萄糖耐量的常用藥物
| 可引起血糖升高的藥物 | 可引起血糖降低的藥物 |
| 咖啡因、兒茶酚胺、皮質醇類、阿密替林、呋喃苯胺酸(速尿)、氯噻酮、噻嗪類、氯壓定、吲哚美辛(消炎痛)、口服避孕藥、氟哌啶醇、碳酸鋰 | 磺胺、磺醯脲、乙醇、水楊酸鹽 |
一般根據5次葡萄糖水平,以測定血糖的時間為橫座標(空腹時為0時),血糖濃度為縱座標,繪製耐糖曲線。臨床上常用的方法是清晨抽空腹血後,口服100g葡萄糖(或按1.5-1.75g/kg體重),再於給糖後0.5、1、2、3小時各取血1次,將測得的血糖按上述方法做耐糖曲線。本試驗常用於協助診斷糖代謝紊亂的疾病。
⒈正常糖耐量正常人由於存在精細的代謝調節機制,服糖後0.5-1小時血糖濃度暫時略有升高,耐糖曲線顯示峰值<10mmol/L,但尿糖陰性。1小時後血糖逐漸降低,一般2小時左右恢復至空腹3.9-6.7mmol/L水平。此種糖耐量曲線說明機體處理糖負荷的能力良好(圖3-3)。

圖3-3 葡萄糖耐量曲線
⒉糖尿病性糖耐量典型的糖尿病人糖耐量試驗為:患者空腹血糖≥8.0mmol/L,高於正常值;服糖後血糖急劇升高,血糖增高的時間仍為0.5~1小時,但峰值超過10mmol/L,並出現尿糖;以後血糖濃度恢復緩慢,常常2小時以後仍高於空腹水平。說明病人處理攝入糖的能力降低。
此時重要的判斷指標是服糖後2小時血糖濃度仍然高於空腹水平。對於早期糖尿病人,可只表現為OGTT後2小時血糖濃度仍高於8mmol/L。若空腹血糖正常而OGTT後2小時血糖大於11mmol/L,以及空腹血糖>8mmol/L而OGTT2小時的血糖水平在8-10.9mmol/L者,均應診斷為糖尿病。
⒊糖耐量受損如果非妊娠的成年人OGTT呈現空腹葡萄糖水平<8.0mmol/L,服糖後60、90分鐘的血糖≥11mmol/L(有人30分鐘也可達此值)而2小時血糖值在8-11mmol/L之間則為輕度耐糖能力下降,稱為亞臨床或無症状的糖尿病。這些病人幾年後可能有1/3恢復正常,1/3仍為糖耐量受損,1/3則轉為糖尿病(每年約1%~5%)。近來發現,這些病人容易發生小血管合併症,如冠心病、腦血管病,而不會發生微血管合併症,如視網膜病、腎病。
耐糖試驗受許多因素影響,如年齡、飲食、勞動、應激、藥物、胃腸功能、標本採集和葡萄糖測定方法等。所以臨床上要具體情況具體分析。
對於OGTT正常而有糖尿病家族史的病人,可以進行可的松OGTT,即在應激的同時再給予糖負荷,通過加強機體對胰島素分泌的要求來提高耐糖試驗的敏感性,用以觀察機體有無潛在的耐糖缺陷。具體做法是,在第1次OGTT後給病人口服50mg醋酸可的松,6小時再服1次,兩小時後進行第2次OGTT。年齡在50歲以下的受試者,若血糖濃度在60分鐘時高於10.2mmol/L,90分鐘高於9.4mmol/L,120分鐘高於9.0mmol/L,表示有潛伏性糖尿病。若兩次OGTT的血糖濃度相差2.9mmol/L以上,說明病人對皮質類固醇的影響很敏感。
50歲以上的老年人對葡萄糖的耐受能力有下降趨勢,所以不宜作此類試驗。對於老年人的OGTT結果的判斷,要注意區別是正常老年伴有的變化,還是糖尿病所致。兒童糖尿病的診斷標準與成人相同,但兒童空腹血漿葡萄糖的正常值比成人高0.83mmol/L。
由於妊娠性糖尿病致先天畸形及胎兒死亡增多,所以對孕婦進行有否糖尿病的檢測應予以重視,特別對肥胖、直系親屬有糖尿病、有流產、畸胎或滯胎歷史的孕婦,更應進行OGTT,以便發現糖尿病,並及時進行治療、控制。
糖耐量試驗雖然可以反映機體近期糖代謝的情況,但由於采血次數較多給病人帶來一定的痛苦。臨床上對於血糖持續增高並伴有糖尿,再結合病史及體征能夠確診的病人,毋須再做OGTT。
⒋糖化蛋白的測定成人紅細胞的血紅蛋白(Hb)主要是HbA1,佔90%以上,HbA2佔2.5%,HbF佔0.2%,其餘為HbA3。HbA3為連接有已糖的HbA1,其中HbA3a佔Hb總量的0.8%,HbA3b佔1.6%,HbA3c佔4%。凡連接有已糖的HbA1,統稱為糖化血紅蛋白(glycoseylated,hemoglobin,GHb)。HbA3a、HbA3b、HbA3c也可分別表示為HbA1a、HbA1b、HbA1c。HbA1a還可分為HbA1a1和HbA1a2。HbA1c是Hbβ鏈的氨基末端纈氨酸殘基與葡萄糖醛基通過非酶促反應縮合而成。HbA1a1是與1,6-二磷酸果糖結合,HbA1a2則是與6-磷酸葡萄糖結合形成的GHB。HbA1b的結構還不清楚。在四種GHb中HbA1c最多,佔GHb總量的80%。有報導,正常人血液中HbA1c約佔血紅蛋白總量的5%-8%,而糖尿病時可達8%-30%。
GHb是在紅細胞生存期間,HbA1與血中已糖(主要為葡萄糖)緩慢、連續的非酶促反應產物,為HbA1合成化學修飾的結果。GHb的形成取決於血糖濃度和作用時間,生成量與血中葡萄糖濃度成正比。紅細胞平均壽命為120天,因此GHb的濃度反映測定日前2-3個月內受試者血糖的平均水平,而與血糖的短期波動無關。所以目前測定糖化血紅蛋白,只作為糖尿病病人6-10周前血糖水平的定量指標。在新發生的糖尿病病人,臨床檢測只有血糖水平增高,而GHb正常;而未控制的糖尿病病人,則既有高血糖,也有GHb增多;在糖尿病已被控制的人群中,可見到血糖正常,GHb水平仍較高。這是因為GHb的形成與消失均需要數周時間。所以GHb水平不能反映近期的血糖水平,不能提供近期的治療效果。但它是糖尿病長期監控的良好指標,尤其對IDDM和妊娠期性糖尿病的治療監控有用。
血清白蛋白亦可糖基化,而且白蛋白的半壽期僅為19天。因此測定糖化白蛋白可了解糖尿病近二周的血糖水平,反映糖尿病治療的較近期效果。
GHb的測定方法為:首先將紅細胞樣品在等滲鹽溶液中放置一定時間以除去細胞中游離的葡萄糖,然後將細胞溶解並離心取上清液,進行離子交換層析。洗脫液用分光光度法在410nm處測吸收光度。在所測得的峰值中,HbA1a、HbA1b和HbA1c均為GHb。在血紅蛋白的電泳實驗中,GHb為快動組分。
正常人GHb為6.5%±1.5%。臨床上隨機測GHb,若<8%,多不考慮糖尿病;當所測的GHb>9%,預報糖尿病的準確度約78%,靈敏度為68%,特異性94%;若測得GHb>10%,則有89%為糖尿病,靈敏度43%,特異性99%,有效率86%。GHb的測定還可協助判斷預後。據報導糖尿病合併視網膜病的病人,如果GHb為8%-10%,表示病變為中等程度,可以用雷射治療;若GHb>10%,則為嚴重損害,預後較差。
糖化白蛋白在糖尿病組為6.1%-22.3%,非糖尿病組為1.9%-5.8%,與糖化血紅蛋白相關良好(γ=0.91)。
總之,目前測定糖化蛋白主要測GHb,其在臨床上對糖尿病人治療效果、監測病人對治療的適應性方面應用較廣,且是一個很好的參數,而對糖尿病的診斷作用不如血糖和OGTT靈敏。
⒌胰島素、胰島素原和C肽的測定胰島素是由胰島β細胞合成和分泌的一種蛋白質。和其他蛋白質一樣,有粗面內質網的核糖核蛋白體上新合成的胰島素是由102個胺基酸組成的前體,稱為前胰島素原(preproinsulin)。前胰島素原穿過內質網膜進入腔內,隨即切去前面由16個胺基酸組成的信號肽,生成胰島素原(proinsulin,86肽),並輸送到高爾基體貯存。胰島素原是一條直鏈多肽,兩端分別是胰島素A鏈(21肽)和B鏈(30肽)的肽段,中間是一條由35個胺基酸組成的肽段,與A鏈的N端和B鏈的C端相連(圖3-4)。當胰島素分泌時,在蛋白水解酶的作用下,將這條連接肽兩端分別切下2個鹼性胺基酸(精-精、精-賴),生成胰島素和C肽(connectingpeptide,即連接肽),二者一起分泌入血。所以了解胰島素合成及分泌功能時,可以測定胰島素原、胰島素和C肽。
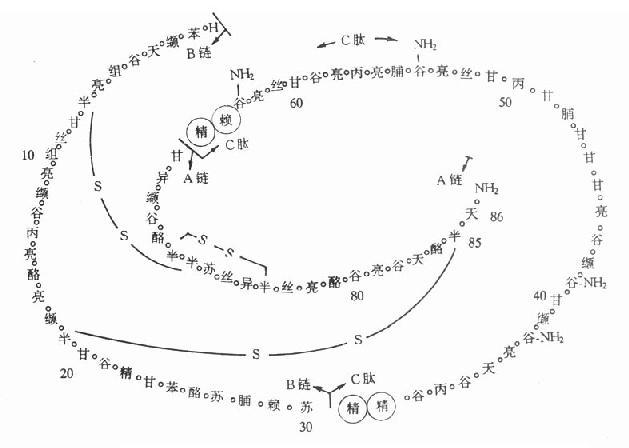
圖3-4 人類胰島素原的一級結構
用胰島素或C肽的抗體建立起來的RIA方法,都可用於胰島素分泌功能的測定。分泌入血的胰島素流經肝時,50%以上將被肝細胞攝取,繼而降解,其在血循環中的半壽期約為5分鐘。胰島素每天僅不足1%由尿排出,而被腎小管重吸收的胰島素60%在腎實質降解。胰島素的基礎分泌量為每小時0.5-1.0單位,進食後分泌量可增加3-5倍。在胰島素依賴型糖尿病病人血清中常常發現有胰島素抗體,後者使胰島素不能發揮其正常生物活性,而且還使胰島素分泌功能逐漸減退,以至完全喪失。雖然檢查胰島素分泌功能對診斷IDDM有重要意義,但因血中本身存在胰島素抗體,患者又使用了外源性胰島素治療,故用RIA測定血中胰島素濃度,或口服葡萄糖耐量試驗都不能得到準確的結果。若改為測定C肽則可克服這些干擾。
由於胰島β細胞分泌胰島素的同時也等摩爾地釋放了C肽,所以測定C肽可以反映β細胞生成和分泌胰島素的能力。特別在用胰島素治療了的病人,測血漿中C肽水平更能準確反映胰島素功能,況且C肽在循環中很少被肝代謝,C肽的清除率也小於胰島素。測定不同時間外周血漿中C肽和胰島素量,可估計肝攝取處理胰島素的能力。近年來用測定基礎C肽及其對某些刺激因子的反應來估計糖尿病病人胰島素的依賴性。目前認為糖尿病病人空腹血漿C肽≥1.9μg/L,口服甲苯磺丁脲後5分鐘,C肽增至20.4μg/L,此類病人90%可通過限制食物和用降低血糖的藥物控制病情,治療中不需用胰島素。若病人空腹C肽<1.9μg/L,則需要用胰島素治療。正常人空腹血漿C肽為2.2μg/L。
正常人每天C肽分泌總量的4%出現於尿中,所以尿C肽的測定也可作為β細胞分泌功能的指標。
目前C肽的測定已用於糖尿病的分型,但由於尚缺乏標準方法,空腹血漿C肽的參考範圍變化相當大,故需進一步改進。
由於糖尿病和糖耐量受損的病人血漿中都可見到低胰島素或高胰島素水平,所以血漿胰島素測定對診斷糖尿病價值不大。如果病人已用胰島素治療了6周,血中已產生了抗胰島素抗體,此時用一般的放免法檢測胰島素更無意義。NIDDM病人多數與靶細胞受體數目減少有關。口服葡萄糖後血液胰島素增高的程度顯著高於非肥胖正常人,說明其胰島素分泌功能正常,病因則是靶細胞對胰島素的敏感性降低。病人血中胰島素增高,即可引起受體的減數調節,進一步降低靶細胞的敏感性,以致病情逐漸加重。顯然這類患者不適於用胰島素治療。對於這些病人,用RIA法測定血中胰島素含量可以反映胰島分泌功能,不必改用C肽測定。臨床上長期大量應用胰島素,常常發現胰島素的療效逐漸下降,甚至完全喪失應答能力。已經證明,這是靶細胞對激素作用的一種自我調節功能,稱為激素受體的減數調節。減數調節的結果是靶細胞表面受體數目逐漸減少。
胰島β細胞分泌胰島素時也分泌有少量胰島素原,約佔血漿總胰島素的5%。由於胰島素原的生物學活性僅為胰島素的3%-6%,且血漿中含量更微量,檢測時需大量樣本,所以臨床並不常用。當血循環中胰島素水平太高且有病理情況時,需測定胰島素原,方法是靈敏度和特異性均高於RIA的雙點放免法。臨床上發現,胰島瘤病人有胰島素原增高。患糖尿病的兒童也表現有胰島素原分泌增加。
由於糖尿病是一個複雜的代謝紊亂性疾病,病人除了有上述代謝紊亂的表現外,還將出現多系統、多方面的代謝紊亂,故實驗室檢查也應多方面輔助檢查。如糖尿病合併有酮症或酮症酸中毒時,可做血、尿酮體及血氣分析;如病人合併有高脂血症,則應做血脂或血漿脂蛋白檢測,以便正確治療;糖尿病病人無酮症酸中毒,但卻出現昏迷時,可能為血糖過高所引起的高滲性昏迷,檢測其血、尿滲透壓可見均升高;對於有脫水症状的病人,則應檢測血清電解質。
| 關於「臨床生物化學/糖尿病的生物化學檢測」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |