病理生理學/繼發性高血壓
| 醫學電子書 >> 《病理生理學》 >> 心力衰竭及高血壓 >> 高血壓 >> 高血壓的原因和機制 >> 繼發性高血壓 |
| 病理生理學 |
|
|
1.腎性高血壓 腎疾患時出現的高血壓謂之腎性高血壓(renal hypertension),為繼發性高血壓中最常見者,發病的主要機製為:
(1)RAS激活:見於各種原因所致的腎動脈狹窄或阻塞時,例如腎動脈粥樣硬化(多見於男性老年人)、腎動脈纖維增生性病變(fibroplsatic disease,多見於中青年)和腎動脈先天性發育不良(見於兒童)等。由於腎臟缺血促進腎素分泌,激活了RAS並進而引起高血壓。其主要依據是:①手術縮窄犬一側腎動脈後,與血壓升高的同時,手術側腎靜脈血中腎素明顯高於對側,且近球小體中含腎素顆粒也明顯增加;解除狹窄後,隨著腎素含量的下降血壓下降血壓也降低;②用血管腎張素轉換酶抑制劑可使血壓下降;③大部分本類高血壓患者血漿中的腎素活性增高。RAS在活性增高的升壓機制主要是使血管收縮,使外周阻力增加。
(2)腎排水、排鈉能力減弱或喪失:多見於急性或慢性腎實質廣泛性病變時(如急性或慢性腎炎、腎盂腎炎、多囊腎等),由於大量腎單位喪失了排水、排鈉能力,而剩餘腎單位又不能充分代償,結果導致鈉水瀦留、血容量增加和心輸出量增大,產生高血壓。此時血管外周阻力可正常甚至低於正常。採取利尿措施以減少血容量可有效地降低血壓。
(3)腎減壓物質生成減少:腎不但分泌加壓物質,腎髓質間質細胞還分泌多種減壓物質,如前列腺素E2(PGE2)和具有抗高血壓作用脂質等物質。這些物質都具有排、擴血管和降低交感神經活性的作用,和RAS既互相對抗又維持著平衡。
現證明這些特質的消長與高血壓的發生有密切關係,例如:①腎髓質乳頭移植,可防止腎實質性高血壓的發展,但移植腎皮質則無此作用:②在鈉負荷的情況下,切除腎髓質可很快發生高血壓,但不切除髓質則不易發生。所以當腎髓質受到破壞或其間質細胞產生減壓物質減少(或被抑制)時,由於RAS與減壓物質失去平衡,即可引起血壓升高。
上述三種機制,在腎性高血壓發病中的作用因腎疾患的種類、部位和程度不同而異。例如:腎血管疾患時以第一種機製為主。腎實質性病變尤其是伴有腎功能不全者以第二種機製為主;腎髓質破壞時則有第三種機制參與;但在慢性腎疾患時,由於病變性質和部位的複雜,三種機制常同時參與作用。
2.內分泌性高血壓由內分泌紊亂引起的高血壓謂之內分泌性高血壓(endocrinic hypertension),主要見於:
(1)嗜鉻細胞瘤:嗜鉻細胞瘤(pheochromocytoma)多發生於腎上腺髓質。由於嗜鉻瘤細胞大量分泌和釋放去甲腎腺素和腎上腺素,使小血管收縮和心輸出量增加,故可導致血壓升高。這種血壓升高多為陣發性的,即當缺氧、麻醉、肌肉活動、性活動或腎上腺部位受剌激時,就可激發瘤細胞釋放這些物質而血壓突然升高,並多伴有心悸、出汗、煩躁、頭痛、胸前區痛和血糖升高等臨床表現;當血中此類物質含量降低時,血壓也隨之下降。但也有少數患者血壓呈持續性升高。應用α-腎上腺體拮抗劑可使血壓恢復正常,用β腎上腺素受體拮抗劑可有效地控制心輸出量增加和其它臨床表現。
(2)原發性醛固酮增多症:原發性醛固酮增多症(primary aldosteronism),多見於腎上腺皮質球狀帶腫瘤或雙側腎上腺皮質增生時。血壓升高主要是由於醛固酮分泌過多導致血容量和心輸出量的增加。血容量增加可抑制腎近球小體細胞的腎素分泌,故血漿腎素低於正常,此和繼發性醛固酮增多症有些不同(後者腎素活性升高)。另外,由於醛固酮促進腎曲小管的Na+-K+交換使排鉀增加,故常導致低鉀血症。
(3)皮質醇增多症;皮質醇增多症(hypercortionlism)是由於腎上腺皮質分泌過量的糖皮質激素(主要是皮質醇)所致。該症如由腎上腺皮質腫瘤所引起,稱為Cushing症候群;本症約有80%伴有高血壓。血壓升高的主要機制是:糖皮質激素可①促進的瀦留和增加血漿容量;②剌激腎素的合成,激活RAS;③加強血管對加壓物質(如去甲腎上腺素)的加壓反應。如果伴有鹽皮質激素(脫氧皮質酮、醛固酮)增加時,則更使鈉水瀦留加重。
(4)腎上腺某些酶的先天性缺陷:常見的是11-β羥化酶和17-α羥化酶的缺乏。當前一種酶缺乏時,皮質醇生成減少,反饋性地促進ACTH分泌增加,使脫氧皮質酮(DOC)生成增多,結果是鈉水瀦留、血壓升高;同時因17-羥孕烯醇酮增多,使雄性激素的生成也增多,故女性患者常出理男性化。當後一種酶缺乏時,因17-羥孕烯醇酮的減少,不但反饋性地促進ACTH分泌增加,從而引起高血壓,並且雄性激素生成也減少,故男性患者出現女性化(圖12-8)。
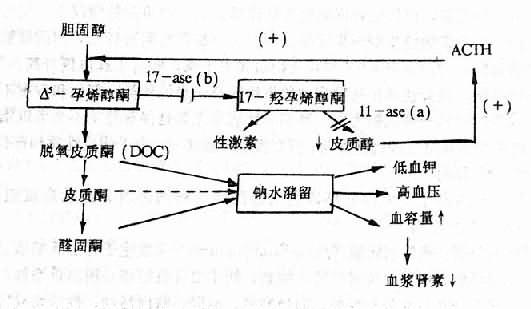
圖12-8 11-β羥化酶(11-ase)和17-α 羥化酶(17-ase)缺乏時發生高血壓機理示意圖,
11-ase(a)示11-β羥化酸缺乏影響部位;
17-ase(b)示17-α羥化酶缺乏影響部位;(+)反饋性興奮
3.妊娠高血壓妊娠期發生和發展起來的高血壓謂之妊娠高血壓(pregenancy-induced hypertension)。由於正常妊娠期的血壓較未妊娠時低,故判斷妊娠高血壓的血壓水平也應較一般的診斷標準低。在妊娠4~6個月時舒張壓超過10.7kPa(80mmHg)或妊娠7~9個月時超過11.3kPa(85mmHg)時,或者高於妊娠早期4.00/2.00kPa(30/15mmHg)時,即可視為高血壓。包括①先兆子癇高血壓(又稱妊娠中毒性高血壓);②慢性高血壓,多來源於原發性或腎性高血壓;和③子癇前合併慢性高血壓。
先兆子癇高血壓(preeclamptic hypertension)是妊娠期特發的高血壓,多發生在妊娠的後期,伴有蛋白尿和/或水腫。主要是由於胎盤組織供血絕對減少(因血液循環障礙)和/或相對減少(因胎盤組織增大)從而導致胎盤缺血的結果。此時,①缺血的胎盤可產生較多的腎素和血管緊張素類物質(患者子宮和胎盤中含量較正常妊娠者高);②胎盤組織產生的抗RAS的減壓物質減少。正常妊娠的胎盤所產生的減壓物質(如前列腺素)能和RAS保持對抗性的動態平衡,從而抵消RAS的加壓效應。先兆子癇高血壓時,因胎盤減壓物質產生減少,故可使兩者失去平衡;③可產生和釋放組織因子(凝血因子Ⅲ)而引起DIC,當腎小球微血管中出現DIC時,可導致小球濾過率嚴重減少而發生水瀦留。
4.主動脈狹窄引起的高血壓高血壓可由於主動脈狹窄所引起。例如可見於先天性主動脈狹窄(coarctation of aorta)。此時,心臟收縮代償性加強,而射出的血液又不能順利通過狹窄部,致使大量血液蓄積在容量有限的狹窄部近心端的主動脈及其分支中,因而使狹窄部近心端的上肢以上的動脈血壓升高,而下肢血壓不高;尤其當運動時,由於心輸出量的增加,可使其收縮壓突然升高,此外,曾有人提出主動脈縮窄時,起源於縮窄部遠心端的腎動脈可能因血灌流不足而引起腎缺血,從而促使腎素的分泌增多,但尚無有力的根據。
5.收縮期高血壓 凡收縮壓≥21.3kPa(≥160mmHg)而舒張壓<12.7kPa(<95mmHg)者,則可定為收縮期高血壓。單純收縮期高血壓在老年人最常見,尤其超過55歲的婦女。這是由於動脈硬化(主要是粥樣硬化)使大動脈順應性降低所致;主要表現是脈壓增寬,左室射血速率和心臟指數降低,總血管外周阻力增高。少數收縮期高血壓繼發於主動脈瓣關閉不全、嚴重貧血和甲狀腺機能亢進時,主要表現是左室射血速率和心臟指數增高,但總血管外周阻力正常。
總之,①繼發性高血壓發生的原因和機制比較簡單,最先多是由於某個參與調壓機制的環節(如腎、腎上腺或垂體)發生障礙的結果;②由於各種調壓機制之間常是相互聯繫著,在高血壓的發生中,一個加壓機制的激活,常可導致另一個加壓機制的激活(如交感神經興奮→腎素分泌↑→血管緊張素↑)或者通過負反饋作用,一個加壓機制的激活又對另一個加壓機制起著抑制作用(如鹽皮質激素↑→血容量↑→腎素↓);這樣,繼發性高血壓一旦發生後,其發展過程又表現出一定的複雜性;③一般認為,不管引起繼發性高血壓的始動機制如何,腎對鈉水排泄能力的降低,是維持各種繼發性高血壓的重要機制,故利尿,排鈉對不同種類的繼發性高血壓都有明顯的降壓效果。
參看
| 關於「病理生理學/繼發性高血壓」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |