臨床生物化學/缺血性冠狀動脈疾病的酶學診斷
| 醫學電子書 >> 《臨床生物化學》 >> 診斷酶學 >> 缺血性冠狀動脈疾病的酶學診斷 |
| 臨床生物化學 |
|
|
|
缺血性冠狀動脈疾病包括了心絞痛和急性心肌梗死(AMI)等疾病,其中AMI是西方已開發國家主要死因之一。近年來隨經濟發展人們生活水平提高,此病在我國發病率明顯增加,早期診斷、適當治療對於減低此病死亡率和合併症是極其重要的。
WHO在1997年提出診斷AMI三個面的依據:即第一,臨床表現和症状主要為胸部劇烈疼痛;第二,心電圖上特異改變,如出現Q波;第三,血清中有關酶濃度出現升高下降的動態過程。一般認為患者具有三大表現中任何兩項都可診斷為AMI。目前一些AMI患者可以缺乏典型胸痛症状,臨床上稱為寂靜型AMI(silentAMI),國外文獻認為此種類型約佔1/4AMI患者。此類患者多見於老年人,尤其是糖尿病患者。另外一些AMI患者心電圖檢查查不到AMI特有的Q波,病理檢查時這些患者的壞死病變不累及或少累及心臟外層,臨床上常稱為內膜下或非穿壁性心梗。目前更多使用「無Q波心梗」術語取代上述名詞,其發病率約佔總AMI的1/3,這樣血清中有關酶濃度的動態變化對AMI診斷具有了較特殊價值,是診斷和鑒別診斷AMI的重要依據。
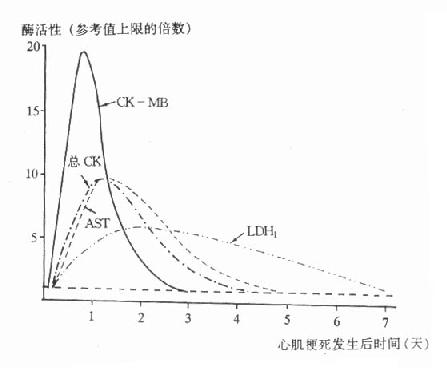
圖7-2 血清酶在單純性AMI後的變化
圖7-2 是AMI患者血清酶濃度的典型變化圖:
從圖7-2可以看到AMI時,任何酶變化都有一個延遲期,也就是說出現心肌梗死時雖然酶已釋放到細胞外,但由於病變局部沒有血液通過,釋放的酶需經由系統緩慢進入血液,大約在4-8小時後,血清酶活性才開始超過參考範圍的上限值。在常測酶中首先升高的是CK-MB,升高程度可高達參考值上限的10-25倍,由於骨骼肌中也含有少量CK-MB,但不超過5%,所以臨床上更多地願意用CK-KB佔總CK的百分比(<6%)來診斷AMI。CK-MM或者說總CK變化類似CK-MB,但升高和恢復正常都略遲,常在AMI發病8-12小時後才開始升高,24-48小時達到峰值,總酶升高持續7天,LD1持續時間更長達10天,升高程度較低,一般為參考上限的3-4倍。由於心肌中的LD主要為LD1,因此在理論上LD1診斷特異性更高,但這二者的測定都受到溶血干擾,輕度溶血就有可能引起血清LD和LD1非病理性升高,臨床上應用此酶必須注意此點。
在我國醫院實驗室,往往還將天冬氨酸氨基轉移酶(AST)和羥丁酸脫氫酶(HBDH)和上述兩種酶作為一組測定項目,用於論斷AMI。但從圖可以看出總AST測定對論斷AMI毫無優點,當AST升高時幾乎無一例外都伴有CK/或LD升高,如果考慮到AST還大量存在於其它器官,如肝、肌肉內,其測定特異性明顯低於CK。
至於HBDH實際上並不存在此種酶,所測的仍是LD的活性,只在當以酮丁酸取代丙酮酸為底物測LD活性時,LD1比其它同工酶對酮丁酸有更大活性,所測結果更能反映出LD1的活性。隨著有更好方法,如電泳法、免疫法和化學抑製法測LD同工酶,已無必要再測定此酶以診斷AMI。
隨科學技術發展,人們對缺血性冠狀動脈疾病的發病機制、分類和治療有了進一步認識:冠狀動脈粥樣硬化開始於血管壁上出現富含膽固醇及其酯類的脂肪條紋,病變進一步增大成為粥樣硬化斑(atheroma),斑塊可以大部分阻塞血管內腔,限制血流,勞累後由於心肌供氧不足,引起心區疼痛,而在休息後或者用血管擴張藥後得到緩解,這就是典型的穩定型心絞痛症状。斑塊的變化是多種多樣的,斑塊可鈣化變得僵硬和易碎,部分斑塊可能進入血流引起下面小血管栓塞,在動脈壁上由於斑塊脫落形成潰瘍,血小板聚集在潰瘍面,釋放出強有力的血管收縮因子如TBX-2,有可能在血小板聚集基礎上形成血栓,阻塞血流,引起供血障礙,心肌組織病變乃至壞死,出現典型的AMI症状。
栓塞形成後,可能激活體內的溶栓系統活性,促使血栓溶解,血液又重新灌注(reperfusion),但此過程往往已在梗死發生後較長時間後才發生,此時心肌組織已經壞死,如果溶栓出現在心梗發生後6小時內,病變心肌組織有可能不壞死,病變轉逆。目前治療AMI廣泛在早期應用溶栓藥,如尿激酶、鏈激酶、組織型纖溶酶原激活劑等,防止心肌壞死形成瘢痕。這些新療法的出現對實驗室提出一些新的要求,如要求早期診斷AMI,用常規測酶方法常不易達到此要求,因為發病後4-6小時正相當這些酶的延遲期,CK同工酶亞型的發現為早期診斷AMI提供新的可能性。
80年代以來發現CK同工酶MM和MB雖然都各由基因位點控制形成組織型的CK-MM3和CK-MB2,但它們釋放入體液後在體液中羧基肽酶作用下,分解M亞基羧基端的賴氨酸,改變了MM3和MB2的等電點,可以進一步分為不同亞型(isoform),即CK-MM3可進一步變為電泳速度較快的MM2和MM1,CK-MB2變為MB1。正常血清中亞型含量分別為MM1>MM2>MM3,MB1>MB2,但當AMI時由於組織型MM3和MB2大量釋放入血,MM3/MM1和MB2/MB1,比值超過1.0,此變化明顯早於CK和CK-MB升高。MB2/MB1在AMI發病後1.5小時達到峰值,MM3/MM1則在3小時達到峰值,Wu在最近提出早期診斷首選的是CK亞型和肌紅蛋白,確診Ami則仍以CK-MB以及最近提出的肌鈣蛋白(troponin)為佳,晚期則選用LD和肌鈣蛋白。
另一較大進展是使用免疫學方法測CK-Mb的質量(μg/L),而不是用經典方法測CK-MB的活性濃度(U/L)。特別是使用抗CK-MB單克隆血清合併化學發光技術,不僅靈敏度很高,檢出值為0.8μg/L,操作簡單,時間短,特別適合於急症標本。在已開發國家已逐步取代其方法成為測定MB的主要方法,臨床上也常以CK-MB指數>6%來診斷AMI,指數按下式計算CK-MB(μg/L)/CK(U/L)。最近有人報告用酶聯法測糖原磷酸化酶BB同工酶的質量和CK、CK-MB、肌紅蛋白以及肌鈣蛋白,比其早期診斷AMI靈敏度高。
使用溶栓藥後,需了解用藥是否有效,即是否出現再灌注。冠狀動脈血管造影是判斷是否出現再灌注可靠的方法,但需一定設備,並且是一種損傷性檢查,臨床醫師往往可以根據酶峰值出現時間提早來診斷,如栓塞溶解,出現再灌注,血液通過梗塞部分,可將釋放到病變組織中的酶沖洗到血中,酶峰值出現變早。
從冠狀動脈粥樣硬化的病變和血栓形成、溶栓過程的動態變化,不難理解在典型的心絞痛和心肌梗死之間還存在著各種過渡的病變。例如在按WHOAMI診斷標準未能診斷AMI患者死亡時,可發現有小灶性壞死病變。
最近提出一個的分類,將此類伴有壞死病變的缺血性心臟疾病命名為IMD(ischemicmyocardialdamage)缺血性心肌損傷,包括兩類疾病:一類是符合WHO診斷標準的AMI,另一類缺乏典型心電圖和酶學變化,但靈敏的心肌損傷指標如肌損傷MMD(mi-normyocardialdamage)。
另一方面心絞痛發作可不僅限於勞累時,一部分患者在安靜時也可以出現心絞痛,其中一部分還可以進一步發展為AMI和出現猝死。臨床上將其分類為不穩定型心絞痛,目前認為TnT和CK-MB質量測定有助於臨床判斷這些患者的預後,一些臨床醫師主張對這些患者開展一些較積極的抗凝或溶栓治療。
最近發現一些心肌蛋白可作為心肌損傷的較好指標,尤其是TnT和肌鈣蛋白I(TnI)。肌鈣蛋白是由三個亞單位組成(TnT,TnI和TnC),它們為心肌的調節單位,在控制心肌收縮中起著重要作用,心肌TnT和TnI的抗原性與骨骼肌有明顯差異,可以得到特異性很高的單克隆血清。由於血清中濃度很低,TnT一般不超過0.1μg/L,心肌病變時可成百倍升高,由於分子量較小,升高出現時間都長。目前用TnT診斷AMI,判斷不穩定型心絞痛患者預後的價值已為臨床所公認,但也發現在腎透析患者血中可有不明原因TnT濃度升高。TnI臨床價值仍在探索中,有望成為另一靈敏的心肌損傷指標。
| 關於「臨床生物化學/缺血性冠狀動脈疾病的酶學診斷」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |