阿法替尼
| A+醫學百科 >> 阿法替尼 |
 |
|
|---|---|
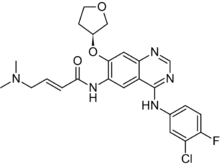
| IUPAC命名 | |
| N-[4-[(3-Chloro-4-fluorophenyl)amino]-7-[[(3S)-tetrahydro-3-furanyl]oxy]-6-quinazolinyl]-4(dimethylamino)-2-butenamide | |
| 識別 | |
| CAS號 | 439081-18-2 |
| ATC編碼 | L01XE13 |
| PubChem | CID 10184653 |
| ChemSpider | 8360155 |
| UNII | 41UD74L59M |
| ChEBI | CHEBI:61390 |
| ChEMBL | CHEMBL1173655 |
| 異名 | BIBW 2992 |
| 化學性質 | |
| 化學式 | C24H25ClFN5O3 |
| 分子量 | 485.937 g/mol |
| SMILES | 搜尋Jmol 3D模型,eMolecules,PubChem |
|
|
| 藥代動力學性質 | |
| 生物利用度 | 92%[1] |
| 蛋白結合 | 95% |
| 代謝 | CYP not involved |
| 半衰期 | 37 hours |
| 排泄 | Faeces (85%), urine (4%) |
| 治療考量 | |
| 許可資料 | EMA:連結, US FDA:連結 |
| 懷孕分級 | C (澳) D (美) |
| 合法狀態 | 限醫師處方 (S4) (澳) ℞-only (加) POM (英) ℞-only (美) |
| 途徑 | Oral |
阿法替尼(英語:Afatinib),是一種創新的抗癌標靶治療藥物,即新一代口服標靶藥,為全球首種不可逆轉地結合ErbB家族(包含四種不同的癌細胞表皮生長因子受體,如 EGFR、HER2、 ErbB3 及 ErbB4)的抗癌標靶藥,進而更有效地及針對性地阻斷引發癌細胞生長的訊號,減少或延緩癌細胞的增生。阿法替尼已在美國、歐洲和台灣多國家地區獲批用作為一線治療藥物[2] ,應用於具有表皮生長因子受體(英語:EGFR)突變癌細胞的非小細胞肺癌(英語:NSCLC)治療,是每日一次的口服標靶治療藥物。
阿法替尼由德國藥廠勃林格殷格翰研發,經過多項大型臨床驗証,被FDA評為突破性治療[3]。世界權威學術雜誌《自然》亦指出「阿法替尼」於2013年成為全球正面的頭條新聞之一。阿法替尼於2013年在美國及歐洲上市,商品名稱分別為「Gilotrif」及 「Giotrif」;中文商名在台灣及香況分別為「妥復克」及「標必達」(英語:Giotrif),香港及中國的正式批刻使用現正於審核中[4]。
通過抑壓上述ErbB家族的信號傳導,對於防止腫瘤生長和擴散擔當關鍵性的角色。阿法替尼的作用能不可逆轉地與ErbB家族受體結合,中斷下游信息傳導,從而阻止癌細胞生長,並誘導癌細胞凋亡(程序性死亡)。 因此,相比其他標靶藥物,阿法替尼與ErbB家族受體不可逆轉地結合的特性能夠提供更具持久、選擇性、共價及完全地中斷通過癌細胞的信息傳導,從而帶來獨特的抗癌治療效益,更具潛力去抑制廣泛類別的腫瘤細胞增長,其療效亦更顯注[5][6][7]。
目錄 |
作用機制
阿法替尼為不可逆轉的ErbB家族阻斷劑,能抑壓信息傳導和阻隔與癌細胞生長和分裂相關的主要通道。由於通過ErbB家族信息傳導機制可由多個同二聚體跟異二聚體引發,所以同時抑制多個ErbB家族成員(如 EGFR, HER2, ErbB3 及 ErbB4),能較有效地中斷下游信息傳導[8]。
於癌細胞中,ErbB家族的運作經常失調。當控制細胞生長機制的因子過度表現或運作異常,有機會引發各種實質固態腫瘤。受體過度表現會刺激細胞內部信息傳導超越正常水平,引致不受控的腫瘤細胞增長、遷移和轉移及抑制其凋亡[9]。引發以上細胞信息傳導異常的情況有以下各種不機制﹕受體變異(例如﹕肺癌腫瘤EGFR變異)、受體過度表現(例如﹕乳癌腫瘤HER2過度表現)或配體(ligand)過度表現[10]。
審批和使用
基於在臨床研究的取得突破性療效結果,阿法替尼早前被納入美國食品及藥物管理局(FDA)優先審核流程[11]。FDA優先審核流程將為那些安全、有效、尚無滿意的替代治療選擇、而且相較於目前上市的產品具有顯著改善優勢的藥物提供快速審核的通道,以加快提供突破性的藥物予有需要的患者。
阿法替尼於 2013年7月12日獲美國食品及藥物管理局(FDA)核准上市,作為新型一線治療藥物,應用於通過經FDA批准的檢測方法檢出存在表皮生長因子受體(EGFR)外顯子19缺失突變或外顯子21(L858R)替代突變的轉移性非小細胞肺癌(NSCLC)患者[12]。
歐盟藥物管理機構(European Medicines Agency)亦於2013年7月25日核准「阿法替尼」用於醫治因表皮生長因子受體(EGFR)突變的非小細胞肺癌(NSCLC)患者[13]。
中華民國行政院衛生署食品藥物管理局(TFDA)亦早於2013年5月17日搶先核准阿法替尼藥物上市[14]。
主要研究發展
肺癌
LUX-Lung臨床研究計劃,現正探討阿法替尼用於中晚期非小細胞肺癌患者的療效。兩個關鍵性的第三期研究﹕LUX-Lung 3(n=345)和LUX-Lung 6(n=364)為至今最大、最有力和最貫徹始終的臨床註冊研究計劃,針對因EGFR突變而導致的晚期非小細胞肺癌。於2013年,LUX-Lung 3研究結果在臨床腫瘤學雜誌(Journal of Clinical Ontology)刊出[15][16],而LUX-Lung 6研究結果則在美國臨床腫瘤學會(ASCO)周年會議上發表[17][18]。
美國臨床腫瘤醫學會(ASCO)官方年會發表的數據證明[19][20],病人經過嶄新試驗性化合物阿法替尼治療後長達一年時間,其腫瘤才恢復生長,相反那些接受化學治療 (吉西他濱gemcitabine / 順鉑cisplatin)的病人,不到六個月後腫瘤便複發。經過獨立審查的腫瘤評估數據顯示,阿法替尼的無疾病惡化存活期(PFS)是11個月, 相比化療的PFS只有5.6個月更為優勝。此外,接受阿法替尼治療的病人,接近一半(47%)於療程一年後依然生存而且病情無惡化,而接受化療的病人卻只有2%維持這個狀況。
作為LUX-Lung臨床研究計劃一部分,現時其有八項研究同時進行中,研究項目的設計皆以分析「亞法替尼」在中晚期非小細胞肺癌各種環境的療效(包括出現EGFR突變的非小細胞肺癌患者和持續患病的患者)為目標。
其他癌症
阿法替尼亦被選作多種腫瘤類別研究用途[21],現正進行頭頸癌等的晚期臨床試驗。
研究資料總覽
療效和安全性
LUX-Lung 3與LUX-Lung 6是多中心臨床試驗、隨機化及開放標示的第三期研究,旨在比較「阿法替尼」和化療(分別為培美曲塞pemetrexed/順鉑cisplatin 和吉西他濱gemcitabine / 順鉑cisplatin),用作一線治療患上中晚期轉移性、因EGFR突變的非小細胞肺癌患者[22] [23]
這些關鍵性的第三期研究提出有力證據顯示阿法替尼相對傳統化療(分別為培美曲塞/順鉑和吉西他濱/ 順鉑),療效更加卓越。此外,兩份研究報告一致證明「阿法替尼」的療效和安全性,進一步增強大家對研究成果的信心。
綜合LUX-Lung 3與LUX-Lung 6的主要研究結果[24][25][26][27][28][29]
無惡化存活期 (PFS - 患者存活並且腫瘤沒有再重新生長的時間)
| LUX-Lung 3 (阿法替尼 vs 培美曲塞pemetrexed/順鉑cisplatin ) | ! LUX-Lung 6 (阿法替尼 vs 吉西他濱gemcitabine / 順鉑cisplatin ) |
|---|---|
| 根據獨立審查,所有出現表皮生長因子受器變種的患者(總數=345)﹕ 11.1個月 vs 6.9個月 | 根據獨立審查,所有出現表皮生長因子受器變種的患者﹕11個月vs 5.6個月 |
| 根據獨立審查,小組群中出現最常見變種的患者(總數=308,即病人總數90%,del19和L858R)﹕13.6個月vs 6.9個月 | 根據調查員審查,接受「亞法替尼」治療的患者存活超過一年後,其腫瘤才恢復生長﹔相比之下,接受傳統化療的存活不過半年(無惡化存活期13.7個月vs 5.6個月) |
| 此外,接受「阿法替尼」治療的患者有47%在療程一年後仍然活著而並腫瘤無惡化,而接受傳統化療的患者出現同樣狀況的只有2%。 |
兩個研究一致顯示「阿法替尼」延遲腫瘤生長的功效,證明其療效顯著及研究資料可靠。
客觀反應 (腫瘤萎縮)
| LUX-Lung 3 (阿法替尼 vs 培美曲塞pemetrexed/順鉑 cisplatin ) | LUX-Lung 6 (阿法替尼 vs 吉西他濱gemcitabine / 順鉑cisplatin ) |
|---|---|
| 根據獨立審查,每兩名接受亞法替尼療程的患者中,有一位(56%)腫瘤萎縮,相比接受傳統化療的,四名患者中只有一位(23%)的情況有明顯改善。 | 根據獨立審查,67%接受「阿法替尼」療程的患者,其腫瘤體積大為萎縮,只有23% 接受傳統化療的患者情況有如此大幅改善。 |
腫瘤萎縮亦有助改善疾病有關的徵狀。
與疾病有關的徵狀
兩個研究結果均證明,較多接受「阿法替尼」療程的患者,病徵如呼吸困難、咳嗽和胸痛均得到改善。此外,「阿法替尼」療程有助延遲這些徵狀出現。
生活質素 (患者問卷統計)
LUX-Lung 6與LUX-Lung 3的研究結果,一致證明接受「阿法替尼」療程的患者相比接受傳統化療的患者,享有更高的生活質素(例如﹕工作和日常起居活動)。
Grade =3不良事件
| LUX-Lung 3 (阿法替尼 vs 培美曲塞pemetrexed/順鉑cisplatin ) | LUX-Lung 6 (阿法替尼 vs 吉西他濱gemcitabine / 順鉑cisplatin ) |
|---|---|
| 接受「阿法替尼」療程後,最常見因藥物引發的不良反應包括肚瀉、皮膚過敏和甲溝炎 | 接受「阿法替尼」療程後,最常見因藥物引發的不良反應包括肚瀉、過敏/痤瘡、和口腔炎/口腔黏膜炎。 |
| 接受化療後,最常見因藥物引發的不良反應包括頭暈嘔吐,食慾下降和疲倦。 | 接受化療後,最常見因藥物引發的不良應包括嗜中性白血球低下(嗜中性白血球是白血球的一種,患者體內這種白血球數量不正常偏低)、嘔吐和白細胞減少症(患者體內白血球數量減少)。 |
| 因不良反應中止療程的比率偏低(阿法替尼的中止率為8%﹔化療的為12%)。 | 因不良反應而中止「阿法替尼」療程的患者比率為6%,而中止化療的患者比率為40%。 |
| 接受「阿法替尼」治療的患者中,有1%因肚瀉而停止療程。 | 接受「阿法替尼」療程的患者,很少因藥物不良反應而中止療程,其中只有2%因過敏/痤瘡中止療程,當中沒有病人因肚瀉而中止療程。 |
耐受性
「阿法替尼」的副作用大致上可管理和逆轉的。直致目前為止,研究顯示藥物引致的不良反應大部分涉及腸胃(如肚瀉)和皮膚(如過敏),這跟表皮生長因子受器酪胺酸激脢抑制劑有關。[30][31][32][33]
臨床潛力
信號傳導抑制劑為癌症研究中一個主要發展目標。「阿法替尼」其獨特不可逆轉結合的功能與具選擇性地阻斷癌細胞信息傳導作用,可能有助改善多種癌細胞的抑制能力,從 而擴大癌症藥物的潛在療效。
現時發展階段顯示,「阿法替尼」可能優勝過其他耐受性相若(40mg劑量)的信號傳導抑制劑。目前仍有很多有關「阿法替尼」的研究計劃正在進行中,於未來將會提供更多臨床資料,鞏固「阿法替尼」於癌症治療的效用。
參考文獻
- ↑ Gilotrif (afatinib) dosing, indications, interactions, adverse effects, and more. Medscape Reference. WebMD [28 January 2014].
- ↑ Dungo RT, Keating GM.Drugs. 2013 Sep;73(13):1503-15.
- ↑ FDA Website. http://www.fda.gov/downloads/aboutfda/reportsmanualsforms/reports/userfeereports/performancereports/pdufa/ucm384035.pdf. Accessed in Feb 2014.
- ↑ http://www.worldpharmanews.com/boehringer-ingelheim/2318-fda-grants-priority-review-to-boehringer-ingelheims-afatinib-nda-for-egfr-mutation-positive-advanced-nsclc
- ↑ Hynes NE, MacDonald G. ErbB receptors and signalling pathways in cancer. Curr Opin Cell Biol 2009; 21:177-84.
- ↑ Reid A, Vidal L, Shaw H, do Bono J.Dual inhibition of ErbB1 (EGFR/HER1) and ErbB2 (HER2/neu). Eur J Cancer 2007;43:481-9.
- ↑ Solca F, Dahl G, Zoephel A, et al. Target binding properties and cellular activity of afatinib (BIBW 2992), an irreversible ErbB family blocker. J Pharmacol Exp Ther 2012;343:342-50.
- ↑ Reid A, Vidal L, Shaw H, do Bono J.Dual inhibition of ErbB1 (EGFR/HER1) and ErbB2 (HER2/neu). Eur J Cancer 2007;43:481-9.
- ↑ Hanahan D, Weinberg RA. The Hallmarks of Cancer. Cell,100(1), pp.57-70.
- ↑ Wieduwilt MJ, Moasser MM. The epidermal growth factor receptor family: biology driving targeted therapeutics. Cell Mol Life Sci 2008;65:1566-84.
- ↑ Drugs.com. U.S. FDA Grants Priority Review to Boehringer Ingelheim's Afatinib NDA for EGFR Mutation-Positive Advanced NSCLC. http://www.drugs.com/nda/afatinib_130115.html. Accessed on Feb 2014.
- ↑ U.S. Food and Drug Administration website: http://www.fda.gov/Drugs/InformationOnDrugs/ApprovedDrugs/ucm360574.htm. Accessed in Feb 2014.
- ↑ European Medicines Agency: http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/human/002280/WC500152394.pdf. Accessed in Feb 2014.
- ↑ 中央廣播電台. http://news.rti.org.tw/index_newsContent.aspx?nid=424830. Accessed in Feb 2014.
- ↑ Yang J, Hirsh V, Schuler M, et al. Symptom Control and Quality of Life in LUX-Lung 3: A Phase III Study of Afatinib or Cisplatin/Pemetrexed in Patients With Advanced Lung Adenocarcinoma With Epidermal Growth Factor Receptor Mutations. J Clin Oncol 2013;DOI: 10.1200/JCO.2012.46.1764
- ↑ Sequist L, Yang J, Yamamoto N, et al. Phase III Study of Aaftinib or Cisplatin Plus Pemetrexed in Patients With Metastatic Lung Adenocarcinoma With Epidermal Growth Factor Receptor Mutations. J Clin Oncol 2013;DOI: 10.1200/JCO.2012.44.2806
- ↑ Wu, Y., MD. LUX-Lung 6: A randomized, open-label, Phase III study of afatinib (A) vs. gemcitabine/cisplatin (GC) as first-line treatment for Asian patients (pts.) with EGFR mutation-positive (EGFR M+) advanced adenocarcinoma of the lung. (Abstract #8016) at American Society of Clinical Oncology, Chicago, June 2, 2013.
- ↑ Geater, SL, MD. LUX-Lung 6: Patient reported outcomes (PROs) from a randomized open-label, Phase III study in 1st-line advanced NSCLC patients (pts.) harbouring epidermal growth factor receptor (EGFR) mutations. Poster (Abstract #8061) at American Society of Clinical Oncology, Chicago, June 1, 2013.
- ↑ Agus DB, Terlizzi E, Stopfer P, et al. A Phase I dose escalation study of BIBW 2992, an irreversible dual EGFR/HER2 receptor tyrosine kinase inhibitor, in a continuous schedule in patients with advanced solid tumors. J Clin Oncol 2006;24(18,Suppl):Abstract 2074.
- ↑ Mom CH, Eskens FA, Gietema JA, et al. Phase 1 study with BIBW 2992, an irreversible dual tyrosine kinase inhibitor of Epidermal Growth Factor Receptor 1 (EGFR) and 2 (HER2) in a 2 week on 2 week off schedule. J Clin Oncol 2006;24(18,Suppl):Abstract 3025.
- ↑ Li D, Ambrogio L, Shimamura T, et al. BIBW2992, an irreversible EGFR/HER2 inhibitor highly effective in preclinical lung cancer models. Oncogene 27:4702-11.
- ↑ Yang J, Hirsh V, Schuler M, et al. Symptom Control and Quality of Life in LUX-Lung 3: A Phase III Study of Afatinib or Cisplatin/Pemetrexed in Patients With Advanced Lung Adenocarcinoma With Epidermal Growth Factor Receptor Mutations. J Clin Oncol 2013;DOI: 10.1200/JCO.2012.46.1764
- ↑ Wu, Y., MD. LUX-Lung 6: A randomized, open-label, Phase III study of afatinib (A) vs. gemcitabine/cisplatin (GC) as first-line treatment for Asian patients (pts.) with EGFR mutation-positive (EGFR M+) advanced adenocarcinoma of the lung. (Abstract #8016) at American Society of Clinical Oncology, Chicago, June 2, 2013.
- ↑ Yang J, Hirsh V, Schuler M, et al. Symptom Control and Quality of Life in LUX-Lung 3: A Phase III Study of Afatinib or Cisplatin/Pemetrexed in Patients With Advanced Lung Adenocarcinoma With Epidermal Growth Factor Receptor Mutations. J Clin Oncol 2013;DOI: 10.1200/JCO.2012.46.1764
- ↑ Sequist L, Yang J, Yamamoto N, et al. Phase III Study of Aaftinib or Cisplatin Plus Pemetrexed in Patients With Metastatic Lung Adenocarcinoma With Epidermal Growth Factor Receptor Mutations. J Clin Oncol 2013;DOI: 10.1200/JCO.2012.44.2806
- ↑ Wu, Y., MD. LUX-Lung 6: A randomized, open-label, Phase III study of afatinib (A) vs. gemcitabine/cisplatin (GC) as first-line treatment for Asian patients (pts.) with EGFR mutation-positive (EGFR M+) advanced adenocarcinoma of the lung. (Abstract #8016) at American Society of Clinical Oncology, Chicago, June 2, 2013.
- ↑ Geater, SL, MD. LUX-Lung 6: Patient reported outcomes (PROs) from a randomized open-label, Phase III study in 1st-line advanced NSCLC patients (pts.) harbouring epidermal growth factor receptor (EGFR) mutations. Poster (Abstract #8061) at American Society of Clinical Oncology, Chicago, June 1, 2013.
- ↑ Plummer R, Vidal L, Li L, et al. Phase I study of BIBW2992, an oral irreversible dual EGFR/HER2 inhibitor, showing activity in tumours with mutated EGFR. Eur J Cancer Suppl 2006;4(12):173-4 (Abstract 573).
- ↑ Agus DB, Terlizzi E, Stopfer P, et al. A Phase I dose escalation study of BIBW 2992, an irreversible dual EGFR/HER2 receptor tyrosine kinase inhibitor, in a continuous schedule in patients with advanced solid tumors. J Clin Oncol 2006;24(18,Suppl):Abstract 2074.
- ↑ Plummer R, Vidal L, Li L, et al. Phase I study of BIBW2992, an oral irreversible dual EGFR/HER2 inhibitor, showing activity in tumours with mutated EGFR. Eur J Cancer Suppl 2006;4(12):173-4 (Abstract 573).
- ↑ Agus DB, Terlizzi E, Stopfer P, et al. A Phase I dose escalation study of BIBW 2992, an irreversible dual EGFR/HER2 receptor tyrosine kinase inhibitor, in a continuous schedule in patients with advanced solid tumors. J Clin Oncol 2006;24(18,Suppl):Abstract 2074.
- ↑ Mom CH, Eskens FA, Gietema JA, et al. Phase 1 study with BIBW 2992, an irreversible dual tyrosine kinase inhibitor of Epidermal Growth Factor Receptor 1 (EGFR) and 2 (HER2) in a 2 week on 2 week off schedule. J Clin Oncol 2006;24(18,Suppl):Abstract 3025.
- ↑ Eskens FA, Mom CH, Planting AS, et al. A Phase I dose escalation study of BIBW 2992, an irreversible tyrosine kinase inhibitor of epidermal growth factor receptor 1 (EGFR-1) and 2 (HER 2) in a 2 week on 2 week off schedule in patients with advanced solid tumors. Poster A235 presented at AACR-NCI-EORTC International Conference on Molecular Targets and Cancer Therapeutics, Philadelphia, PA, USA, 14-18 November 2005.
|
||||||||||||||||||||||||
參考來源
| 關於「阿法替尼」的留言: | |
給阿法替尼條目的留言--印度緣生堂 2017年10月6日 (五) 14:36 (CST) 留言: 阿法替尼 QQ2087828428 | |
| 添加留言 | |