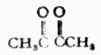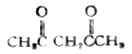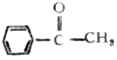醫用化學/醛和酮
| 醫學電子書 >> 《醫用化學》 >> 醛、酮、醌 >> 醛和酮 |
| 醫用化學 |
|
|
目錄 |
一、醛和酮的構造
羰基與一個氫原子和一個烴基相連的化合物叫做醛(甲醛例外,它的,羰基與兩個氫原子相連),可用通式表示![]()
。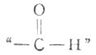 」稱為醛基,是醛的官能團,可簡寫為-CHO,它位於碳鏈的一端。
」稱為醛基,是醛的官能團,可簡寫為-CHO,它位於碳鏈的一端。
羰基與兩個烴基相連的化合物叫做酮,可用通式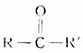 表示。酮的官能團
表示。酮的官能團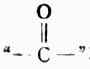
稱為酮基,位於碳鏈中間。在一元酮中,兩個烴基相同的叫單酮,兩個烴基不同的叫做混酮。
羰基中的碳原子為sp2雜化,其中一個sp2雜化軌道與氧原子的一個p軌道按軸向重疊形成σ鍵;碳原子未參與雜化的p軌道與氧原子的另一個p軌道平行重疊形成π鍵。因此,羰基碳氧雙鍵是由一個σ鍵和一個π鍵組成的。
由於氧原子的電負性比碳原子大,因此羰基中π電了雲偏向於氧原子一邊,使羰基碳原子帶有部分正電荷,而氧原子則帶有部分負電荷。羰基的極化情況可表示如下:
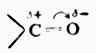
二、醛和酮的命名
(一)普通命名法
簡單的脂肪醛按分子中的碳原子的數目,稱為某醛。例如:
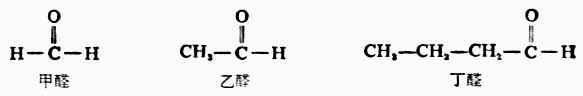
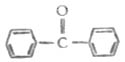
簡單的酮可按羰基所連接的兩上烴基命名。例如:
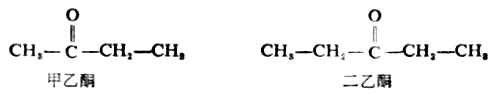
(二)系統命名法
對構造比較複雜的醛、酮則用系統命名法命名。命名時先選擇包括羰基碳原子在內的最長碳鏈作主鏈,稱為某醛或某酮。從醛基一端或從靠近酮基一端開始把主鏈中碳原子編號。由於醛基一定在碳鏈的鏈端,故不必用數字標明其位置,但酮基的位置必須標明,寫在酮名的前面。主鏈上如有支鏈或取代基,應標明位次,把它的位次(按次序規則)、數目、名稱寫在某醛、某酮的前面。主鏈中碳原子的編號也可以用希臘字母表示,即把與羰基碳直接相連的碳原子用α表示,其它碳原子依次為β,γ…
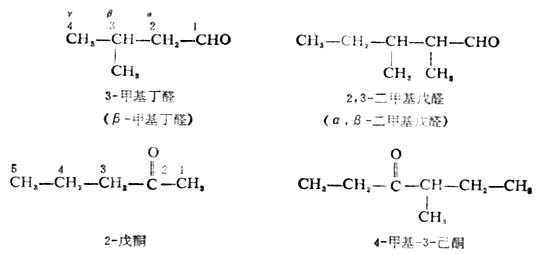
命名不飽和醛、酮則需標出不飽和鍵和羰基的位置。
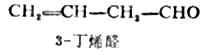
多元醛、酮命名時,同樣選擇包括羰基碳原子在內的最長碳鏈作為主鏈,編號時使羰基位置數字最小,同時加上用漢字數字表示的羰基數目。
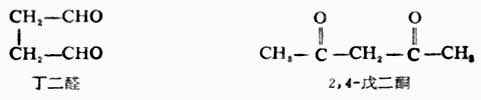
芳香醛、酮的命名,是以脂肪醛、酮為母體,芳香烴基作為取代基。
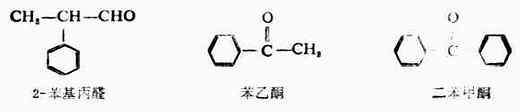
三、醛、酮的物理性質
在常溫下,除甲醛是氣體外,12個碳原子以下的脂肪醛、酮都是液體,高級脂肪醛、酮和芳香酮多為固體。
由於醛或酮分子之間不能形成氫鍵,沒有締合現象,故它們的沸點比相對分子質量相近的醇低。但由於羰基的極性,增加了分子間的引力,因此沸點較相應的烷烴高。如表15-1所示。
表15-1 相對分子質量相近的烷、醇、醛、酮的沸點
| 名稱 | 正戊烷 | 正丁醇 | 丁醛 | 丁酮 |
| 相對分子質量 | 72 | 74 | 72 | 72 |
| 沸點/℃ | 36.1 | 117.7 | 74.7 | 79.6 |
醛、酮羰基上的氧可以與水分子中的氫形成氫鍵,因而低級醛、酮(如甲醛、乙醛、丙酮等)易溶於水,但隨著分子中碳原子數目的增加,它們的溶解度則迅速減小。醛和酮易溶於有機溶劑。一些醛、酮的物理常數見表15-2。
表15-2一些醛、酮的物理常數
| 名稱 | 構造式 | 熔點/℃ | 沸點/℃ | 相對密度 | 溶解度g.(100H2O)-1 |
| 甲醛 | HCHO | -92 | -19.5 | 0.815 | 55 |
| 乙醛 | CH3CHO | -123 | 20.8 | 0.781 | 溶 |
| 丙醛 | CH3CH2CHO | -81 | 48.8 | 0.807 | 20 |
| 丁醛 | CH3CH2CH2CHO | -97 | 74.7 | 0.817 | 4 |
| 乙二醛 |
|
15 | 50.4 | 1.14 | 溶 |
| 丙烯醛 | CH2=CHCHO | -87.7 | 53 | 0.841 | 溶 |
| 苯甲醛 |
|
-26 | 179 | 1.046 | 0.33 |
| 丙酮 | CH3COCH3 | -95 | 56 | 0.792 | 溶 |
| 丁酮 | CH3COCH2CH3 | -86 | 79.6 | 0.805 | 35.3 |
| 2-戊酮 | CH3COCH2CH2CH3 | -77.8 | 102 | 0.812 | 幾乎不溶 |
| 3-戊酮 | CH3CH2COCH2CH3 | -42 | 102 | 0.814 | 4.7 |
| 環己酮 |
|
-16.4 | 156 | 0.942 | 微溶 |
| 4-甲基-3-戊烯-2-酮 | (CH3)2C=CHCOCH3 | -59 | 130 | 0.865 | 溶 |
| 丁二酮 |
|
-2.4 | 88 | 0.980 | 25 |
| 2,4-戊二酮 |
|
-23 | 138 | 0.792 | 溶 |
| 苯乙酮 |
|
19.7 | 202 | 1.026 | 微溶 |
| 二苯甲酮 |
|
48 | 306 | 1.098 | 不溶 |
四、醛、酮的化學性質
醛、酮的化學性質主要決定於羰基。由於構造上的共同特點,使這兩類化合物具有許多相似的化學性質。但是醛與酮的構造並不完全相同,使它們在反應性能上也表現出一些差異。一般說來,醛比酮活潑,有些反應醛可以發生,而酮則不能。
(一)羰基的加成
同碳碳雙鍵一樣,羰基中的碳氧雙鍵也是由一個σ鍵和一個π鍵所組成,所以醛、酮都易發生加成反應。但和烯烴的親電加成不同,羰基的加成屬於親核加成。由於氧原子的電負性大於碳原子,使羰基發生極化,氧原子帶有部分負電荷,碳原了帶有部分正電荷。一般說來,帶負電荷的氧比帶正電荷的碳較為穩定。所以,當羰基化合物發生加成反應時,首先是試劑中帶負電荷的部分加到羰基的碳原子上,形成氧帶負電荷的中間體,然後試劑中帶正荷部分加到帶負虵荷的氧上。這種由親核試劑(能提供電子對的試劑)進攻而引起蝗加成反應叫做親核加成反應。這類加反應可用於下式表示:
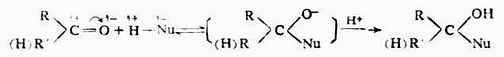
醛和酮可以與氫氰酸、亞梳酸氫鈉、醇、氨的衍生物(如羥胺、肼等)試劑起加成反應。在反應產物中都是試劑中的氫與羰基上的氧相連接,其餘部分與羰基的碳相連。
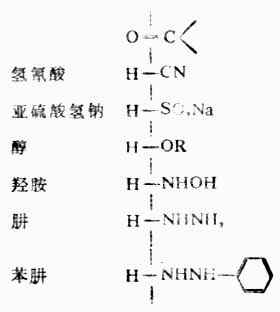
1.加氫氰酸
醛及脂肪族甲基酮與氫氰酸作用,生成α-α羰基腈。
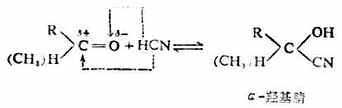
從上面的反應式或以看出,生成物比反應物增加了一個碳原子,因此這個反應可用來增長化合物的碳鏈。羥基腈在酸性水溶液中水解,即可得到羥基酸。
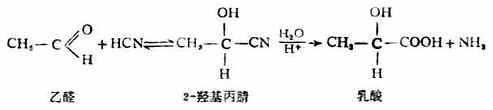
如果在醛、酮與氫氰酸反應中加入少量鹼時,則反應速率明顯加快;但如果加入酸,則抑制反應的進行。其原因是氫氰酸是一個弱酸,其離解過程為:
![]()
在上述平衡體系中加入酸, 能HCN的離解,加入鹼則促進HCN的離解,使CN-濃度增大。鹼能加速羰基與氫氰酸的加成反應表明,氫氰 酸不是以分子,而是以CN-及H+參加反應的。又因鹼的加入,能增加CN-的濃度,所以首先向羰基進攻的是CN-。這是親核加成反應歷程的實驗基礎。
對於同一種親核試劑,親核加成的難易取決於羰基碳原子所帶正電荷的強弱及位阻效應的大小。所謂位阻效應是指分子中相鄰的原子或原子團,在空間所佔的體積和位置而產生的影響。羰基碳原子所帶正電荷越多,反應越容易進行;羰基上連接的烴基越大則位阻效應越大,親核試劑就越不容易靠近,反應也就越不容易進行。酮的羰基和兩個烴基相連,由於烷基的斥電子作用,降低了羰基碳原子的正電荷;另一方面酮的兩上烴基增大了位阻效應,所以在許多親核加成反應中,酮一般不如醛活潑。醛、酮親核加成反應活潑性順序排列如下:
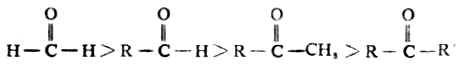
2.加亞硫酸氫鈉
醛、脂肪族甲基酮和低級環酮(成環的碳原子在8個以下)都能與過量的飽和亞硫酸氫鈉溶液發生加成反應,生成穩定的亞硫酸氫鹽中成物。
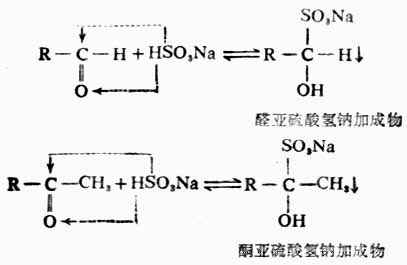
上述反應是可逆的。為使反應完全,常加入過量的飽和亞硫酸氫鈉溶液,促使反應向右移動。由於這些加成物能被稀酸或稀鹼分解成原來的醛或甲基酮,故常用這個反應來分離、精製醛或甲基酮。
其它脂肪酮或芳香酮(包括芳香族甲基酮)由於受位阻效應的影響難以進行這種加成反應。
3.加醇
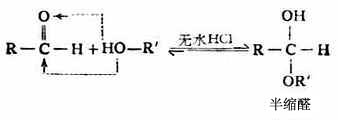
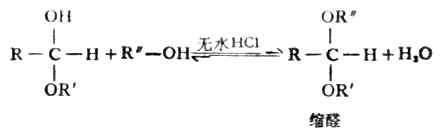
開鏈半縮醛是一類不穩定的化合物,能繼續與另一分子醇作用,失去一分子水生成縮醛。縮醛是具有水果香味的液體,性質與醚相近。縮醛對氧化劑和還原劑都很穩定,在鹼性溶液中也相當穩定,但在酸性溶液中則可以水解生成原來的醛和醇。在有機合成中,常先將含有醛基的化合物轉變成縮醛,然後再進行別的化學反應,最後使縮醛變為原來的醛,這樣可以避免活潑的醛基在反應中被破壞,即利用縮醛的生成來保護醛基。
酮在同樣情況下不易生成縮酮。但是環狀的縮酮比較容易形成。例如:
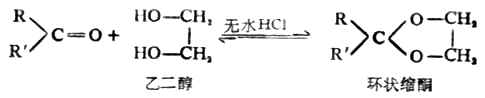
若在同一分子中既含有羰基又含有羥基,則有可能在分子內生成環狀半縮醛(酮)。半縮醛(酮)、縮醛(酮)比較重要,因為它是學習糖類化學的基礎,以後還要討論。
4.與氨的衍生物的反應
醛、酮與氨的衍生物如羥胺、肼、2,4-二硝基苯肼等試劑作用,則生成相應的含碳氨雙鍵的化合物,其名稱及構造分別為:
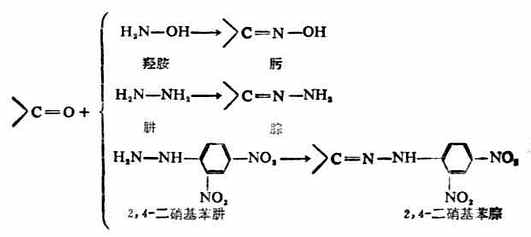
這此反應首先是N-H鍵斷裂和與羰基加成,然後再脫去一分子水生成肟或腙。例如:
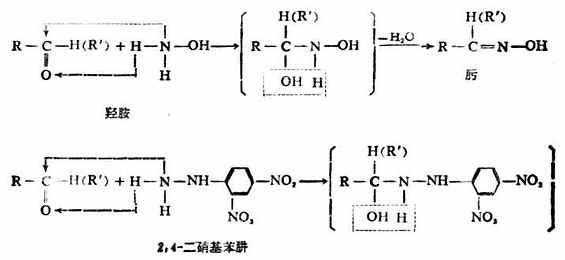
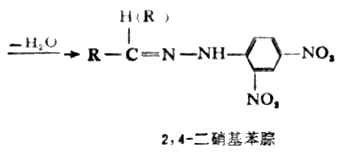
醛、酮與2,4-二硝基苯肼作用生成的2,4-二硝基苯腙是黃色結晶,具有一定的熔點,反應也很明顯,便於觀察,所以常被用來鑒別醛、酮。其它反應的產物肟、腙大都也是具有一定熔點的晶體,亦可用來鑒別醛、酮。因此,把這些氨的衍生物稱為羰基試劑(即檢驗羰基的試劑)。
肟、腙等在稀酸作用下,可水解為原來的醛、酮,故可利用這些反應來分離和精製醛、酮。
(二)α碳原子上氫的反應
醛、酮分子中的α碳原子上的氫比較活潑,容易發生反應,故稱為α活潑氫原子。若α碳原子上連接三個氫原子,則稱其為活潑甲基。
醛、酮α碳原子上的氫因受羰基的影響具有活潑性,這是由於羰基的極化使α碳原子上C-H鍵的極性增強,氫原子有成為質子離去的趨向,很容易發生反應。
醛或酮的α氫原子易被鹵素取代,生成α-鹵代醛或酮。例如:
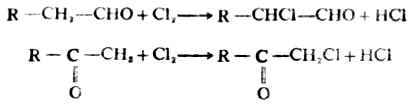
鹵化反應繼續進行時,也可生成α,α-二鹵代物和α,α,α-三鹵代物。
鹵代醛或鹵代酮都具有特殊的刺激性氣味。三氯乙醛的水合物CCL3CH(OH)2,又稱水合氯醛,具有催眠作用;溴丙酮具有催淚作用;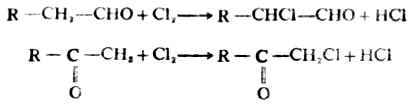
-溴苯乙酮的催淚作用更強,可用作淚瓦斯。
含有活潑甲基的醛或酮與鹵素的鹼溶液作用,三個α氫原子都被鹵素取代,但生成的α,α,α三鹵代物在鹼性溶液中不穩定,立即分解成三鹵甲烷(鹵仿)和羧酸鹽。
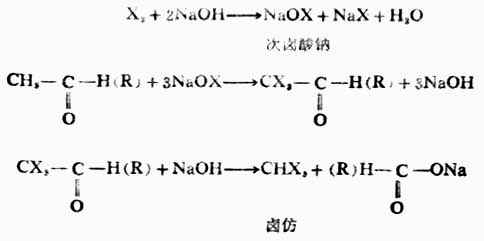
因為這個反應生成鹵仿,所以稱為鹵仿反應。如用碘的鹼溶液,則生成碘仿(稱為碘仿反應)。碘仿為黃色晶體,難溶於水,並具有特殊的氣味,容易識別,可用來鑒別是否含有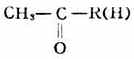
構造的羰基化合物。
次鹵酸鹽是一種氧化劑,可以使醇類氧成相應的醛、酮。因此,凡具有
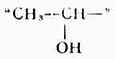
構造的醇會先被氧化成乙醛或甲基酮,再進行鹵仿反應。所以碘仿
2.羥醛縮合
含有氫原子的醛在稀鹼的作用下,一分子醛的α氫原子加到另一分子醛的羰基氧原子上,其餘部分加到羰基的碳原子上,生成既含有羥基又含有醛基的β-羥基醛(醇醛),這個反應稱為羥醛縮合或醇醛縮合。例如:
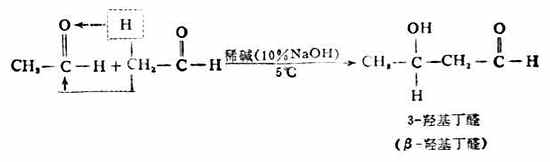
在鹼或酸性溶液中加熱時,β-羥 基醛易脫水生成α,β-不飽和醛。例如:
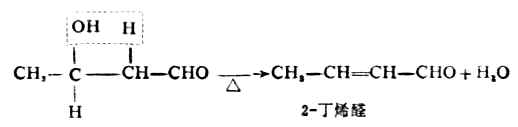
含有α氫原子的酮也可以發生類似的反應,生成β-羥 基酮,脫水後生成α,β-不飽和酮。
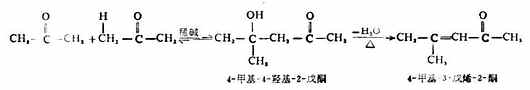
(三)還原反應
醛或酮經催化氫化可分別被還原為伯醇或仲醇。
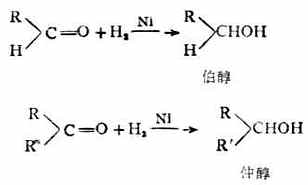
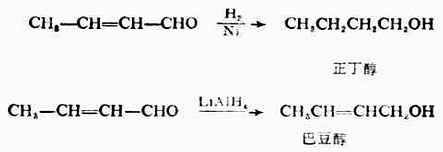
醛、酮與氫化鋁鋰(LiALH4)、硼氫化鈉(NaBH4)或異丙醇鋁(AL[OCH(CH3)2]3)作用,也都還原生成相應的醇。這些還原劑具有較高的選擇性,只能還原羰基,而不影響分子中的碳碳雙鍵等其它可被催化氫化的基團。例如,巴豆醛若用鎳催化氫化則得到正丁醇,而用LiALH4還原可以得到巴豆醇。 >
(四)醛的特殊反應
醛的羰基碳原子上連有氫原子,因此容易被氧化,不僅強氧化劑,即使氧化劑也可以使它氧化。醛氧化時生成同碳數的羧酸。酮則不易被氧化。
一些弱氧化劑只能使醛氧化而不能使酮氧化,說明醛具有還原性而酮一般沒有還原性。因此,可以利用弱氧化劑來區別醛和酮。常用的弱氧化劑有土倫試劑、費林試劑和本尼迪特。
1.與土倫試劑反應
土倫試劑是由硝酸銀鹼溶液與氨水製得的銀氨配合物的無色溶液。它與醛共熱時,醛被氧化成羧酸,試劑中的一價銀離子被還原成金屬銀析出。由於析出的銀附著在容器壁上形成銀鏡,因此這個反應叫做銀鏡反應。
氧化劑也可以使它氧化。醛氧化時生成同碳數的羧酸。酮則不易被氧化。
一些弱氧化劑只能使醛氧化而不能使酮氧化,說明醛具有還原性而酮一般沒有還原性。因此,可以利用弱氧化劑來區別醛和酮。常用的弱氧化劑有土倫試劑、費林試劑和本尼迪特。
1.與土倫試劑反應
土倫試劑是由硝酸銀鹼溶液與氨水製得的銀氨配合物的無色溶液。它與醛共熱時,醛被氧化成羧酸,試劑中的一價銀離子被還原成金屬銀析出。由於析出的銀附著在容器壁上形成銀鏡,因此這個反應叫做銀鏡反應。
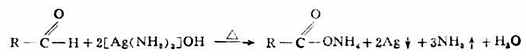
此反應可簡單表示如下:
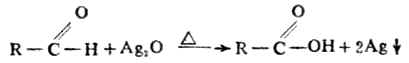
2.與費林試劑反應
費林試劑包括甲、乙兩種溶液,甲液是硫酸銅溶液,乙液是酒石鉀鈉和氫氧化鈉溶液。使用時,取等體積的甲、乙兩液混合,開始有氫氧化銅沉澱產生,搖勻後氫氫化銅即與酒石酸鉀鈉形成深藍色的可溶性配合物。
費林試劑能氧化脂肪醛,但不能氧化芳香醛,可用來區別脂肪醛和芳香醛。費林試劑與脂肪醛共熱時,醛被氧化成羧酸,而二價銅離子則被還原為磚紅色的氧化亞銅沉澱。
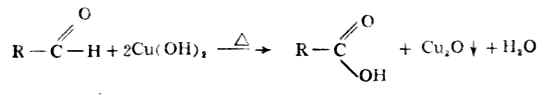
本尼迪特試劑也能把醛氧化成羧酸。它是由硫酸銅、碳酸鈉和檸檬酸鈉組成的溶液。它與醛的作用原理和費林試劑相似。臨床上常用它來檢查尿液中的葡萄糖。
(五)聚合反應
甲醛、乙醛等低級醛可以發生聚合反應,生成鏈狀或環狀化合物。例如:
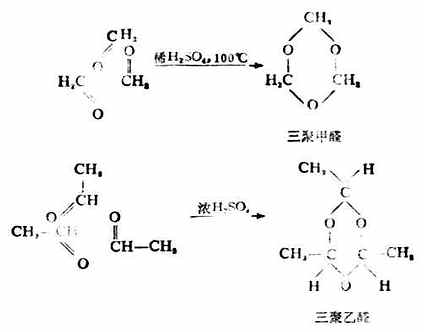
甲醛溶液長期放置後,生成多聚甲醛的白色固體。一般認為甲醛在水溶液中是以水合物形式存在的,這些水合物失去縮合即生成鏈狀的多聚甲醛。
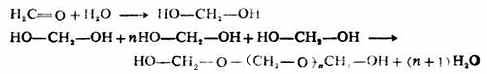
n一般最多可達100。多聚甲醛對熱不穩定,在100℃時迅速地分解成甲醛。
高級的醛酮較難聚合。
五、個別醛和酮
(一)甲醛
甲醛又叫蟻醛,是具有強烈刺激臭味的無色氣體,沸點-21℃。易溶於水,其40%的水溶液叫「福爾馬林「,用作消毒劑和防腐劑。甲醛溶液能夠消毒防腐的原因是因為甲醛具有使蛋白質凝固的性能。
(二)丙酮
丙酮是最簡單的酮類化合物,它是無色液體,沸點56.5℃.丙酮極易溶於水,幾乎能與一切有機溶劑混溶,也能溶解油脂、蠟、樹脂和塑料等,故廣泛用作溶劑。
患糖尿病的人,由於新陳代謝紊亂的緣故,體內常有過量丙酮產生,從尿中排出。尿中是否含有丙酮可用碘仿反應檢驗。在臨床上,用亞硝醯鐵氰化鈉[Na2Fe(CN)5NO]溶液的呈色反應來檢查:在尿液中滴加亞硝醯鐵氰化鈉和氨水溶液,如果有丙酮存在,溶液就呈現鮮紅色。
(三)樟腦
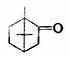
樟腦是無色半透明晶體,具有穿透性的特異芳香,味略苦而辛,有清涼感,熔點176-177℃,易升華。不溶於水,能溶於醇等。樟腦是我國的特產,台灣省的產量約佔世界總產量的70%,居世界第一位,其它如福建、廣東、江西等省也有出產。樟腦在醫學上用途很廣,如作呼吸循環興奮藥的樟腦油注射劑(10%樟腦的植物油溶液)和樟腦磺酸鈉注射劑(10%樟腦磺酸鈉的水溶液);用作治療凍瘡、局部炎症的樟腦醑(10%樟腦酒精溶液);成藥清涼油、十滴水和消炎鎮痛膏等均含有樟腦。樟腦也可用於驅蟲防柱。
(四)麝香酮
麝香酮為油狀液體,具有麝香香味,是麝香的主要香氣成分。沸點328℃,微溶於水,能與乙醇互溶。麝香酮的構造為一個含15個碳原子的大環,環上有一個甲基和一個羰基,屬脂環酮。
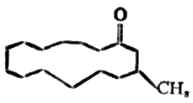
香料中加入極少量的麝香酮可增強香味,因此許多貴重香料常用它作為定香劑。人工合成的麝香廣泛應用於製藥工業。
| 關於「醫用化學/醛和酮」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |