醫用化學/胺類
| 醫學電子書 >> 《醫用化學》 >> 含氮有機化合物 >> 胺類 |
| 醫用化學 |
|
|
胺類是比較重要的含氮有機化合物。例如苯胺是合成藥物、染料等的重要原料;膽鹼是調節脂肪代謝的物質,它的乙醯衍生物——乙醯膽鹼是神經傳導的遞質;乙二胺是製造EDTA的原料等。
一、胺的構造、分類和命名
(一)胺的構造和分類
胺可以看作是氨(NH3)分子中的氫原子被烴基取代所生成的化合物。通式為RNH2,R2NH或R3N,其中R代表脂肪烴基或芳香烴基,它們分別屬於伯、仲和叔胺。
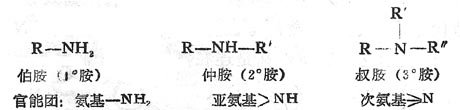
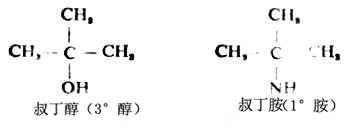
但要注意,這裡的伯、仲、叔的含義與醇中的不同,它們分別是指氮原子上連有一個、兩個或是三個烴基,而與連接氨基的碳是伯、仲還是叔碳原子沒有關係。例如,叔丁醇是叔醇,而叔丁胺卻是伯胺。
季胺化合物可看作是銨鹽(NH4+X-)或氧氧化銨(NH4OH)分子中氮原子上的四個氫原子都被烴基取代生成的化合物,它們分別稱為季銨鹽和季銨鹼。
仲、叔胺或季銨化合物分子中的烴基可以是相同的,也可以是不同的。
在這裡,應注意「氨」、「胺」及「銨」的含義。在表示基(如氨基、亞氨基等)時,用「氨」;表示NH3的烴基衍生物時,用「胺」;而銨鹽或季銨類化合物則用「銨」。
胺也可以根據NH3分子中的氫原子被不同種類的烴基取代而分為脂肪胺和芳香胺。氨基與脂肪烴基相連的是脂肪胺,與芳香環直接相連的叫芳香胺。
R-NH2Ar-NH2
脂肪胺 芳香胺
胺還可以根據分子中所含氨基數目的不同而分為一元胺、二元胺和多元胺。
(二)命名
1.普通命名法
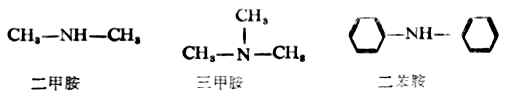
這種方法是按照分子中烴基的名稱及數目叫做「某胺」。
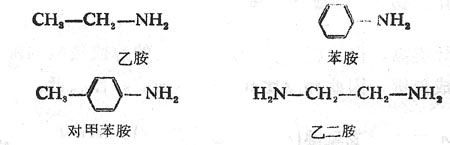
當胺分子中氮原子上所連的烴基不同時,則按次序規則列出,小者在前,「較優」者在後。
CH3-NH-C2H5
甲乙胺
若原子上連有兩個或三個相同的烴基時,則須表示出烴基的數目。
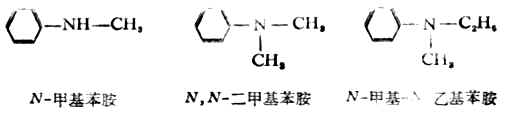
氮原子上同時連有芳香烴基和脂肪烴基的仲胺和叔胺的命名,則以芳香胺為母體,脂肪烴基作為芳胺氮原子上的取代基,將名稱和數目寫在前面,並在基前冠以「N」字(每個「N」只能指示一個取代基的位置),以表示這個脂肪烴基是連在氮原子上,而不是連在芳香環上。
2.系統命名法
烴基比較複雜的胺,以烴為母體,將氨基作為取代基命名。
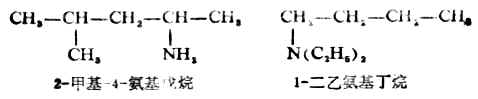
季銨化合物的命名與無機銨的命名相似。
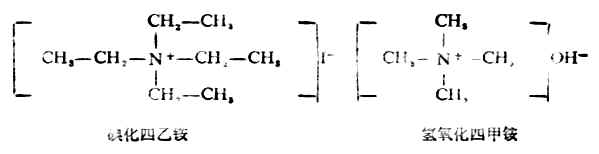
二、胺的性質
(一)物理性質
胺與氨的性質很相似。低級脂肪胺是氣體或易揮發的液體,具有難聞的臭味。高級胺為固體。芳香胺為高沸點的液體或低熔點的固體,具有特殊氣味,難溶於水,易溶於有機溶劑。芳香胺具有一定的毒性,如苯胺可以通過消化道、呼吸道或經皮膚吸收而引起中毒;聯苯胺等有致癌作用。因此,在處理這些化合物時應加以注意。
同氨一樣,胺是極性化合物。除叔胺外,都能形成分子間氫鍵
![]() 。胺的沸點比相對分子質量相近的烴類高,但比相對分子質量相近的醇或羧酸的沸點低。叔胺氮原子上無氫原子,分子間不能形成氫鍵,因此沸點比其異構體的伯、仲胺低。
。胺的沸點比相對分子質量相近的烴類高,但比相對分子質量相近的醇或羧酸的沸點低。叔胺氮原子上無氫原子,分子間不能形成氫鍵,因此沸點比其異構體的伯、仲胺低。
伯、仲、叔胺都能與水分子形成氫鍵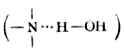 ,因此低級的胺
,因此低級的胺
易溶於水。胺的溶解度隨相對分子質量的增加而迅速降低,從6個碳原子的胺開始就難溶於水。一般胺能溶於醚、醇、苯等有機溶劑。
(二)化學性質
1.胺的鹼性和成鹽反應
胺中的氮原子和氨中一樣,有一對未共用電子對。能接受質子,因此胺具有鹼性。
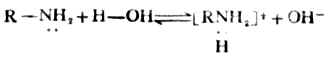
胺的鹼性以鹼式離解常數Kb或其負對數pKb值表示。Kb值愈大或pKb值愈小則鹼性愈強;Kb值愈小或pKb值愈大則鹼性愈弱。胺的鹼性也可用其共軛酸銨離子的離解常數Ka或pKa來表示。Ka值愈小或pKa值愈大,則胺的鹼性愈強。
在水溶液中,脂肪胺一般以仲胺的鹼性最強。但是,無論伯、仲或叔胺,其鹼性都比氨強。芳香胺的鹼性則比氨弱。氨、甲胺、二甲胺、三甲胺和苯胺的鹼性強弱次序為:
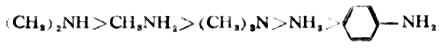
(1)脂肪胺的鹼性 影響脂肪胺鹼性的因素有三個。①誘導效應——胺分子中與氮原子相連的烷基具有斥電子誘導效應(+I,![]()
,使氮上的電子云密度增加,從而增強了對質子的吸引能力,而生成的銨離子也因正電荷得到分散而比較穩定。因此,氮上烷基數增多,鹼性要增強。②水化作用——在水溶液中,胺的鹼性還決定於與質子結合後形成的銨離子水化的難易。氮原子上所連的氫愈多,則與水形成氫鍵的機會就愈多,水化程度亦愈大,銨離子就更穩定,胺的鹼性也就增強。③位阻效應——胺分子中的烷基愈多、愈大,則佔據空間的位置就愈大,使質子不易靠近氮原子,因而胺的鹼性就降低。
因此,脂肪伯、仲、叔胺鹼性的強弱是上述三個因素共同影響的結果。
(2)芳香胺的鹼性 芳香胺的鹼性比脂肪胺弱得多。例如苯胺的pKb=9.40,這是因為苯胺中氮原子的未共用電子對與苯環的π電子相互作用,形成一個均勻的共軛體系而變得穩定,氮原子上的電子云部分地轉向苯環,因此氮原子與質子的結合能力降低,故苯胺的鹼性比氨弱得多。
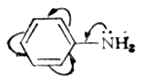
芳香胺氮原子上所連的苯環愈多,共軛程度愈大,鹼性也就愈弱。?
■[此處缺少一些內容]■
季銨鹽是有機化合物中的強鹼。它們在固態時即是離子狀態,例如(CH3)4N+O-H易溶於水,其鹼性與氫氧化鈉或氫氧化鉀相當。
季銨鹽和銨鹽不同,前者是強鹼的鹽,與氫氧化鈉等不發生反應。鹵化季銨鹽的水溶液用氧化銀處理時則生成季銨鹼。
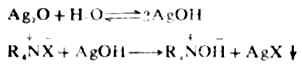
2.酯化反應
伯、仲胺都能與醯化劑(如乙醯氯、乙酸酐)作用,氨基上的氧原子被醯基取代,生成醯胺,這種反應叫做胺的醯化。叔胺因氮上沒有氫,故不發生醯化反應。
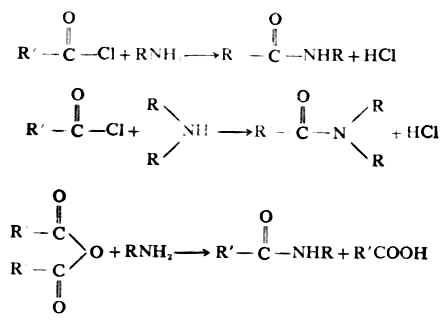
醯胺是晶形很好的固體,有一定的熔點,所以利用醯化反應可以鑒定伯胺和仲胺。叔胺不起醯化反應,故此性質可用來區別叔胺,並可以從伯、仲、叔胺的混合物中把叔胺分離出來。此外,醯胺在酸或鹼的催化下,可水解游離出原來的胺。由於氨基活潑,且易被氧化,因此在有機合成中可以用醯化的方法來保護芳胺的氨基。例如:
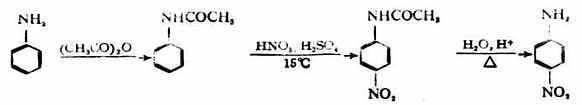
3.與亞硝酸反應
伯、仲、叔胺與亞硝酸反應時,產物各不相同,藉此可區別三種胺。
由於亞硝酸(HNO2)是一種很不穩定的酸,所以通常用亞硝酸鈉和強酸作用產生。
NaNO2+HCl→HNO2+NaCl
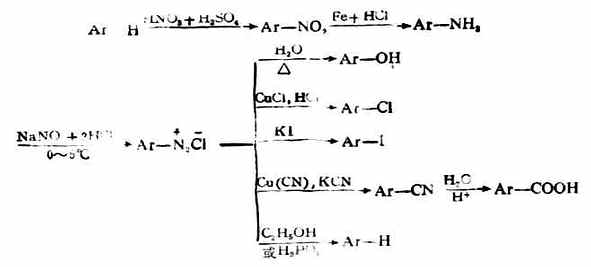
(1)伯胺與亞硝酸反應脂肪伯胺與亞硝酸反應,放出氮氣,並生成醇、烯烴等的混合物。其反應式可簡單地用下式表示:
R-NH2+HONO→ROH+N2↑+H2O
CH3-NH2+HONO→CH3OH+N2↑+H2O
由於此反應能定量地放出氮氣,故可用於伯胺及氨基化合物的分析。
芳香族伯胺與脂肪伯胺不同,在低溫和強酸存在下,與亞硝酸作用則生成芳香族重氮鹽,這個反應稱為重氮化反應。例如:
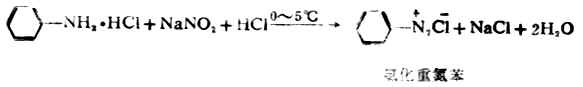
芳香重氮鹽比脂肪重氮鹽穩定,如在5℃以下,氯化重氮苯在水溶液中不會分解但溫度升高,使分解放出氮氣,同時生成酚類化合物。
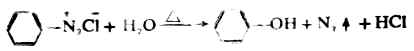
芳香重氮鹽化學性質很活潑,是有機合成的重要中間體。例如,通過重氮鹽的反應,可以製備許多芳香族化合物。芳香重氮鹽的反應主要分為放氮反應和偶合反應兩大類。
基、氫原子等取代,生成相應的芳香族衍生物,放出氮氣。因此,利用這些反應可以從芳香烴開始合成一系列芳香族化合物。
偶合反應:重氮鹽與酚類或芳香叔胺作用,生成有顏色的偶氮化合物,這個反應稱為偶合反應。
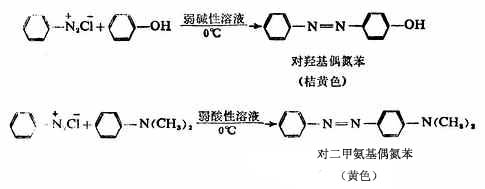
重氮鹽與酚或芳香胺偶合時,如果羥基或氨基的對位有其它原子或原子團,則可在鄰位偶合;如果對位及鄰位都有取代基時,則不發生反應。
偶氮化合物都有顏色。許多偶氮化合物可用作染料,稱為偶氮染料,有些偶氮化合物的顏色能隨溶液PH值的不同而變化,這些化合物可用作酸鹼指示劑。例如甲基橙。
(2)仲胺與亞硝酸反應脂肪仲胺和芳香族仲胺與亞硝酸作用生成N-亞硝基胺。
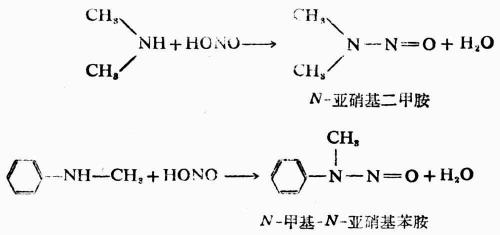
N-亞硝基胺為黃色的中性油狀物質,不溶於水,可從溶液中分離出來;與稀酸共熱則分解為原來的仲胺,故可利用此性質鑒別、分離或提純仲胺。
N-亞硝基胺是較強的致癌物質。
(3)叔胺與亞硝酸反應脂肪叔胺因氮上沒有氫,與亞硝酸作用時只能生成不穩定的亞硝酸鹽。

芳香族叔胺與亞硝酸作用,發生環上取代反應,在芳香環上引入亞硝基,生成對亞硝基取代物,在酸性溶液中呈黃色,若對位上已有取代基,則亞硝基取代在鄰位。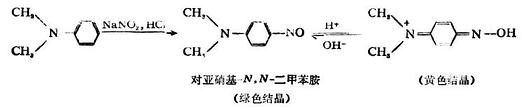
由於三種胺與亞硝酸的反應不同,所以可利用與亞硝酸的反應鑒別伯、仲、叔胺。
三、重要的胺及其衍生物
(一)苯胺
苯胺是最簡單也是最重要的芳香伯胺,是合成藥物,染料等的重要原料。苯胺為油狀液體,沸點184℃,微溶於水,易溶於有機溶劑。新蒸餾的苯胺無色,但久置會因氧化而顏色變深。苯胺有毒,能透過皮膚或吸入蒸氣使人中毒。因此,接觸苯胺時應加註意。
(二)膽鹼
膽鹼[(CH3)3N+CH2CH2OH]OH-是一種季銨鹼,廣泛存在於生物體中,在腦組織和蛋黃中含量較多,是卵磷脂(見第二十章)的組成部分。膽鹼為白色結晶,吸濕性強,易溶於水和乙醇,而不溶於乙醚和氯仿等。它在體內參與脂肪代謝,有抗脂肪肝的作用。
膽鹼分子中醇羥基的氫原子被乙醯基取代所生成的酯叫做乙醯膽鹼[CH3COOCH2CH2N+(CH3)3]OH-,是神經傳導的遞質。
(三)新潔爾滅
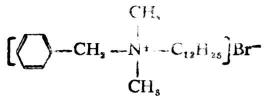
新潔爾滅(溴化二甲基十二烷基苄基銨)
在常溫下,新潔爾滅為微黃色的粘稠液,吸濕性強,易溶於水和醇。水溶液呈鹼性。新潔爾滅是具有長鏈烷基的季銨鹽,屬陽離子型表面活性劑,也是消毒劑。臨床上上用於皮膚、器皿及手術前的消毒。
| 關於「醫用化學/胺類」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |