醫用化學/醯胺
| 醫學電子書 >> 《醫用化學》 >> 含氮有機化合物 >> 醯胺 |
| 醫用化學 |
|
|
一、醯胺的構造和命名
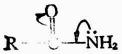
醯胺是羧酸的衍生物。在構造上,醯胺可看作是羧酸分子中羧基中的羥基被氨基或烴氨基(-NHR或-NR2)取代而成的化合物;也可看作是氨或胺分子中氮原子上的氫被醯基(![]() )取代而成的化合物。
)取代而成的化合物。
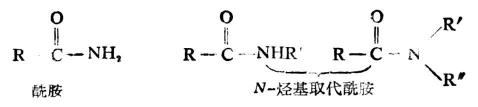
醯胺的命名是根據相應的醯基名稱,並在後面加上「胺」或「某胺」,稱為「某醯胺」或「某醯某胺」。例如:
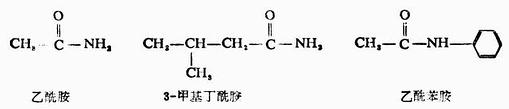
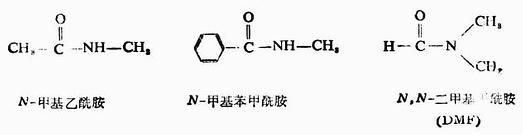
當醯胺中氮上連有烴基時,可將烴基的名稱寫在醯基名稱的前面,並在烴基名稱前加上「N-」「N,N-」,表示該烴基是與氮原子相連的。
二、醯胺的性質
(一)物理性質
在常溫下,除甲醯胺是液體外,其它醯胺多為無色晶體。醯胺分子中含有羰基和氨基,它們分子間能形成氫鍵。由於醯胺分子間氫鍵締合能力較強,因此其熔點、沸點甚至比相對分子質量相近的羧酸還高。
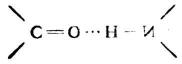
當醯胺中氮原子上的氫被烷基取代後,締合程度減小,熔點和沸點則降低。脂肪族N-烷基取代醯胺一般為液體。
低給醯胺易溶於水,隨著相對分子質量的增大,溶解度逐漸減小。液體醯胺不但可以溶解有機物,而且也可以溶解許多無機物,是良好的溶劑。例如HCON(CH3)2。
(二)化學性質
1.酸鹼性
醯胺一般是近中性的化合物,但在一定條件下可表現出弱酸或弱鹼性。醯胺是氨或胺的醯基衍生物,分子中有氨基或烴氨基,但其鹼性比氨或胺要弱得多。醯胺鹼性很弱,是由於分子中氨基氮上的未共用電子對與羰基的π電子形成共軛體系,使氮上的電子云密度降低,因而接受質子的能力減弱。這時C-N鍵出現一定程度的雙鍵性。
然而,氮上的電子云密度降低,卻使N-H鍵的極性增加,從而表現出微弱的酸性。如果氨分子中有兩個氫原子被一個二元酸的醯基取代,則生成環狀的亞氨基化合物(醯亞胺)。由於兩個羰基的吸電子作用,使亞氨基的N-H鍵極性明顯增加,氮上的氫原子較易變為質子,而呈弱酸性。例如:
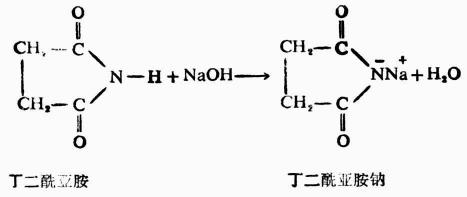
2.水解
醯胺在通常情況下較難水解。在酸或鹼的存在下加熱時,則可加速反應,但比羧酸酯的水解慢得多。
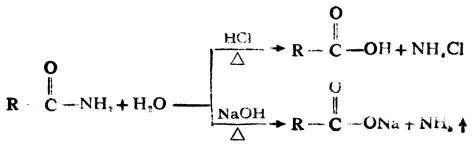
N-取代醯胺同樣可以進行水解,生成羧酸和胺。
3.與亞硝酸反應
醯胺與亞硝酸作用生成相應的羧酸,並放出氮氣。
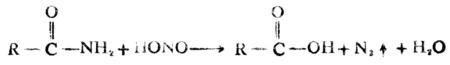
三、重要的醯胺及其衍生物
(一)尿素
尿素又稱脲,是碳酸的二醯胺。
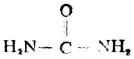
尿素是哺乳動物體內蛋白質代謝的最終產物,存在於動物的尿中。許多含氮化合物在代謝過程中所釋放的氨是有毒的,通過轉變為尿素從尿中排出而使氨的濃度降低。正常成人每天排泄的尿中約含尿素30g。
尿素是很重要的物質,用途廣泛。它在農業上用作高效固體氮肥,也是有機合成的重要原料。用於合成藥物、塑料等。尿素本身也是藥物,對降低腦顱內壓和眼內壓有顯著療效。
尿素具有醯胺的結構,有醯胺的一般化學性質。但因兩個氨基連在一個羰基上,所以它又表現出某些特殊的性質。
1.弱鹼性
尿素分子中有兩個氨基,其中一個氨基可與強酸成鹽,故呈弱鹼性。
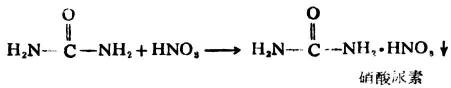
尿素的硝酸鹽、草酸鹽均難溶於水而易結晶。利用這種性質,可從尿液中提取尿素。
2.水解反應
尿素是醯胺類化合物,在酸、鹼或尿素酶的作用下很易水解。
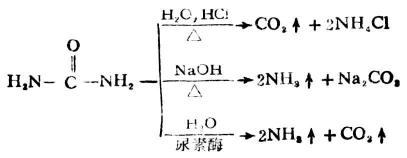
3.縮二脲的生成及縮二脲反應
尿素是一種特殊的醯胺,它的兩個氨基連在同一個羰基上,所以它又有與一般醯胺不同的性質。若將尿素加熱到稍高於它的熔點時,則發生雙分子縮合,兩分子尿素脫去一分子氨而生成縮二脲。
![]()
縮二脲是無色針狀晶體,熔點190℃,難溶於水,能溶於鹼液中。它在鹼性溶液中與少量的硫酸銅(CuSO4)溶液作用,即顯紫紅色,這個顏色反應叫做縮二脲反應。凡分子中含有兩個或兩上以上醯胺鍵( ![]()
,肽鍵)合
物如多肽、蛋白質等都能發生這種顏色反應。
(二)丙二醯脲
尿素與醯氯、酸酐或酯作用,則生成相應的醯脲。例如,尿素與丙二醯氯反應生成丙二醯脲。
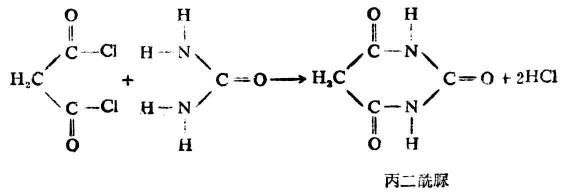
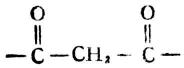
丙二醯脲是無色晶體,熔點245℃,微溶於水。它的分子中含有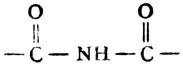
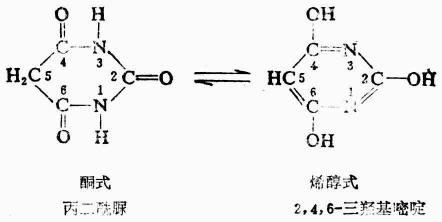
由於丙二醯脲中由酮式轉變為烯醇式而呈酸性,所以丙二醯脲又稱巴比土酸。
巴比土酸本身沒有藥理作用,但它的C-5亞甲基上的兩個氫原子都被烴基取代(5,5-二取代)後所得許多取代物,卻是一類重要的鎮靜催眠藥,總稱為巴比妥類藥物。其通式為:
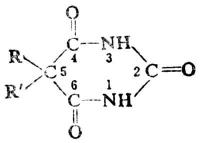
巴比妥類藥物很多,主要的有巴比妥、苯巴比妥(魯米那)、戊巴比妥、異戊巴比妥等。它們是晶體或結晶性粉末,難溶於水,能溶於一般有機溶劑中。
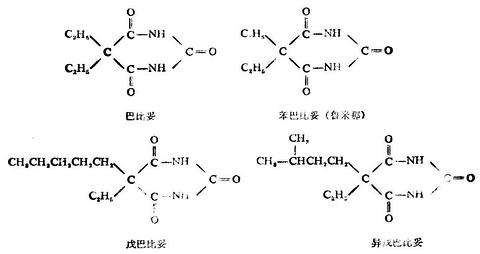
巴比妥類催眠藥的鈉鹽,可作注射用。
(三)磺胺類及氯胺類藥物
烴分子中的氫原子被磺基(-SO3H)取代而成的化合物叫磺酸。芳香磺酸最為重要,例如苯磺酸。
![]()
磺酸的化學性質與羧酸類似,但酸性比羧酸強得多。
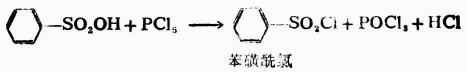
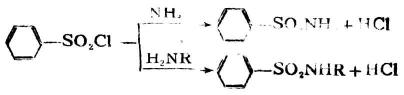
在醫藥上,重要的磺醯胺類化合物有磺胺類藥物及氯胺類藥物。
1.磺胺類藥物
磺胺類藥物是優良的化學治療劑,開始應用於20世紀30年代。它們能抑制多種細菌,如鏈球菌、葡萄球菌、肺炎球菌、腦膜炎球菌、痢疾桿菌等的生長和繁殖,因此常用以治療由上述細菌所引起的疾病。
![]()
磺胺是無色晶體,熔點163℃,味微苦,微溶於水。磺胺能溶於強酸或強鹼溶液中,這是由於它在苯環上連有氨基,因此能與酸作用生成鹽;同時。與磺胺基結合的氨基上的氫原子,因受磺醯基的影響而呈酸性,故又能與鹼作用。
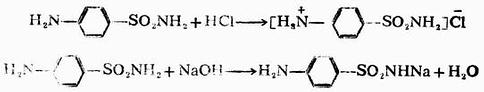
磺胺口服時副作用很大,僅外用以治療化膿性創傷。為了減少磺胺的副作用,一般採用其它原子團取代磺醯氨基上的氫原子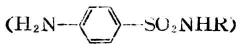 ,其副作用較小,稱為磺胺類藥物。
,其副作用較小,稱為磺胺類藥物。
磺胺類藥物的抗菌譜廣,性質穩定,口服吸收良好,使用方便。表18-2是一些常見的磺胺類藥物。
甲氧芐氨嘧啶(TMP),在化學結構上不屬於磺胺類,但它能加強磺胺藥的作用,也能增強多種抗生素的療效,稱為磺胺增效劑,常與磺胺類藥物或抗生素伍用。
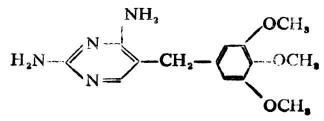
甲氧苄氨嘧啶(TMP)
表18-2 常見的磺胺類藥物
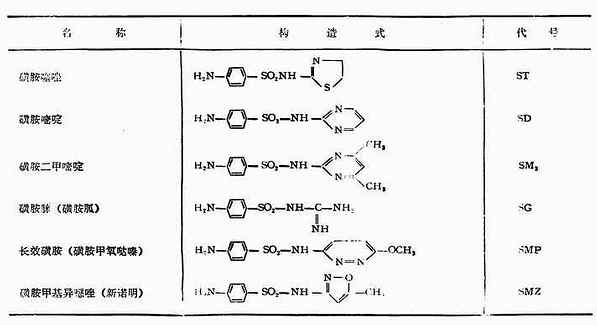
2.氯胺類藥物
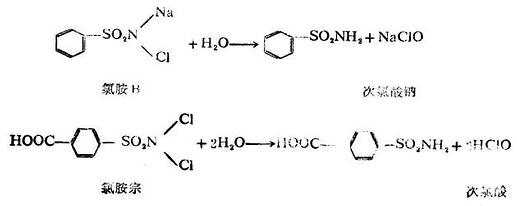
苯磺醯胺分子中,氨基的氫原子被氯原子取代的化合物叫做氯胺類藥物。例如:
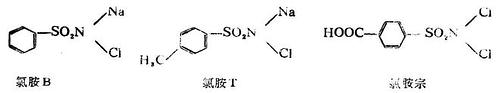
氯胺類藥物是白色或黃色結晶性粉末,微具氯氣味。能溶於水及乙醇,難溶於乙醚等有機溶劑。
氯胺類藥物都是氧化劑,它們與水反應生成次氯酸或次氯酸鈉,而有殺菌和對化學毒劑的消毒作用,故在軍事醫學上有重要意義。
| 關於「醫用化學/醯胺」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |