醫用化學/醇
| 醫學電子書 >> 《醫用化學》 >> 醇、酚、醚 >> 醇 |
| 醫用化學 |
|
|
目錄 |
一、醇的分類
醇可根據烴基的不同、羥基所連碳原子的類型、羥基數目等三種方法進行分類。
1.

2.
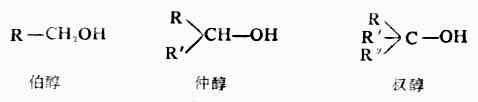
3.例如:
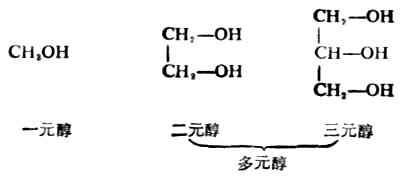
二、醇的命名
(一)普通命名法
簡單的一元醇多用普通命名法命名。通常是在醇字前面加上烴基的名稱,「基」字一般可以省略。例如:
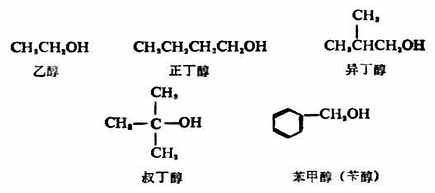
(二)系統命名法
選擇連有羥基碳原子在內的最長碳鏈為主鏈,從靠近羥基的一端開始編號,根據主鏈碳原子數稱某醇。羥基位次用阿拉伯數字表明。支鏈或其它取代基按「次序規則」列出。
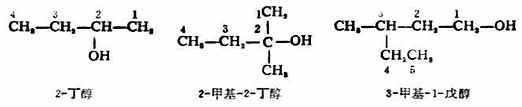
不飽和醇的命名,應選擇連有羥基同時含有雙鍵或三鍵碳原子在內的碳鏈作業主鏈,編號時應以羥基位次為最小。例如:
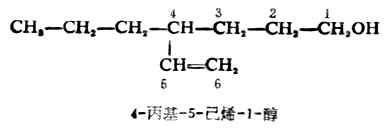
芳香醇也是按照上面的命名原則,把芳香烴當作取代基。例如:

多元醇的命名是選擇包括連有儘可能我的羥基的碳鏈作主鏈,依次基數稱某二醇、某三醇等。因為羥基是連在不同碳原子上的,所以當羥基數與主鏈碳原子數相同時可以不必標明羥基位次。例如:
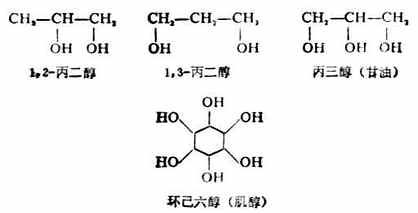
三、醇的性質
(一)物理性質
低級飽和一元醇是易揮發的液體,較高級的醇為粘稠的液體,C11及C11以上的醇為蠟狀固體。由於羥基的存在,醇分子間可以形成氫鍵,故醇隨著羥基的增多,形成氫鍵數目增多,所以多元醇具有更高的沸點。
低級的醇如甲醇、乙醇、丙醇等均能以任何比例與水混溶,這是因為醇羥基也可與水形成氫鍵,結果使醇有可能在水分子間取得位置而溶入水中。當醇中的烴基鏈增長時,由醇的烴基部分引起的分子之間的吸引力(即范德華力)就會超過醇羥基和水間的氫鍵引起的吸引力。結果醇在水中的溶解度就很快隨著降低。例如:在25℃的100g水中,正丁醇的溶解度為7.9g、正己醇為0.6g、正辛醇為0.5g,而癸醇則不溶於水,不溶於非極性溶劑。表14-1是飽和一元醇的物理常數。
表14-1 一些飽和一元醇的物理常數
| 名稱 | 構造式 | 熔點/℃ | 沸點/℃ |
相對密度 20℃ |
溶解度 g.(100水)-1,,25℃ |
| 甲醇 | CH3OH | -97.8 | 64.5 | 0.792 | ∞ |
| 乙醇 | CH3CH2OH | -117.3 | 78.5 | 0.789 | ∞ |
| 正丙醇 | CH3CH2CH2OH | -127 | 97.8 | 0.804 | ∞ |
| 異丙醇 | (CH3)2CHOH | -86 | 82.5 | 0.789 | ∞ |
| 正丁醇 | CH3(CH2)2CH2OH | -89.8 | 117.7 | 0.810 | 7.9 |
| 異丁醇 | (CH3)2CHCH2OH | -108 | 108 | 0.802 | 10.0 |
| 正戊醇 | CH3(CH2)3CH2OH | -78.5 | 137.9 | 0.817 | 2.3 |
| 正己醇 | CH3(CH2)4CH2OH | -52 | 156.5 | 0.819 | 0.6 |
| 正辛醇 | CH3(CH2)6CH2OH | -15 | 195 | 0.827 | 0.05 |
| 正癸醇 | CH3(CH2)8CH2OH | 6 | 228 | 0.829 | |
| 正十二醇 | CH3(CH2)10CH2OH | 24 | 259 | 0.831 | |
| 苯甲醇 | C6H5CH2OH | -15 | 205 | 1.046 | |
| 2-苯基乙醇 | C6H5CH2CH2OH | -26 | 219 | 1.013 | 4 |
| 環己醇 |
|
25 | 161 | 0.962 | 5.7 |
(二)化學性質
醇的官能團是羥基,它由氫氧兩原子組成。氧原子的電負性較大,吸電子的能力較強,所以醇分子中的C-O鍵和O-H鍵都有明顯的極性。鍵的極性有利於異裂反應的發生,所以C-O鍵和O-H鍵都比較活潑,多數反應都發生在這兩個部位。另外,由於誘導效應,與羥基鄰近的碳原子上的氫也參與某些反應。
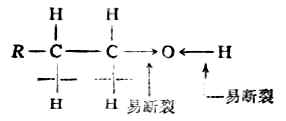
1.與鹼金屬的反應
醇與水相似,羥基里的氫可被活潑金屬取代生成醇化物和氫氫氣。例如:
2ROH+2Na→2RONa+H2↑
醇鈉
2CH3-CH2OH+2Na→2CH2CH2ONa+H2↑
乙醇鈉
醇與金屬鈉的反應不如水與金屬反應時那樣劇烈。這是由於烴基的斥電子作用,使羥基中氧原子上的電子云密度增加,減低了氧原子吸引氫氧間電子對的能力,降低了氫氧鍵的極性。
H-O:h
R→O:h
由於上述誘導效應的存在,使得醇羥基中的氫不如水中的氫那樣活潑,不易成為離子,所以反應也較緩和。由此可見,烴基的斥電子能力愈強,醇羥基中氫原子的活潑性愈低,與金屬鈉的反應就愈緩慢。故伯、仲、叔醇中,伯醇與鈉反應速率最快,叔醇最慢。
醇鈉是白色固體,遇水即水解,生成醇和氫氧化鈉,因此醇鈉的水溶液具有強鹼性。
RONa+H2O→ROH+NaOh
除金屬鈉外,醇也可與鋰、鉀等其它活潑金屬起類似的反應,生成相應醇的金屬化合物,統稱醇化物。
2.氧化反應
醇分子中的α碳原子上若有氫原子時,該氫原子受羥基的影響,比較活潑易於被氧化。用高錳酸鉀或重鉻酸鉀加硫酸等氫氧化劑氧化為相應的醛或酮。例如,伯醇氧化生成醛,醛繼續氧化生成羧酸;仲醇氧化生成酮。叔醇在同樣條件下不易被氧化。
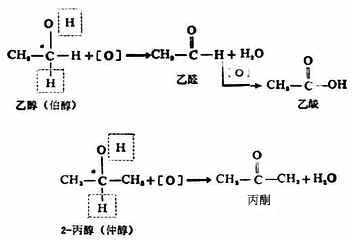
醇的氧化實質上是脫去兩個氫原子,一個是羥基上的氫、一個是α碳(即與-OH相連的C)上的氫。因叔醇α碳上不連氫,所以在一般條件下不起氧化反應。但在反應條件劇烈時,則可發生分子斷裂,產生含碳較少的產物。
用催化脫氫的方法也可將醇氧化。在Cu 、Ag等金屬催化下,醇經高溫可失去兩個氫原子而生成相應的醛和酮,此法可用於工業生產。
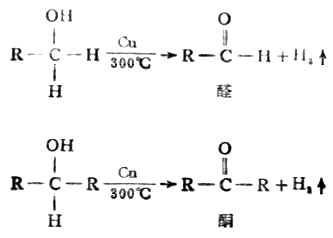
3.與氫鹵酸的反應
醇與氫鹵酸作用時,醇中的羥基可被鹵素取代,生成鹵代烴和水。
![]()
上述反應是可逆的,如其中一種反應物過量或移去產物水,可使平衡右移,提高鹵代烴的收率。這個反應的速率與氫鹵酸和醇的類型有關。當同一種醇與不同的氫鹵酸作用時,反應速率是:HI>HBr>HCL。同一種氫鹵酸與不同的醇作用時,反應速率是:叔醇>仲醇>伯醇。如用無水氯化鋅作催化劑,濃鹽酸可與叔醇立即反應,生成的鹵代烴因不溶於反應試劑而呈混濁;如與仲醇反應,需幾分鐘才呈混濁;如與伯醇反應,則幾小時也不見混濁。因此利用上述不同的反應速率,可作為區別伯、仲、叔醇的一種化學方法。這種由濃鹽酸和無水氯化鋅所配成的試劑又稱為盧卡斯試劑。
4.脫水反應
醇與濃硫酸共熱發生脫水反應,產物隨反應條件及醇的類型而異在較高溫度下,主要發生分子內的脫水(消除反應)生成烯烴;而在稍低溫度下,則發生分子間脫水生成醚。
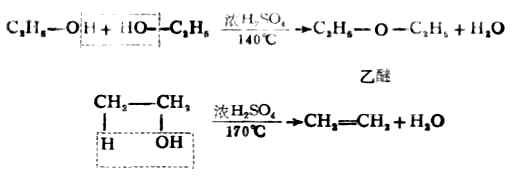
有些仲醇及叔醇的脫水可能生成兩種烯烴。
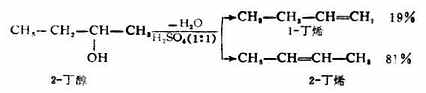
實驗證明,醇脫水生成烯的反應主要產物是碳碳雙鍵上連烴基最多的烯烴。即遵從扎依采夫規律。
5.與無機酸反應
醇可與無機含氧酸如硝酸、亞硝酸β硫酸和磷酸等作用,失去一分子水而生成無機酸酯。例如:
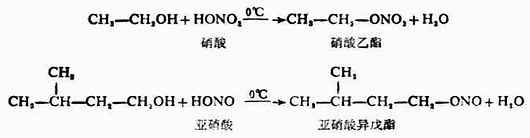
硫酸是二元酸,除可與一分子乙醇作用生成酸性酯外,尚可與兩分子乙醇生成中性酯。
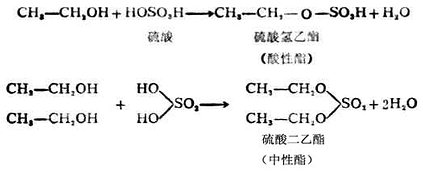
磷酸是一個三元酸,它可以形成三種類型的磷酸酯。即:
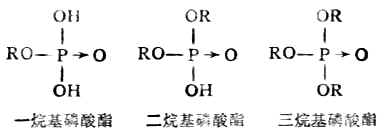
醇的無機酸具有多方面的作途。高級醇(含碳原子8-18個)的酸性硫酸酯的鈉ROSO2Ona具有去垢作用,可用作洗滌劑;亞硝酸異戊酯是緩解心絞痛的藥物;常用的殺蟲藥敵敵畏是具有磷酸酯結構的化合物。
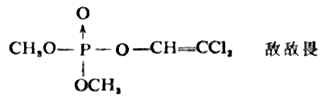
含有無機酸酯的物質也廣泛存在於人體內。如存在於軟骨中的硫酸軟骨質就是具有硫酸酯結構;組成細胞的重要萬分核酸及磷脂中都含有磷酸酯的結構;體內某些代謝過程也往往通過形成磷酸酯作為中間產物。
醇與羧酸作用生成羧酸酯的反應將在第十六章中討論。
6.多元醇的特性
多元醇的化學性質與飽和一元醇類似,也能起酯化、氧化等反應。但由於多元醇所含的羥基比一元醇多,因此又存在著不同於一元醇的某些性質。例如多元醇除了能與鹼金屬反應外,還可與重多屬的氫氧化物反應。如把丙三醇(甘油)加到氫氧化銅沉澱中去就可看到沉澱消失,產生一種深藍色的甘油銅溶液,此反應可用來鑒定具有兩個相鄰羥基的多元醇。
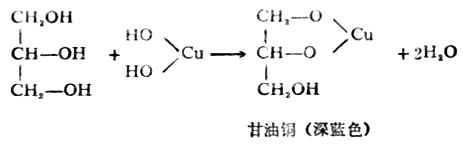
此外,對多元醇分子來講,由於一種反應可在不同位置的羥基上進行,也可在幾個羥基上同時進行,所以往往可得到多種沒的產物。如丙三醇氧化就會生成各種氧化產物的混合物,例如:
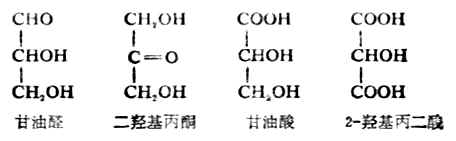
甘油的某些氧化產物的磷酸酯是人體內物質代謝的中間產物。
四、重要的醇
(一)甲醇
甲醇最初由木材乾餾製得,故俗名木精。甲醇為無色透明液體,沸點64.5℃,能與水及多數有機溶劑混溶。甲醇有毒,誤服少量(10ml)能使雙目失明,30ml能中毒致死。甲醇可作溶劑,也是一種重要的化工原料。
(二)乙醇
乙醇是酒的主要成分,故俗名酒精。乙醇為牆角色液體,沸點78.5℃,用途廣泛,是一種重要的有機合成原料和溶劑。我國藥典規定乙醇濃度在20℃時不得小於94.58%(ml/ml),臨床使用的是70%-75%乙醇水溶液作外用消毒劑,因它能使細菌蛋白質脫水變性。長期臥床病人用50%乙醇溶液塗擦皮膚,有收斂作用,並能促進血液循環,可預防褥瘡。在醫藥上常用乙醇配製酊劑,如碘酊,俗稱碘酒,就是碘和碘化鉀的乙醇溶液。
(三)丙三醇
丙三醇俗名甘油,為無色、吸濕性強、有甜味的粘稠液體,沸點290℃,能與水或乙醇混溶。甘油有潤膚作用,但它的吸濕性很強,會對皮膚產生刺激,所以在使用時須先用適量水稀釋。在醫藥上甘油可用作溶劑,如酚甘油、碘甘油等。對便秘患者,常用甘油栓劑或50%甘油溶液灌腸,它既有潤滑作用,又能產生高滲壓,可引起排便反射。甘油三硝酸酯(俗稱硝酸甘油)是緩解心絞痛藥物。它受到震動或撞擊能猛烈分解引起爆炸,故可用作炸藥。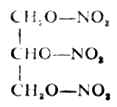
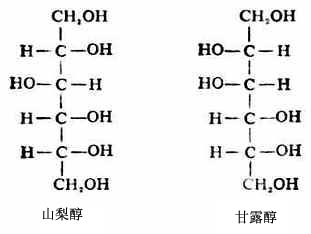
它們都是白色結晶粉末,味甜,廣泛存在於植物中,如許多水果及蔬菜中均含有。
山梨醇和甘露醇均易溶於水。它們的20%或25%的溶液,在臨床上用作滲透性利尿藥,能將周圍組織及腦組織的水分吸入血中隨尿排出,從而降低顱內壓,消除水腫,對治療腦水腫與循環衰竭有效。
(五)苯甲醇
苯甲醇又名芐醇,常以酯的形式存在於植物香精油中。它是無色液體,有芳香味,沸點205℃,微溶於水,可與乙醇、乙醚混溶。
(六)龍腦
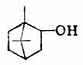
龍腦又名冰片或2-莰烷醇。它是透明或半透明片狀結晶,熔點204℃,通過蒸餾艾納香的新鮮葉子而得,藥用的冰片是用化學方法合成的。有特異香氣。它具有止痛消腫的作用。是人丹、冰硼散等中成藥的成分之一。
參看
| 關於「醫用化學/醇」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |