生物化學與分子生物學/真核基因轉錄水平的調控
| 醫學電子書 >> 《生物化學與分子生物學》 >> 基因表達調控 >> 真核基因表達調控 >> 真核基因轉錄水平的調控 |
| 生物化學與分子生物學 |
|
|
|
真核細胞的三種RNA聚合酶(Ⅰ、Ⅱ和Ⅲ)中,只有RNA聚合酶Ⅱ能轉錄生成mRNA,以下主要討論RNA聚合酶Ⅱ的轉錄調控。
(一)順式作用組件(cisacting elements)
真核基因的順式調控組件是基因周圍能與特異轉錄因子結合而影響轉錄的DNA序列。其中主要是起正性調控作用的順式作用組件,包括啟動子(promoter)、增強子(enhancer);近年又發現起負性調控作用的組件棗沉寂子(silencer)。
1.啟動子 與原核啟動子的含義相同,是指RNA聚合酶結合併起動轉錄的DNA序列。但真核同啟動子間不像原核那樣有明顯共同一致的序列,而且單靠RNA聚合酶難以結合DNA而起動轉錄,而是需要多種蛋白質因子的相互協調作用,不同蛋白質因子又能與不同DNA序列相互作用,不同基因轉錄起始及其調控所需的蛋白因子也不完全相同,因而不同啟動子序列也很不相同,要比原核更複雜、序列也更長。真核啟動子一般包括轉錄起始點及其上游約100-200bp序列,包含有若干具有獨立功能的DNA序列元件,每個元件約長7-30bp。最常見的哺乳類RNA聚合酶Ⅱ啟動子中的元件序列見表19-1。
表19-1 哺乳類RNA聚合酶Ⅱ啟動子中常見的元件
| 元件名稱 | 共同序列 | 結合的蛋白因子 | ||
| 名稱 | 分子量 | 結合DNA長度 | ||
| TATAbox | TATAAAA | TBP | 30,000 | ~10bp |
| GC box | GGGCGG | SP-1 | 105,000 | ~20bp |
| CAA box | GGCCAATCT | CTF/NF1 | 60,000 | ~22bp |
| Octamer | ATTTGCAT | Oct-1 | 76,000 | ~10bp |
| Oct-2 | 53,000 | ~20bp | ||
| kB | GGGACTTTCC | NFkB | 44,000 | ~10bp |
| ATF | GTGACGT | AFT | ? | 20bp |
啟動子中的元件可以分為兩種:
①核心啟動子元件(core promoter element) 指RNA聚合酶起始轉錄所必需的最小的DNA序列,包括轉錄起始點及其上游-25/-30bp處的TATA盒。核心元件單獨起作用時只能確定轉錄起始位點和產生基礎水平的轉錄。
②上游啟動子元件(upstream promoter element) 包括通常位於-70bp附近的CAAT盒和GC盒、以及距轉錄起始點更遠的上游元件。這些元件與相應的蛋白因子結合能提高或改變轉錄效率。不同基因具有不同的上游啟動子元件,其位置也不相同,這使得不同的基因表達分別有不同的調控。圖19-14以人金屬硫蛋白基因為例子,說明真核基因上游啟動子元件的組織情況和各元件相應結合的轉錄因子。
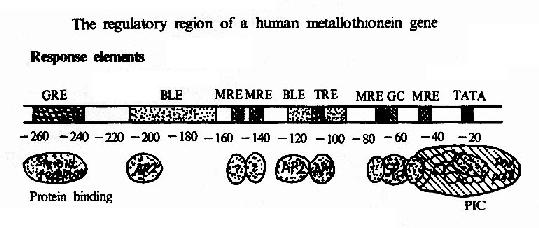
圖19-14 人金屬硫蛋白基因的調控區
2.增強子 是一種能夠提高轉錄效率的順式調控元件,最早是在SV40病毒中發現的長約200bp的一段DNA,可使旁側的基因轉錄提高100倍,其後在多種真核生物,甚至在原核生物中都發現了增強子。增強子通常佔100-200bp長度,也和啟動子一樣由若干組件構成,基本核心組件常為8-12bp,可以單拷貝或多拷貝串連形式存在。增強子的作用有以下特點:
①增強子提高同一條DNA鏈上基因轉錄效率,可以遠距離作用,通常可距離1-4kb、個別情況下離開所調控的基因30kb仍能發揮作用,而且在基因的上游或下游都能起作用。
②增強子作用與其序列的正反方向無關,將增強子方向倒置依然能起作用。而將啟動子倒就不能起作用,可見增強子與啟動子是很不相同的。
③增強子要有啟動子才能發揮作用,沒有啟動子存在,增強子不能表現活性。但增強子對動子沒有嚴格的專一性,同一增強子可以影響不同類型啟動子的轉錄。例如當含有增強子的病毒基因組整合入宿主細胞基因組時,能夠增強整合區附近宿主某些基因的轉錄;當增強子隨某些染色體段落移位時,也能提高移到的新位置周圍基因的轉錄。使某些癌基因轉錄表達增強,可能是腫瘤發生的因素之一。
④增強子的作用機理雖然還不明確,但與其他順式調控元件一樣,必須與特定的蛋白質因結合後才能發揮增強轉錄的作用。增強子一般具有組織或細胞特異性,許多增強子只在某些細胞或組織中表現活性,是由這些細胞或組織中具有的特異性蛋白質因子所決定的。
3.沉寂子 最早在酵母中發現,以後在T淋巴細胞的T抗原受體基因的轉錄和重排中證實這種負調控順式元件的存在。目前對這種在基因轉錄降低或關閉中起作用的序列研究還不多,但從已有的例子看到:沉寂子的作用可不受序列方向的影響,也能遠距離發揮作用,並可對異源基因的表達起作用。
(二)反式作用因子(transactingfactors)
以反式作用影響轉錄的因子可統稱為轉錄因子(transcription factors, TF)。RNA聚合酶是一種反式作用於轉錄的蛋白因子。在真核細胞中RNA聚合酶通常不能單獨發揮轉錄作用,而需要與其他轉錄因子共同協作。與RNA聚合酶Ⅰ、Ⅱ、Ⅲ相應的轉錄因子分別稱為TFⅠ、TFⅡ、TFⅢ,對TFⅡ研究最多。表19-2列出真核基因轉錄需要基本的TFⅡ。
表19-2 RNA聚合酶Ⅱ的基本轉錄因子
| 轉錄因子 | 分子量(kD) | 功能 |
| TBP | 30 | 與TATA盒結合 |
| TFⅡ-B | 33 | 介導RNA聚合酶Ⅱ的結合 |
| TFⅡ-F | 30,74 | 解旋酶 |
| TFⅡ-E | 34,37 | ATP酶 |
| TFⅡ-H | 62,89 | 解旋酶 |
| TFⅡ-A | 12,19,35 | 穩定TFⅡ-D的結合 |
| TFⅡ-I | 120 | 促進TFⅡ-D的結合 |
以前認為與TATA盒結合的蛋白因子是TFⅡ-D,後來發現TFⅡ-D實際包括兩類成分:與TATA盒結合的蛋白是TBP(TATAbox binding protein),是唯一能識別TATA盒並與其結合的轉錄因子,是三種RNA聚合酶轉錄時都需要的;其他稱為TBP相關因子(TBPassociated factors TAF),至少包括8種能與TBP緊密結合的因子。轉錄前先是TFⅡ-D與TATA盒結合;繼而TFⅡ-B以其C端與TBP-DNA複合體結合,其N端則能與RNA聚合酶Ⅱ親和結合,接著由兩個亞基組成的TFⅡ-F加入裝配,TFⅡ-F能與RNA聚合酶形成複合體,還具有依賴於ATP供給能量的DNA解旋酶活性,能解開前方的DNA雙螺旋,在轉錄鏈延伸中起作用。這樣,啟動子序列就與TFⅡ-D、B、F及RNA聚合酶Ⅱ結合形成一個「最低限度」能有轉錄功能基礎的轉錄前起始複合物(preintitiationcomplex, PIC),能轉錄mRNA。TFⅡ-H是多亞基蛋白複合體,具有依賴於ATP供給能量的DNA解旋酶活性,在轉錄鏈延伸中發揮作用;TFⅡ-E是兩個亞基組成的四聚體,不直接與DNA結合而可能是與TFⅡ-B聯繫,能提高ATP酶的活性;TFⅡ-E和TFⅡ-H的加入就形成完整的轉錄複合體(圖19?5),能轉錄延伸生成長鏈RNA,TFⅡ-A能穩定TFⅡ-D與TATA盒的結合,提高轉錄效率,但不是轉錄複合體一定需要的。
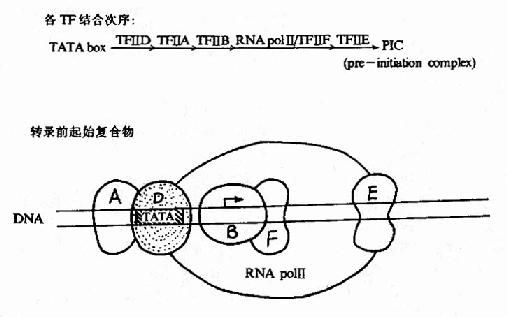
圖19-15 RNA聚合酶Ⅱ轉錄複合體的形成示意圖
以上所述是典型的啟動子上轉錄複合體的形成,但有的真核啟動子不含TATA盒或不通過TATA盒開始轉錄。例如有的無TATA盒的啟動子是靠TFⅡ-I和TFⅡ-D共同組成穩定的轉錄起始複合體開始轉錄的。由此可以看到真核轉錄起始的複雜性。
不同基因由不同的上游啟動子元件組成,能與不同的轉錄因子結合,這些轉錄因子通過與基礎的轉錄複合體作用而影響轉錄的效率。現在已經發現有許多不同的轉錄因子,看到的現象是:同一DNA序列可被不同的蛋白因子所識別;能直接結合DNA序列的蛋白因子是少數,但不同的蛋白因子間可以相互作用,因而多數轉錄因子是通過蛋白質-蛋白質間作用與DNA序列聯繫並影響轉錄效率的(見圖19-16)。轉錄因子之間或轉錄因子與DNA的結合都會引起構象的變化,從而影響轉錄的效率。
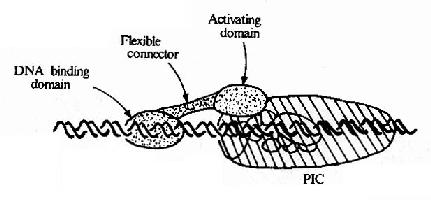
圖19-16 轉錄因子與轉錄複合體相互作用模式圖
圖19-16所示,作為蛋白質的轉錄因子從功能上分析其結構可包含有不同區域,①DNA結合域(DNa binding domain),多由60-100個胺基酸殘基組織的幾個亞區組成;②轉錄激活域(activating domain),常由30-100胺基酸殘基組成,這結構域有富含酸性胺基酸、富含谷氨醯胺、富含脯氨酸等不同種類,以酸性結構域最多見;③連接區,即連接上兩個結構域的部分。不與DNA直接結合的轉錄因子沒有DNA結合域,但能通過轉錄激活域直接或間接作用於轉錄複合體而影響轉錄效率。
與DNA結合的轉錄因子大多以二聚體形式起作用,與DNA結合的功能域常見有以下幾種:
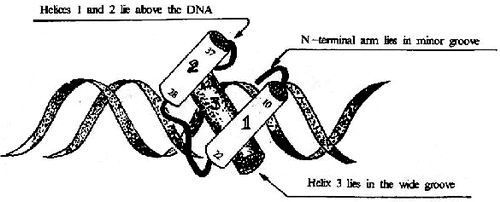
圖19-17 HTH結構及其與DNA的結合
①螺旋轉角螺旋(helixturnhelix, HTH)及螺旋-環-螺旋(helixloophelix,HLH) 這類結構至少有兩個α螺旋,其間由短肽段形成的轉角或環連接,兩個這樣的motif結構以二聚體形式相連,距離正好相當於DNA一個螺距(3.4nm),兩個α螺旋剛好分別嵌入DNA的深溝(圖19-17)。
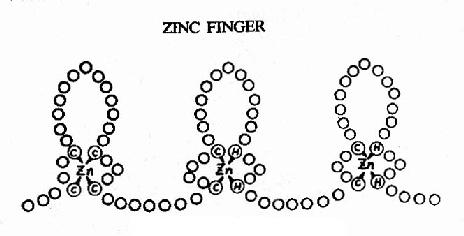
圖19-18 蛋白質的鋅指結構
②鋅指(zinc finger) 其結構如圖19-18所示,每個重複的「指」狀結構約含23個胺基酸殘基,鋅以4個配價鍵與4個半胱氨酸、或2個半胱氨酸和2個組氨酸相結合。整個蛋白質分子可有2?個這樣的鋅指重複單位。每一個單位可以其指部伸入DNA雙螺旋的深溝,接觸5個核苷酸。例如與GC盒結合的轉錄因子SP1中就有連續的3個鋅指重複結構。
③鹼性-亮氨酸拉鏈(basic leucine zipper, bZIP),該結構的特點是蛋白質分子的肽鏈上每隔6個胺基酸就有一個亮氨酸殘基,結果就導致這些亮氨酸殘基都在α螺旋的同一個方向出現。兩個相同結構的兩排亮氨酸殘基就能以疏水鍵結合成二聚體,該二聚體的另一端的肽段富含鹼性胺基酸殘基,借其正電荷與DNA雙螺旋鏈上帶負電荷的磷酸基團結合。若不形成二聚體則對DNA的親和結合力明顯降低。在肝臟、小腸上皮、脂肪細胞和某些腦細胞中有稱為C/EBP家族的一大類蛋白質能夠與CAAT盒和病毒增強子結合,其特徵就是能形成bZIP二聚體結構。
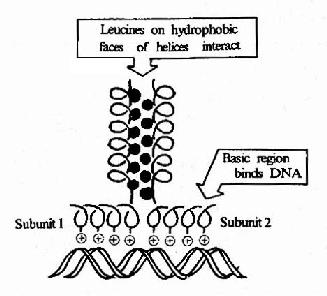
圖19-19 鹼性亮氨酸拉鏈結構及其與DNA的結合
從上述可見:轉錄調控的實質在於蛋白質與DNA、蛋白質與蛋白質之間的相互作用,構象的變化正是蛋白質和核酸「活」的表現。但對生物大分子間的辨認、相互作用、結構上的變化及其在生命活動中的意義,人們的認識和研究還只在起步階段,其中許多內容甚至重要的規律我們可能至今還一無所知,有待於努力探索。
| 關於「生物化學與分子生物學/真核基因轉錄水平的調控」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |