生物化學與分子生物學/RNA轉錄後的加工與修飾
| 醫學電子書 >> 《生物化學與分子生物學》 >> RNA的生物合成 >> RNA轉錄後的加工與修飾 |
| 生物化學與分子生物學 |
|
|
|
不論原核或真核生物的rRNAs都是以更為複雜的初級轉錄本形式被合成的,然後再加工成為成熟的RNA分子。然而絕大多數原核生物轉錄和翻譯是同時進行的,隨著mRNA開始的DNA上合成,核蛋白體即附著在mRNA上並以其為模板進行蛋白質的合成,因此原核細胞的mRNA並無特殊的轉錄後加工過程,相反,真核生物轉錄和翻譯在時間和空間上是分天的,剛轉錄出來的mRNA是分子很大的前體,即核內不均一RNA。hnRNA分子中大約只有10%的部分轉變成成熟的mRNA,其餘部分將在轉錄後的加工過程中被降解掉。
(一)mRNA的加工修飾
原核生物中轉錄生成的mRNA為多順反子,即幾個結構基因,利用共同的啟動子和共同終止信號經轉錄生成一條mRNA,所以此mRNA分子編碼幾種不同的蛋白質。例如乳糖操縱子上的Z、Y及A基因,轉錄生成的mRNA可翻譯生成三種酶,即半乳糖苷酶,透過酶和乙醯基轉移酶。原核生物中沒有核模,所以轉錄與翻譯是連續進行的,往往轉錄還未完成,翻譯已經開始了,因此原核生物中轉錄生成的mRNA沒有特殊的轉錄後加工修飾過程。
真核生物轉錄生成的mRNA為單順反子,即一個mRNA分子只為一種蛋白質分子編碼。
真核生物mRNA的加工修飾,主要包括對5』端和3』端的修飾以及對中間部分進行剪接。
1.在5』端加帽
成熟的真核生物mRNA,其結構的5』端都有一個m7G-PPNmN結構,該結構被稱為甲基鳥苷的帽子。如圖17-9所示。鳥苷通過5』-5』焦磷酸鍵與初級轉錄物的5』端相連。當鳥苷上第7位碳原子被甲基化形成m7G-PPNmN時,此時形成的帽子被稱為「帽0」,如果附m7G-PPNmN外,這個核糖的第「2」號碳上也甲基化,形成m7G-PPNm,稱為「帽1」,如果5』末端N1和N2中的兩個核糖均甲基化,成為m7G-PPNmPNm2,稱為「帽2」。從真核生物帽子結構形成的複雜可以看出,生物進化程度越高,其帽子結構越複雜。
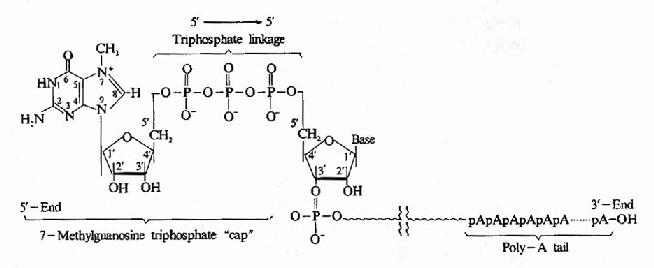
圖17-9 Post-transcriptional modification of mRNa showing the7-methylguanosine cap and poly-A tail.
真核生物mRNA 5』端帽子結構的重要性在於它是mRNa 做為翻譯起始的必要的結構,對核糖體對mRNA的識別提供了信號,這種帽子結構還可能增加mRNA的穩定性,保護mRNa 免遭5』外切核酸酶的攻擊。
2.在3』端加尾
大多數的真核mRNA 都有3』端的多聚尾巴(A),多聚(A)尾巴大約為200bp。
多聚(A)屠巴不是由DNA編碼的,而是轉錄後在核內加上去的。受polyA聚合酶催化,該酶能識別,mRNa 的游離3』-OH端,並加上約200個A殘基。

近年來已知,在大多數真核基因的3』一端有一個AATAA序列,這個序列是mRNa 3』-端加polyA尾的信號。靠核酸酶在此信號下游10-15鹼基外切斷磷酸二酯鍵,在polyA聚合酶催化下,在3』-OH上逐一引入100-200個A鹼基。關於polyA尾巴的功能問題儘管經過極其廣泛的探索,但還不完全清楚。有人推測polyA可能與mRNA從細胞核轉送到細胞質有關,但是相當數量,的沒有polyA屠巴的mRNA如組蛋白mRNA,也照樣通過核膜進入細胞質。還有人認為這種結構對真核mRNA的翻譯效率具有某種作用,並能穩定mRNA結構,保持一定的生物半衰期。
3.mRNA前體(hnRNA)的拼接
原核生物的結構基因是連續編碼序列,而真核生物基因往往是斷裂基因,即編碼一個蛋白質分子的核苷酸序列被多個插入片斷所隔開,一個真核生物結構基因中內含子的數量,往往與這個基因的大小有關,例如胰島素是一個很小的蛋白質,它結構基因只有兩個內含子,而有些很大的蛋白質,它的結構基因中可以有幾十個內含子。經過複雜的過程後,切去內元,將有編碼意義的核苷酸片段(Extron外元也叫外顯子)連接起來(圖17-10)。
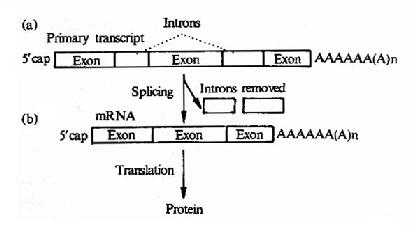
圖17-10 Primary polymerase 11transcript of a eukaryote gene showing(a)introns after capping and addition of polyA tail.(b)Excision of introns toform the mature mRNA is called splicing.
真核生物的結構的基因中具有可表達活性的外顯子,也含有無表達活性的內含子,但內含子序列下是無意義的,越來越多的實驗證明有許多基因中的內含子參與基因表達調控,在轉錄時,外顯子及內含子均轉錄到hnRNA中。在細胞核中hnRNA進行剪接作用,首先在核酸內切酶作用下剪切掉內含子;然後在連接酶作用下,將外顯子各部分連接起來,而變為成熟的mRNA,這就是剪接作用,也有少數基因的hnRNA不需進行剪接作用,例如α-干擾素基因,圖17-11以卵清蛋白基因為例,介紹一個典型的轉錄及加工過程。
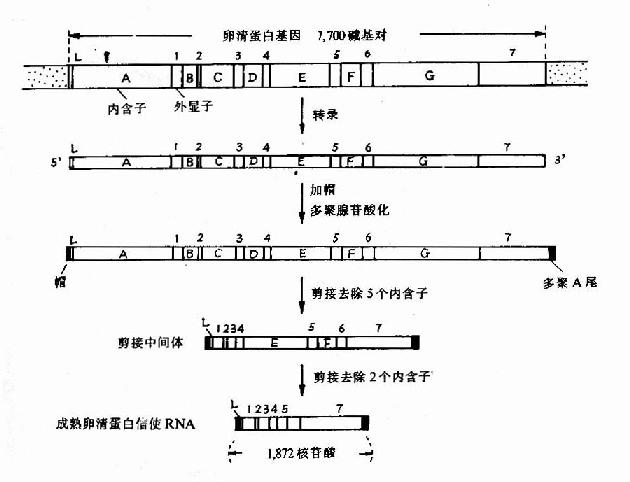
圖17-11 卵清蛋白基因轉錄及加工過程
圖中外顯示以1、2、3、4……表示,內含子以A、B、C、D…表示
mRNA的拼接,需要在拼接部位有供拼接識別的保守性強的一致順序,通過對100多種真核細胞基因的分析,發現外元和內元拼接部位部分鹼基順序有一定的規律(見表17-4)。
表17-4 含有內元的轉錄產物其拼接處的鹼基順序
| 基因區域 | Exon | Intron | Exon |
| 卵清蛋白內元2 | UAAG GUGA | ~~~~~~~ | ACAGGUUG |
| 卵清蛋白內元3 | UCAG GUAC | ~~~~~~~ | UCAGUCUG |
| β-珠蛋白內元1 | GCAG GUUG | ~~~~~~~ | UCAGGCUG |
| β-珠蛋白內元2 | CAGG GUGA | ~~~~~~~ | ACAGUCUC |
| Igλ內含子1 | UCAG GUCA | ~~~~~~~ | GCAGGGGC |
| SV40病毒早期T抗原 | UAAG GUAA | ~~~~~~~ | UUAGAUUC |
表中劃線的鹼基對拼接識別有重要作用,如將兔的β-珠蛋白的拼接部位的GT改為AT後,拼接反應即受到影響。
mRNA前體拼機制
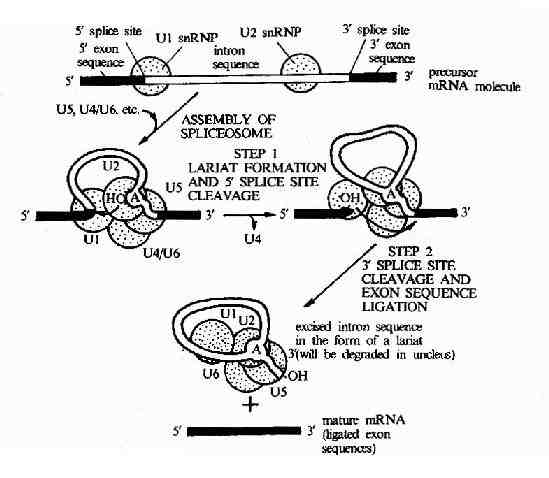
圖17-12 The RNA splicing mechanism.RNA splicing is catalyzed by aspliceosome formed from the assembly of U1,U2,U5,and sn RNPs(shown as greencircles )plus other components (not shown).After assembly of the spliceosome,the reaction occures in two speps:in step 1the branch-point A nucleotide inthe intron sequence,which is located colse to the 3'splice site ,attacks the5'splice site and cleaves it;the cut 5'end of the intron sequence therebybecomes covalently linked to this A nucleotide,forming the branched nucleotideshown in Figure 8-55.In step 2 the 3'-OH end of the first exon sequence,whichwas created in the first step,adds to the beginning of the second exonsequence,cleqving the RNA molecule at the 3'splice site;the two exon sequencesare thereby joined to each other and the intron sequence is released ad aribosone.These splicing reactions occur im the nucleus and gengerate mRNamolecules from primary RNA transcripts (mRNA precursor molecules).
mRNA拼接反應需要有核內小分子RNA參與它們與蛋白質形成的複合物稱為小核糖核蛋白顆粒,SnRNA分別被命名為U1,U2,U3,U4,U5,和U6RNA。SnRNA中的U2RNA由與內元右端拼接部位附近的UACUAA順序高度互補,形成一個環狀結構,由特定的酶來識別切除該環狀結構,完成拼接過程,如圖17-12所示。
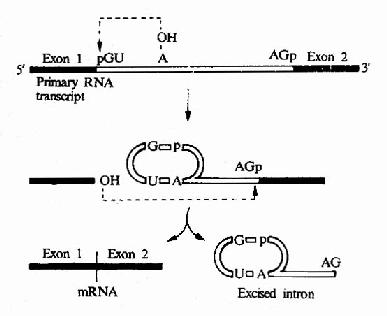
圖17-13 Mechanim of mRNa splicing.Note that,for clarity,the process is shownin two stages;energy is not required for the process since transesterificationreactions are involved.
真核生物 mRNA前體在剪接過程中,還可以形成套索樣的結構,在內含子序列中常有一個分支部位的腺苷酸殘基,它的2』-OH可以自動攻擊內含子5』端與外顯子1連接的磷酸二酯鍵,切開了外噗子1,而腺苷酸原來已有3』,5』--磷酸二酯鍵相連的兩個相鄰的核苷酸殘基,加上此3』,5』-磷酸二酯鍵連接後,在腺苷酸處出現了一個套索,已被切下的外顯子1的3』-OH攻擊內含子3』末端與外顯子2之間的3』,5』-磷酸二酯鍵,鍵斷裂後,內含子以套索的形式被節下來,此時外顯子1和外顯子2可以連接起來(圖17-13)。
不論拼接過程如何,拼接必須極為精確,否則會導致遺傳信息傳遞障礙,合成的蛋白質可能喪失其正常的功能。我國南方廣大地區是β-地中海貧血的高發區,這是由於β-珠蛋白鏈的合成受到部分或完全抑制所引起的一種血紅蛋白病。實驗表明β-珠蛋白基因元1中核苷酸的點突變改變了正常拼接部位的鹼基順序,結果造成錯誤部位的拼接。加工成熟的mRNA雖能翻譯,但產物不是正常的β-珠蛋白,結果引起血紅蛋白級結構和功能的改變。
(二)rRNA轉錄後加工
原核生物rRNA轉錄後加工,包括以下幾方面:①rRNA前體被大腸桿菌RNaseⅢ,RNaseE等剪切成一定鏈長的rRNA分子;②rRNA在修飾酶催化下進行鹼基修飾;③rRNA與蛋白質結合形成核糖體的大、小亞基(見圖17-14)
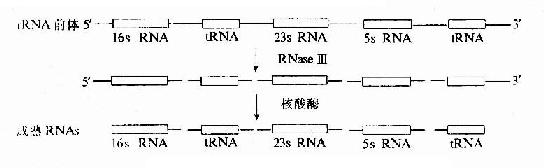
圖17-14 大腸桿菌rRNA前體的加工
真核生物rRNA前體比原核生物大,哺乳動物的初級轉錄產物為45s,低等真核生物的rRNA前體為38s,真核生物5sRNA前體獨立於其他三種rRNA的基因轉錄(圖17-15)。
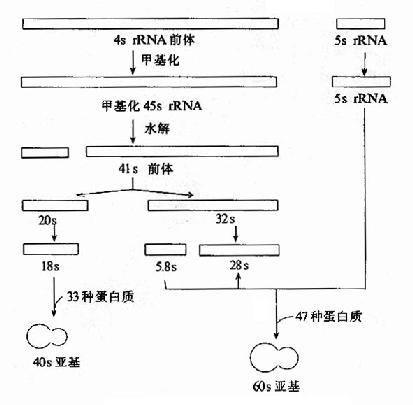
圖17-15 真核生物rRNA前體的加工
真核生物rRNA前體中含有插入順序,rRNA前體要形成成熟的rRNA,需要經過拼接反應。例如,四膜蟲的rRNA前體的拼接是一種無酶催化的自動拼接過程。四膜蟲基因組內,26srRNA編碼的區域內有413bp的插入順序。該插放序列可以不消耗能量從rRNA前體中被除掉。用SDS煮沸和用蛋白酶外理等破壞酶活性辦法,都不能破壞拼接活性,但反應中Mg2+和鳥嘌呤核苷酸是必在的。用32P-GTP進行追蹤實驗表明,起始過程是GTP在插入順序5』端發生親核反應,同時GMP與5』端切點的切除段形成磷酸二酯鍵並使原RNA斷開。第二步是5』切點的外元3』-OH與3』切點的外元5』-P共價連接,獲得成熟的rRNA,被切除部分最後環化,形成一個環狀結構,同時從5』端去掉一個核苷酸啐片。剩餘部分連接成399核苷酸的環狀產物,再經過幾步,最後切下一個19個核苷酸的線性內含子序列即L-19,它具有催化活性,上面的剪接作用,是由內含子本身的催化性質決定的(圖17-16)。
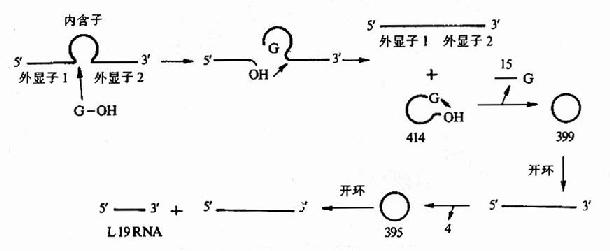
圖17-16 四膜蟲rRNA前體的自我剪接
這種rRNA的自身剪接反應給人們一個提示:即RNA分子也有酶的催化活性。這向酶的化學本質是蛋白質這一傳統概念提出了挑戰。這種有酶催化活性的RNA分子命名為Ribozyme。T.Cech和S.Altman各自分別發現RNA具有催化作用,他們的發現對於了解生命進行過程有重要意義。很可能在原始生命中,RNA所催化的斷裂一連接反應是最早出現的催化過程。為此,他們共同獲得了1989年Nobel化學獎。
從大多數Ribozymw的結構中發現一些特徵,例如:錘頭狀結構的RNA分子有13個保守的核苷酸序列,如果它們中的鹼基改變會使這種催化活性失去作用。根據這種特片,科學家們在體外沒計並人工合成這種RNA分子,用於抗腫瘤及抗病毒的實驗中(圖17-17)。
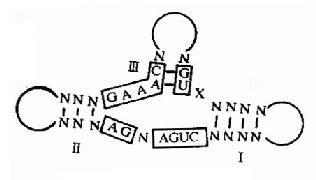
圖17-17 錘頭結構模式圖
(三)tRNA轉錄後的加工修飾
原核生物和真核生物剛轉錄生成的tRNA前體一般無生物活性,需要進行①剪切和拼接②鹼基修飾③3』-OH連接-ACC結構(圖17-18)。
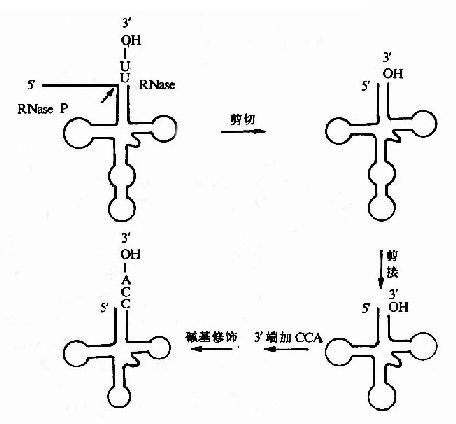
圖17-18 tRNA前體的加工
①tRNA前體在tRNA剪切酶的作用下,切成一定在小的tRNA分子。大腸桿菌RNase P可特異剪切tRNA前體的5』旁順序,因此,該酶被稱為tRNA5』成熟酶。除了RNaseP外,tRNA前體的剪切尚需要一個』-核酸內切酶,這可將tRNA前體3』端的一段核苷酸序列切下來。此外RNaseD是tRNA3』端成熟酶。近年來的研究表明大腸桿菌RNaseP是一種非常特殊的酶分子,它是由RNA和蛋白質組成,最近發現RNAaseP分子中的RNA部分在某些條件下,可以單獨地催化tRNA前體的加工成熟,這個發現和四膜蟲tRNA能自我拼接被認為是近十年來生化領域內最令人鼓舞的發現之一。說明RNA分子確具有酶的催化活性。經過剪切後的tRNA分子還要在拼接酶作用下,將成熟tRNA分子所需的片段拼起來。
②成熟的tRNA分子中有許多的稀有鹼基,因此tRNA在甲基轉移酶催化下,某些嘌呤生成甲基嘌呤如A→mA,G→mA。有些尿嘧啶還原為雙氫尿嘧啶。尿嘧啶核苷轉變不假尿嘧啶核苷。某些腺苷酸脫氨基為成為次黃嘌呤核苷酸(Ⅰ)
③3』末端加上CCA:在核苷酸轉移酶作用下,3』--末端除去個別鹼基後,換上tRNA分子統一的CCA-OH末端,完成tRNA分子中的胺基酸臂結構。
| 關於「生物化學與分子生物學/RNA轉錄後的加工與修飾」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |