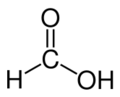
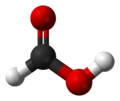
甲酸
| A+醫學百科 >> 甲酸 |
| 甲酸 | |||
|---|---|---|---|
|
|
|||
| IUPAC名 Formic acid, Methanoic acid |
|||
| 別名 | HCOOH | ||
| 識別 | |||
| CAS號 | 64-18-6 | ||
| SMILES |
|
||
| RTECS | LQ4900000 | ||
| 性質 | |||
| 化學式 | CH2O2 HCOOH |
||
| 摩爾質量 | 46.0254 g·mol⁻¹ | ||
| 外觀 | 無色發煙液體 | ||
| 密度 | 1.22 g/mL (液) | ||
| 熔點 | 8.4 °C (47.1 °F) | ||
| 沸點 | 100.8 °C (213.3 °F) | ||
| 溶解性(水) | 混溶 | ||
| pKa | 3.744 | ||
| 黏度 | 1.57 cP, 26 °C | ||
| 結構 | |||
| 分子構型 | 平面 | ||
| 偶極矩 | 1.41 D (氣態) | ||
| 危險性 | |||
| 警示術語 | R:R10-R35 | ||
| 安全術語 | S:S1/2-S23-S26-S45 | ||
| MSDS | ScienceLab.com | ||
| 主要危害 | 腐蝕性、刺激性 | ||
| NFPA 704 | |||
| 閃點 | 69 °C (156 °F) | ||
| 相關物質 | |||
| 相關羧酸 | 乙酸、丙酸 | ||
| 相關化學品 | 甲醛、甲醇 | ||
| 若非註明,所有數據均出自一般條件(25 ℃,100 kPa)下。 | |||
甲酸(英文:Formic acid)又稱作蟻酸,化學式為HCOOH。螞蟻分泌物和蜜蜂的分泌液中含有蟻酸,當初人們蒸餾螞蟻時製得蟻酸,故有此名。甲酸無色而有刺激氣味,且有腐蝕性,人類皮膚接觸後會起泡紅腫。熔點8.4℃,沸點 100.8℃。由於甲酸的結構特殊,它的一個氫原子和羧基直接相連。也可看做是一個羥基甲醛。因此甲酸同時具有酸和醛的性質。在化學工業中,甲酸被用於橡膠、醫藥、染料、皮革種類工業。
目錄 |
性質
甲酸與水和大多數的極性有機溶劑混溶,在烴中也有一定的溶解性。在烴中及氣態下, 甲酸以通過以氫鍵結合的二聚體形態出現。在氣態下,氫鍵導致甲酸氣體與理想氣體狀態方程之間存在較大的偏差。液態和固態的甲酸由連續不斷的通過氫鍵結合的甲酸分子組成。
甲酸具有與大多數其他羧酸相同的性質,儘管在通常情況下甲酸不會生成醯氯或者酸酐。直到不久以前,所有試圖將甲酸轉化成這些衍生物的嘗試都以產物一氧化碳告終。甲酸酐可由甲醯氟和甲酸鈉在零下78攝氏度反應得到。甲醯氯可由將氯化氫氣體通過零下60度1-甲醯基咪唑的一氯甲烷溶液得到。甲酸脫水分解為一氧化碳和水。甲酸具有和醛類似的還原性。它能起銀鏡反應,把銀氨絡離子中的銀離子還原成金屬銀,而自己被氧化成二氧化碳和水:
HCOOH+2AgOH→2Ag+2H2O+CO2
甲酸是唯一能和烯烴進行加成反應的羧酸。甲酸在酸的作用下(如硫酸,氫氟酸),和烯烴迅速反應生成甲酸酯。但是類似於Koch反應的副反應也會發生,產物是更高級的羧酸。
大多數的甲酸鹽溶於水。
製備
製備其他化學藥品(尤其是乙酸)的過程中,大量的甲酸作為副產物被生產出來。 然而這樣的製備遠遠的不能滿足目前對甲酸的需要,所以有些甲酸被直接生產。
- CH3OH + CO → HCOOCH3
在工業生產中, 此反應在液態和加壓的狀態下進行。 典型的反應條件為80攝氏度和40個大氣壓。廣泛使用的鹼為甲醇鈉。水解甲酸甲酯得到甲酸。
- HCOOCH3 + H2O → HCOOH + CH3OH
水解甲酸甲酯需要大量的水來保證反應順利進行。 有些生產商使用一種間接的水解途徑, 即先將甲酸甲酯和氨反應產生甲醯胺,然後用硫酸水解甲醯胺得到甲酸:
- HCOOCH3 + NH3 → HCONH2 + CH3OH
- 2HCONH2 + 2H2O + H2SO4 → 2HCOOH + (NH4)2SO4
這種技術有其自身缺點,尤其是在對副產物硫酸銨的處理上。有些生產商最近發展了一類節能的方法,即將甲酸從直接水解的大量水溶液中提取出來。在其中一種方法(由巴斯夫所使用)中,甲酸在有機鹼的作用下由濕法萃取得到。
在實驗室製備中,甲酸可由在無水丙三醇中加熱草酸,然後蒸汽蒸餾得到。另外一種製備方法(必須要在通風櫥中進行)是在鹽酸作用下的異乙腈的水解。
- C2H5NC + 2H2O → C2H5NH2 + HCOOH
異腈的製備由乙胺和氯仿反應獲得。(異腈過於令人不快的氣味使此反應必須在通風櫥中進行。)
安全
化學性質
甲酸具有羧酸的通性。但甲酸同時具有一個醛基,這使它可以被進一步氧化:
- 2HCOOH + O2 → 2CO2 + 2H2O
甲酸在濃硫酸或氧化鋁催化下加熱脫水生成一氧化碳,這是實驗室製取純淨一氧化碳的方法。
- HCOOH → CO + H2O (在濃硫酸催化下加熱)
- HCOOH → CO2 + H2
參見
參考資料
參考來源
| 關於「甲酸」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |