三磷酸腺苷合酶
| A+醫學百科 >> 三磷酸腺苷合酶 |
三磷酸腺苷合酶或ATP合酶,三磷酸腺苷酶(ATPase)的一種,在這裡並特指F類的FoF1ATP合酶(F Type FoF1 ATP Synthase)。它利用呼吸鏈產生的質子的電化學勢能,通過改變蛋白質的結構來進行ATP的合成。
| ATP合酶 | |||||||
|---|---|---|---|---|---|---|---|
|
|||||||
| 識別碼 | |||||||
| EC編號 | 3.6.3.14 | ||||||
| CAS號 | 9000-83-3 | ||||||
| 資料庫 | |||||||
| IntEnz | IntEnz瀏覽 | ||||||
| BRENDA | BRENDA入口 | ||||||
| ExPASy | NiceZyme瀏覽 | ||||||
| KEGG | KEGG入口 | ||||||
| MetaCyc | 代謝路徑 | ||||||
| PRIAM | 概述 | ||||||
| PDB | RCSB PDB PDBe PDBsum | ||||||
| 基因本體 | AmiGO / EGO | ||||||
|
|||||||
目錄 |
分布
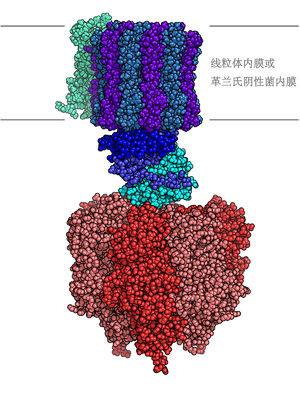
FoF1三磷酸腺苷合酶分子模型
通過使用電子顯微鏡,蘑菇狀的F型ATP酶可以在真核細胞的粒線體內膜和原核生物的細胞膜上觀察到。
位置
在真核細胞中,ATP合酶存在於粒線體的內膜或,Fo亞單位存在於膜內,F1
- F型ATP酶(ATPase)– 也稱為『Phosphorylation Factor』存在在各種生物中,利用電化學勢進行ATP的合成。
- P型ATP酶(也稱 E1-E2 ATP酶)– 存在在細菌,和真核細胞中,消費ATP進行離子運輸。
- V型ATP酶 – 存在在液泡(Vesicle),如高爾基體,溶酶體上,消費ATP進行離子運輸
- A型ATP酶 – 存在在古細菌(Archaea)中,雖然有F型ATP酶類似的功能--ATP合成,但是在結構上其更接近與V型ATP酶,反映了古細菌為適應極端條件的進化。
結構
當前,原核生物的F型ATP酶的結構已經比較清楚了:
- F1單元 – α(3個)、β(3個)、γ(1個)、δ(1個)、ε(1個)
- Fo單元 – a(1個)、b(2個)、c(9-12個)
真核生物的F型ATP酶F1單元的種類的數量與原核生物相同、Fo單元的結構與原核生物相似,但是亞單位的數量不是很明了。
ATP合酶的反應
F1 單元催化以下ATP合成反應。
F1單元催化的反映是可逆的,在進行離子運輸時,進行ATP水解反應。
Fo單元形成離子通道,質子可以從中通過:
- H+in
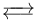 H+out
H+out
當質子利用電化學勢能通過Fo單元時,可以帶動和其連接的軸(γ亞單位),改變F1單元的結構,進而調節F1單元與ATP和ADP:Pi的結合能(Binding Energy),降低ATP生成的活化能,達到ATP合成的目的:
- ADP + Pi + 3 H+out → ATP + 3 H+in
ATP酶γ亞單位的旋轉
在ATP酶的酶學模型中,驗證其γ軸是否旋轉佔有重要地位,1997年,英國自然雜誌(vol. 386, pp. 299–302)刊了日本科學家題為"Direct observation of the rotation of F1-ATPase"的文章,報導了ATP合成酵素F1單元可以通過水解ATP造成γ亞單位(軸)的旋轉,並進行了單分子觀察和錄像、該論文證明了Paul D. Boyer的「ATP合酶的旋轉理論」。同年Paul D. Boyer,John E. Walker和Jens C. Skou因ATP合酶的研究獲得諾貝爾化學獎。
歴史
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||
參考來源
出自A+醫學百科 「三磷酸腺苷合酶」條目 http://cht.a-hospital.com/w/%E4%B8%89%E7%A3%B7%E9%85%B8%E8%85%BA%E8%8B%B7%E5%90%88%E9%85%B6 轉載請保留此連結
| 關於「三磷酸腺苷合酶」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |