成體幹細胞
| A+醫學百科 >> 成體幹細胞 |
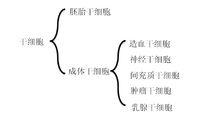
成體幹細胞(Adult Stem Cell,ASCs)是存在於人與哺乳動物已分化組織與器官中,具有自我更新、高度增殖和多向分化潛能的尚未分化的不成熟細胞群體。根據幹細胞所處的發育階段分為胚胎幹細胞(embryonic stem cell,ES細胞)和成體幹細胞(somatic stem cell)本詞條講述成體幹細胞,在適當的誘導條件下,可分化出組成該器官組織的各種細胞類型,替代生理性衰亡細胞在組織受損時起代償性增生作用,維持機體的正常結構和功能。ASCs在體外可跨系、甚至跨胚系分化為某些成熟細胞[3]。各種ASCs在體內外生長特性和表型可能不盡一致,但在組織結構中位置相對固定,處於一個由幹細胞、基底膜和調控細胞組成的微環境之中,形態學表現為細胞體積小,胞內細胞器稀少,細胞內RNA含量低。
ASCs通常處於靜息狀態,分裂緩慢,其分裂生長方式主要為對稱分裂和非對稱分裂。對稱分裂形成兩個相同的幹細胞,非對稱分裂生成一個分化細胞和一個幹細胞。ASCs在損傷或血小板活化、釋出組織生長因子的作用下被激活,取代失去生理活性的細胞或通過修復損傷來維持組織內環境的穩定。
目錄 |
成體幹細胞研究的優越性
雖然胚胎幹細胞(EmbryonicStemCell,ESC)幾乎可向所有的成年組織分化,但由於 (1)ESC是來源於人或動物胚胎內細胞團或原始生殖嵴的一種多能細胞系,其研究受到倫理學問題和取材困難等因素的限制,而主要通過動物實驗進行。 (2)ESC治療相當於異體移植,存在免疫排斥問題。
成體幹細胞與胚胎幹細胞相比,在應用上有更大的優勢: (1)ASCs存在於人體各種組織和器官中,來源廣泛,不涉及倫理問題。 (2)正常情況下ASCs處於靜止狀態,只有在病理情況下才顯示出一定的自我更新潛能,其導致細胞「永生化」甚至癌變的可能性較小。 (3)ASCs可產生一個含有多種細胞成分的特定組織,移植入患者體內後,有望產生該器官所有類型的細胞,達到在結構和功能上的完美修復或替代。 (4)一些類型的ASCs可向體內損傷甚至遠離其發源地的部位遷移,成為前體細胞並分化為終末成熟細胞,用來修復組織損傷。也可將其作為目的基因的理想載體。 (5)某些ASCs可分泌生長因子,發揮動員或保護該組織其他細胞的作用以加強移植效果。人們可以利用基因工程手段對ASCs進行操作,以補充患者組織中缺乏的某些成分。
成體幹細胞的分類
目前發現的ASCs主要有造血幹細胞、間充質幹細胞、神經幹細胞、表皮幹細胞、骨骼肌幹細胞、脂肪幹細胞、胰幹細胞、眼角膜幹細胞、肝臟幹細胞以及腸上皮幹細胞等。
造血幹細胞
造血幹細胞(HSC)在胚胎的早期就已出現,源於主動脈旁-胚臟壁和主動脈-性腺-中腎區,逐漸移植到卵黃囊、肝臟、脾臟及骨髓。HSC存在於骨髓、外周血、臍帶血中,在不同的細胞因子作用下在體外擴增及向紅系、粒系、巨核系等不同血細胞定向分化。應用PDGF體外擴增CD34造血幹細胞和CD41的巨核細胞已取得較為滿意的結果。HSC可分化成心肌細胞、骨骼肌細胞、肝細胞、血管內皮細胞以及分化為肺泡、支氣管、胃、腸、腎小球、皮膚等細胞。
間充質幹細胞
成人的間充質幹細胞(MSCs)主要來源於骨髓,不表達造血幹細胞表面抗原CD34、CD14及白細胞表面抗原CD45,而表達SH2、SH3、CD29、CD106和CD166等表面抗原。PDGF作為結締組織生長因子,對體外MSCs生長有促進作用。在合適的條件下,MSCs易誘導分化為間充質組織細胞如成骨細胞,也可分化為肝細胞、肌細胞、脂肪細胞、軟骨細胞、成骨細胞、神經細胞、成纖維細胞、上皮細胞、造血幹細胞和基質細胞,在一定條件下可形成肌小管和肌腱。
神經幹細胞
神經幹細胞(NeuralStemCell,NSC)分布於成人及胚胎的中樞神經及周圍神經,其特徵性抗原為神經巢蛋白。NSC可分化為不同類型的神經元、星型膠質細胞和少突膠質細胞,並表現相應的形態學和電生理學的能力。中樞神經細胞可分化為血細胞。
表皮幹細胞
皮膚皮脂腺開口處與立毛肌毛囊附著處之間的毛囊外根鞘處含有豐富的幹細胞。可用於自體和異體移植治療重度燒傷、慢性潰瘍等。從鼠皮膚分離獲得的幹細胞可轉化為神經元細胞、神經膠質細胞、平滑肌細胞和脂肪細胞等。
其他幹細胞
骨骼肌幹細胞可用於修復骨缺損等,也可分化為血細胞。脂肪組織中含有的ASCs可在體外被誘導分化為神經細胞、肌細胞、成骨細胞等。胰幹細胞可在體外誘導培養為胰島素分泌細胞。有研究發現用自體眼角膜緣幹細胞培養後形成的細胞層移植到患眼角膜表面,成功實現眼表面重建。腸上皮幹細胞在促進腸道損傷後結構與功能的完全修復上意義重大。肝臟幹細胞在肝功能重建、幹細胞癌治療以及基因治療方面有誘人的前景。
成體幹細胞可能的臨床應用
(1)組織損害類疾病:將ASCs直接移植給患者,如骨髓移植治療白血病,已獲一定療效。將ASCs注入冠狀動脈,能加速改變心肌梗死後斑痕的厚度和大小。將幹細胞注入骨骼肌能夠修復皮膚、角膜、肌腱、韌帶、關節盤和其他結締組織等。幹細胞經神經生長因子處理後能形成神經樣細胞,表達神經膠質酸性蛋白,促進中樞和外周神經組織的再生與修復,也可治療腦卒中。
(2)活性因子缺乏性疾病:將經過定向分化或基因修飾後的幹細胞進行篩選,把合格的細胞移植給病人,這兩種方法都屬於細胞替代,用於糖尿病、帕金森病等多種活性因子缺乏性疾病。
(3)器官替代:幹細胞技術的理想階段就是在體外進行器官克隆以供病人移植。與組織工程技術相結合,幹細胞替代治療的最終目的是利用患者自己的幹細胞來製造替代器官,如皮膚、肝臟以及腎臟等。
(4)腫瘤發生機制的研究:已發現一種新的基因信號能阻止或允許幹細胞發展成特定的細胞類型。這可能導致新的幹細胞療法,有助於癌症的研究。
(5)延緩衰老方面的應用:潘基因家族既可決定細胞類型,又可控制分化。了解該基因的調控對延緩衰老、增長人類壽命可能意義重大。
綜上所述,ASCs及其衍生器官的臨床廣泛應用必將導致一次醫學革命,產生一次全新的治療技術。但應注意到,目前多數試驗結果來自動物體內實驗,許多是群體細胞研究,並未在克隆細胞水平得到證實。人ASCs的特性是否與動物一致,體外結果是否與體內結果一致尚不清楚。更重要的是ASCs的分化潛能到底有多大,分化的具體分子機制還不十分清楚。並且ASCs在臨床應用還存在體外分離、擴增、誘導及移植後增殖調控等技術問題。但是,這些基本問題的深入探索無疑會使ASCs在未來的細胞和組織工程應用中具有廣闊前景。可以預見,對幹細胞可塑性的逐步闡明將把我們帶入一個醫學新紀元。
參看
參考
郭虹趙春華.成體幹細胞及其可塑性的研究進展.《細胞生物學雜誌》 ISTIC -2003年3期
| 關於「成體幹細胞」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |