病理學/各種組織的再生過程
| 醫學電子書 >> 《病理學》 >> 損傷的修復 >> 再生 >> 各種組織的再生過程 |
| 病理學 |
|
|
(一)上皮組織的再生
1.被覆上皮再生 鱗狀上皮缺損時,由創緣或底部的基底層細胞分裂增生,向缺損中心遷移,先形成單層上皮,以後增生分化為鱗狀上皮。粘膜如胃腸粘膜上皮缺損後,同樣也由鄰近的基底部細胞分裂增生來修補,新生的上皮細胞起初為立方形,以後增高變為柱狀細胞。
2. 腺上皮再生腺上皮雖有較強的再生力,但再生的情況依損傷的狀態而異:如果僅有腺上皮的缺損而腺體的基底膜未被破壞,可由殘存細胞分裂補充,完全恢復原來腺 體結構。如腺體構造(包括基底膜)被完全破壞,則難以再生。構造比較簡單的腺體如子宮腺、腸腺等可從殘留部細胞再生。肝細胞有活躍的再生力,肝再生可分為 三種情況:①肝大部分切除後,剩餘的肝細胞分裂增生十分活躍,短期內就能使肝恢復原來的大小。例如大白鼠肝切除90%後,只需2周就可恢復原肝的重量,不 過以後要經過較長時間的結構改建,形成新的肝小葉,才能恢復原結構。②肝細胞壞死時,不認範圍大小,只要肝小葉網狀支架完整,從肝小葉周邊區再生的肝細胞 可沿支架延伸,恢復正常結構。③肝細胞壞死較廣泛,肝小葉網狀支架塌陷,網狀纖維轉化為膠原纖維(網狀纖維膠原化),或者由於肝細胞反覆壞死及炎症刺激, 纖維組織大量增生,形成肝小葉內間隔,此時再生肝細胞難以恢復原來小葉結構,成為結構紊亂的肝細胞團,例如肝硬變時的再生結節。
(二)纖維組織的再生
在 損傷的刺激下,受損處的纖維母細胞進行分裂、增生。纖維母細胞可由靜止狀態的纖維細胞轉變而來,或由未分化的間葉細胞分化而來。幼稚的纖維母細胞胞體大, 兩端常有突起,突起亦可呈星狀,胞漿略顯嗜鹼性。電鏡下,可見胞漿內有豐富的粗面內質網及核蛋白體,說明其合成蛋白的功能很活躍;胞核體積大,染色淡,有 1~2個核仁。當纖維母細胞停止分裂後,開始合成並分泌前膠原蛋白,在細胞周圍形成膠原纖維,細胞逐漸成熟,變成長梭形,胞漿越來越少,核越來越深染,成 為纖維細胞(圖2-1)。
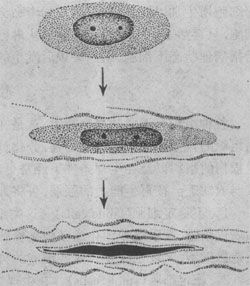
圖2-1 纖維母細胞產生膠原纖維並轉化為纖維細胞模式圖
軟骨組織再生起始於軟骨膜的增生,這些增生的幼稚細胞形似纖維母細胞,以後逐漸變為軟骨母細胞,並形成軟骨基質,細胞被埋在軟骨陷窩內而變為靜止的軟骨細胞。軟骨再生力弱,軟骨組織缺損較大時由纖維組織參與修補。
骨組織再生力強,骨折後可完全修復。
(四)血管的再生
1. 血管的再生 毛細血管多以生芽方式再生。首先在蛋白分解酶作用下基底膜分解,該處內皮細胞分裂增生形成突起的幼芽,隨著內皮細胞向前移動及後續細胞的增生而形成一條細 胞索,數小時後便可出現管腔,形成新生的毛細血管,進而彼此吻合構成毛細血管網(圖2-2)。增生的內皮細胞分化成熟時還分泌IV型膠原、層粘連蛋白和纖 維粘連蛋白,形成基底膜的基板。纖維母細胞分泌Ⅲ型膠原及基質,組成基底膜的網板,本身則成為周細胞(即血管外膜細胞)。至此毛細血管的結構逐告完成。新 生的毛細血管基底膜不完整,內皮細胞間空隙較多較大,故通透性較高。為適應功能的需要,這些毛細血管還會不斷改建:有的管壁增厚發展為小動脈、小靜脈,其 平滑肌等成分可能由血管外未分化間葉細胞分化而來。
2.大血管的修復 大血管離斷後需的手術吻合,吻合處兩側內皮細胞分裂增生,互相連接,恢復原來內膜結構。但離斷的肌層不易完全再生,而由結締組織增生連接,形成瘢痕修復。
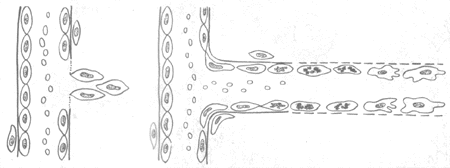
圖2-2 毛細血管再生模式圖
1.基底膜分解,內皮細胞肥大、增生,形成幼芽
2.內皮細胞向前移動,其後的內皮細胞分裂增生,靠近血管處的內皮細胞先分化成熟,並有新的基底膜形成
(五) 肌組織的再生
肌 組織的再生能力很弱。橫紋肌的再生依肌膜是否存在及肌纖維是否完全斷裂而有所不同。橫紋肌細胞是一個多核的長細胞,可長達4cm ,核可多達數十乃至數百個,損傷不太重而肌膜未被破壞時,肌原纖維僅部分發生壞死,此時中性粒細胞及巨噬細胞進入該部吞噬清除壞死物質,殘存部分肌細胞分 裂,產生肌漿,分化出肌原纖維,從而恢復正常橫紋肌的結構;如果肌纖維完全斷開,斷端肌漿增多,也可有肌原纖維的新生,使斷端膨大如花蕾樣。但這時肌纖維 斷端不能直接連接,而靠纖維瘢痕癒合。癒合後的肌纖維仍可以收縮,加強鍛煉後可以恢復功能;如果整個肌纖維(包括肌膜)均破壞,則難以再生,而通過瘢痕修 復。
平滑肌也有一定的分裂再生能力,前面已提到小動脈的再生中就有平滑肌的再生,但是斷開的腸管或是較大血管經手術吻合後,斷處的平滑肌主要通過纖維瘢痕連接。
心肌再生能力極弱,破壞後一般都是瘢痕修復。
(六)神經組織的再生
腦 及脊髓內的神經細胞破壞後不能再生,由神經膠質細胞及其纖維修補,形成膠質瘢痕。外周神經受損時,如果與其相連的神經細胞仍然存活,則可完全再生。首先, 斷處遠側段的神經纖維髓鞘及軸突崩解,並被吸收;近側段的數個Ranvier節神經纖維也發生同樣變化。然後由兩端的神經鞘細胞增生,形成帶狀的合體細 胞,將斷端連接。近端軸突以每天約1mm的速度逐漸向遠端生長,穿過神經鞘細胞帶,最後達到末梢鞘細胞,鞘細胞產生髓磷脂將軸索包繞形成髓鞘(圖 2-3)。此再生過程常需數月以上才能完成。若斷離的兩端相隔太遠(超過2.5cm時),或者兩端之間有瘢痕或其它組織阻隔,或者因截肢失去遠端,再生軸 突均不能達到遠端,而與增生的結締組織混合在一起,捲曲成團,成為創傷性神經瘤(截肢神經瘤),可發生頑固性疼痛。為防止上述情況發生,臨床常施行神經吻 合術或對截肢神經斷端作適當處理。
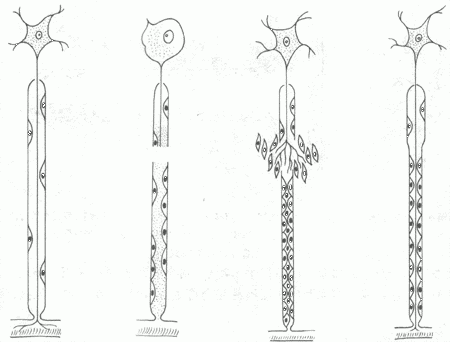
圖2-3 神經纖維再生模式圖
①正常神經纖維 ②神經纖維斷離,遠端及近端的一部分髓鞘及軸突崩解③神經膜細胞增生,軸突生長 ④神經軸突達末梢,多餘部分消失
| 關於「病理學/各種組織的再生過程」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |