醫用化學/硫醇和硫醚
| 醫學電子書 >> 《醫用化學》 >> 原子結構和分子結構 >> 硫醇和硫醚 |
| 醫用化學 |
|
|
硫在周期表內與氧同屬第六主族,最外層未成對的p電子也是兩個,因此硫也能形成與氧相類似的化合物。
R-OH 醇R-O-R 『醚
R-SH硫醇R-S-R『 硫醚
一、硫醇的構造和性質
硫醇可看作是硫化氫(H2S)分子中一個氫被烴基取代的化合物,通式為R-SH。-SH稱為巰基或氫硫基,它是硫醇的官能團。簡單的硫醇有甲硫醇CH3SH、乙硫醇CH3CH2SH等。巰基也存在於某些結構複雜的化合物中,例如與人體代謝有關的輔酶A分子中就含有巰基。
低級的硫醇具有極難聞的臭味,沸點比對應的醇為低,微溶於水。高級的硫醇的臭味隨相對分子質量的增大而逐漸減少,沸點則與相應的醇相近,難溶於水面易溶於有機溶劑中。
硫醇的化學性質與醇有相似的方面,也有不同的地方,如硫醇也可與酸成酯,但硫醇的酸性卻比相應的醇強(例如乙硫醇的pKa為9.5,就比乙醇的pKa=17小得多)。因此硫醇可與氫氧化鈉作用,也能與某些金屬特別是重金屬的氧化物作用,生成相應的硫醇鹽。由重金屬形成硫醇鹽後大減低了重金屬的毒性,因此臨床上常用某些含有巰基的化合物作重金屬中毒時的解毒劑。例如:
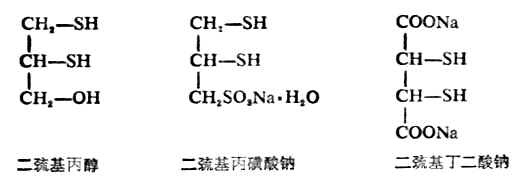
它們均含有兩個相鄰的巰基,能與砷、汞、銻等金屬作用生成穩定無毒的環狀化合物。例如:
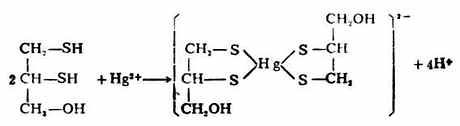
反應產物可由尿排出,從而使金屬不再損害體內酶系統的活性,起到解毒作用。
二巰式丙醇,最早是路易斯氣(一種含砷的毒氣CLCH=CHAsCL2)中毒的解毒劑,因毒性較大,已逐漸被其他解毒劑所代替,如二巰基丁二酸鈉就是由我國創製的一個毒性較低、效力更強的新解毒劑。
硫醇另一個與醇不同的性質是,它容易被氧化生成二硫化物。
![]()
二硫化物
二硫化合物中的「-S-S-」鍵稱二硫鍵,許多蛋白質的結構中存在這種鍵。當二硫化物還原時,二硫鍵斷裂重新恢復原來的巰基。
二、硫醚的構造和性質
硫醚可看作是硫化氫分子中的兩個氫原子都被烴基取代的化合物,通式為R-S-R。例如二甲硫醚CH3-S-CH3、甲乙硫醚CH3-S-C2H5等。
硫醚的物理性質與硫醇相似,但臭味不如硫醇那樣強烈。硫醚易被氧化,而使硫的化合價從二價變為四價或六價,即硫醚第一步可氧化成亞碸,亞碸又可進一步氧化成碸。
芥子氣(β,β『-二氯二乙硫醚)是硫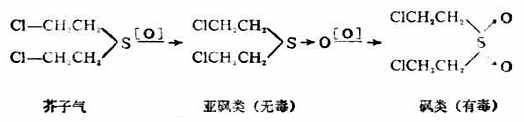 醚的衍生物,是持久性的糜爛性毒劑,對皮膚有腐蝕作用,沾在皮膚上引起難以痊癒的潰瘍。它的蒸氣能透過衣服,對人類的粘膜組織及呼吸器官都有損害作用。
醚的衍生物,是持久性的糜爛性毒劑,對皮膚有腐蝕作用,沾在皮膚上引起難以痊癒的潰瘍。它的蒸氣能透過衣服,對人類的粘膜組織及呼吸器官都有損害作用。
芥子氣是無色油狀液體,沸點217℃,熔點14℃。具有芥末的氣味,不溶於水,易溶於乙醇、苯等有機溶劑。
漂白粉能與芥子氣起氧化、氯代反應,將芥子氣變為毒性較小的亞碸等產物。
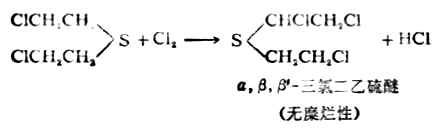
| 關於「醫用化學/硫醇和硫醚」的留言: | |
|
標題應改為 硫醇與硫醚 請問本節的編輯,本書的編者是誰,有問題需要請教編者.
| |
| 添加留言 | |