醫用化學/烷烴
| 醫學電子書 >> 《醫用化學》 >> 鏈烴 >> 烷烴 |
| 醫用化學 |
|
|
目錄 |
一、烷烴的構造
烷烴的構造特點是其中的碳原子與碳原子都以單鍵相結合,其餘價鍵都和氫原子相連接,含有一個、兩個和三個碳原子的烷烴構造如下;
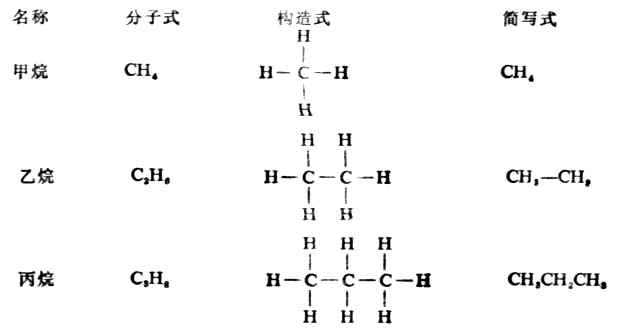
其它烷烴的構造與乙烷、丙烷相似。除甲烷外,烷烴分子中的各個碳原子上所連的四個原子或原子團不盡相同,所以其鍵角稍有變化,但仍接近於109°28′,因為這樣的空間排布,能量最低,體系最穩定。這些分子中碳原子與碳原子連結成鏈狀,其分子的形狀是一系列共享一個頂點的四面體。如乙烷(圖11-1)
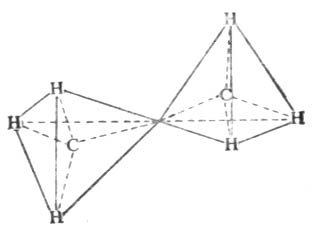
圖11-1 乙烷的鏈狀結構
二、烷烴的同系列和通式
根據烷烴的構造特點和它的原子組成可知,最簡單的烷烴是含有一個碳原子的甲烷CH4,其次是含有兩個碳的乙烷C2H6。按烷烴分子中碳與氫原子數可排列如表11-1。
表11-1 烷烴的同系列
| 碳原子數 | 分子式 | 同系列差 |
| 1 | CH4 | CH2 |
| 2 | C2H6 | |
| 3 | C3H8 | CH2 |
| 4 | C4H10 | CH2 |
| 5 | C5H12 | CH2 |
| … | … | |
| n-1 | CnH2(n-1)+2 | CH2 |
| n | CnH2(n+2) |
從表11-1可見,任何相鄰的兩個烷烴在分子組成上都相差CH2,這叫做同系列差。這樣的一系列化合物叫做同系列。同系列中的化合物互稱同系物。同系列在有機化學中的重要性在於同系物具有相似的化學性質,其物理性質一般隨碳原子數目的增減表現出有規律的變化,對學習及研究有機化合物帶來了很大方便。但是,如果碳原子數目相差過多,其性質也會表現出較大的差異。因此,在運用同系物的概念時,既要考慮到它們的共性,也要注意其個性。
從同系列中可以看出,烷烴分子中的碳和氫原子數間有一定的關係。如果碳原子數為n,則氫原子數即為2n+2。因此,烷烴的分子組成通式是CnH2n+2。
三、烷烴的同分異構現象和構象
(一)碳鏈異構
一種物質只能有一種特定的構造。因此,要了解有機物的特性和反應,常常要研究它們的構造。在研究烷烴的同系列時,發現隨著碳原子數的逐漸增加,會出現同分異構現象。例如:分子式為C4H10的烷烴,碳原子的連結方式有兩種可能,其構造式分別為:
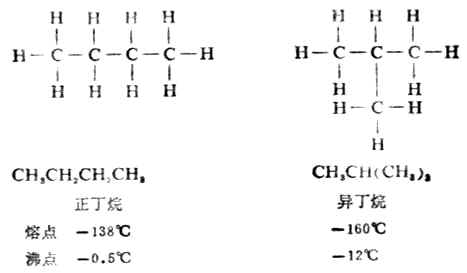
分子式為C5H12的烷烴,碳原子的連結方式則有三種可能,其構造式分別為:
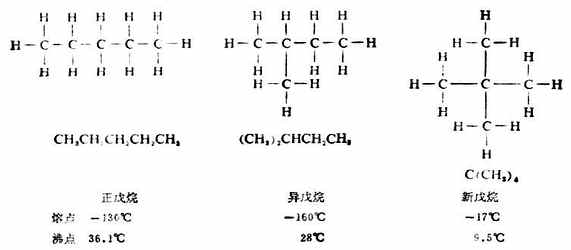
像這樣具有相同的分子式,而有不同的構造的化合物互稱同分異構體,簡稱異構體。若分子式相同,由於碳鏈構造的不同而產生的異構體叫做碳鏈異構體,例如,正丁烷和異丁烷;正戊烷、異戊烷和新戊烷。這種異構現象由於組成分子的原子或原子團連結次序不同引起的,所以屬於構造異構。隨著分子中碳原子數目的增加,同分異構體的數目會很快地增加,如表11-2。
表11-2 隨著碳原子的增加異構體數目增長的情形
| 碳原子數 | 分子式 | 異構體數目 | |
| 1 | CH4 | ||
| 2 | C2H6 | ||
| 3 | C3H8 | ||
| 4 | C4H10 | 2 | |
| 5 | C5H12 | 3 | |
| 6 | C6H14 | 5 | |
| 7 | C7H16 | 9 | |
| 8 | C8H18 | 18 | |
| 9 | C9H20 | 35 | |
| 10 | C10H22 | 75 | |
| 15 | C15H32 | 4 347 | |
| 20 | C20H42 | 366 319 | |
| 40 | C40H82 | 62 491 178 805 831 | |
烷烴中碳鏈構造的不同主要是由碳原子之間的結合方式的不同引起的。在烷烴中碳原子與碳原子之間可能有四種結合方式,因此把碳原子分為伯(以1°表示)、仲(2°)、叔(3°)、季(4°)四類。 .
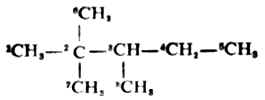
只與另外一個碳原子直接相連的碳原子,如上式中的C-1,5,6,7,8叫做伯碳原子;若碳原子與另外兩個碳直接相連如-4,叫做仲碳原子;與另外三個碳原子直接相連的碳如C-3叫做叔碳原子;與另外四個碳原子直接相連的碳如C-2叫做季碳原子。
連在伯、仲和叔碳原子上的氫,分另稱為伯、仲和叔氫原子。不同類型的氫原子的反應性不同。
(二)構象
有機物的分子中,以單鍵(σ鍵)相連結的兩個碳原子,通過沿C-C單鍵的旋轉,可使這兩個碳原子上的原子或原子團在空間有不同的排布方式。每一種排布方式,都是有機物分子在空間的一種構象。具有一定構型的分子,僅由於圍繞單鍵旋轉,使分子中各原子在空間有不同的排布,稱為構象。
1.乙烷的構象
乙烷是含有碳碳單鍵的最簡單的化合物。當兩個碳原子圍繞C-C鍵旋轉時,兩個碳原子上的兩組原子之間可以相對處於不同的位置,出現無數的空間排布方式,每一種空間排布方式就是一種構象。
不同的構象可用透視式或紐曼投影式表示。(Ⅰ)和(Ⅱ)是乙烷的兩種典型構象。
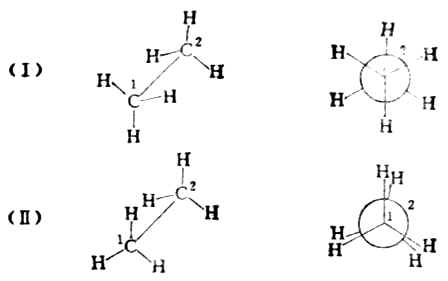
紐曼投影式中,離觀察者較遠的碳原子用圓圈表示,它的三個C-H鍵用圓圈上的實線表示;離觀察者較近的碳原子用圓心的點表示,它的三個C-H鍵則用與圓心相連的三條實線表示。
(Ⅰ)式中兩組氫原子處於交叉的位置,這種構象叫做交叉式。式中兩組氫原子彼此相距最遠,相互斥力最小,能量最低,因而穩定性最大。這種構象是優勢構象。(Ⅱ)式中,兩組氫原子兩兩相對重疊,這種構象叫重疊式。在重疊式構象中,非鍵合氫原子間距離最近,排斥作用最大,這種構象具有較高的內能,是一種不穩定的構象。在室溫時,乙烷分子是交叉式、重疊式以及介於它們兩者之間的許多構象的平衡混合物,不易分離。
2.正丁烷的構象
正丁烷![]()
的構象要比乙烷複雜。當圍繞正丁烷的C(2)-C
(3)鍵旋轉時,可以有全重疊式,鄰位交叉式、部分重疊式和對位交叉式等不同的典型構象。它們的透視式和紐曼投影工表示如下;
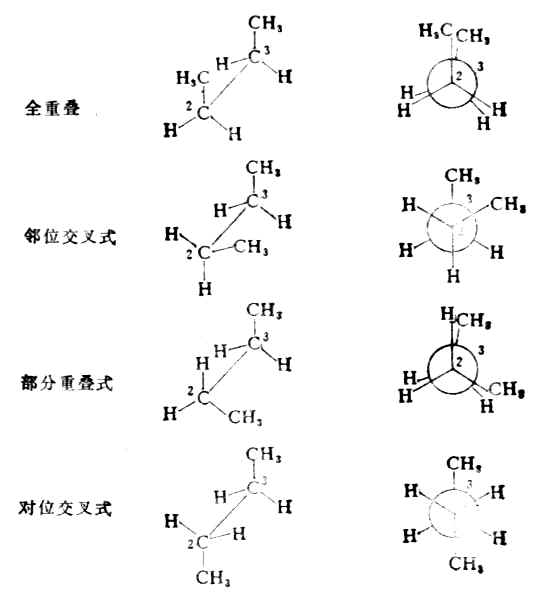
透視式 紐曼投影式
在正丁烷的構象中,對位交叉式的兩個甲基相距最遠,相互作用最弱,內能最低,是最穩定的現象。鄰位交叉式的兩個甲基相距較近些,所以穩定性稍差。部分重疊式的甲基和氫原子十分靠近,相互作用大,穩定性較鄰位交叉式差。而在全重疊式中,由於兩個甲基處於十分靠近的地位,相互作用最大,穩定性最差。因此這幾種構象的內能高低次序為:全重疊式>部分重疊式>鄰位交叉式>對位交叉式。
可見,正丁烷在一般情況下,對位交叉式是佔優勢的構象。
在鏈狀化合物中,優勢構象都是類似於正丁烷對位交叉式的構象。應該注意,分子主要以其優勢構象存在,並不意味著其它的構象不存在,而是所佔比例較小而已。
四、烷烴的命名
有機化合物的種類繁多,數目龐大,又有許多異構體。所以必須有一個合理的命名法,以便於識別。有機化合物的正確的名稱不僅應表示分子的組成,而且要準確、簡便地反映出分子的構造。因此命名法是有機化學的重要內容之一。烷烴的常用命名法有普通命名法和系統命名法。
(一)普通命名法
1.直鏈烷烴的命名
直鏈烷烴按碳原子數叫「正某烷」。十個及十個碳原子以下的烷烴分別用天干(甲、乙、丙、丁、戊、己、庚、辛、壬、癸)表示。例如,CH4四烷,C2H6乙烷,C3H8丙烷……C10H22癸烷。對含有十個碳原子以上的烷烴用漢語數字命名。例如,C11H24十一烷,C12H26十二烷,C20H42二十烷等。
2.含側鏈烷烴的命名
![]()
且無其它支鏈的烷烴,則按碳原子總數叫做異某烷。例如,
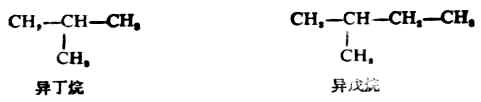
(二)系統命名法
對構造比較複雜的化合物的命名可採用系統命名法。系統命名法可用於各種化合物的命名。
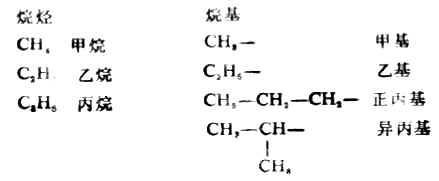
1.烷基
烴分子中去掉一個氫原子所剩下的原子團叫烴基。脂肪烴去掉一個氫原子所剩下的原子團叫做脂肪烴基,通常用R表示。烷烴的基叫做烷基,它的通式CnH2n+1烷基的命名根據烷烴而定。多於兩個碳原子的烷烴,有可能衍生出多個不同的烷基。例如:
2.系統命名法
我國現用的系統命名法是根據IUPAC(International Union of Pure and Applied Chemistry)規定的原則,再結合我國漢語文字的特點而制定的。烷烴的系統命名法的主要之點是如何確定主鏈和處理取代基的位置。
(1)選擇最長的連續的碳鏈為主鏈作為母體,叫某烷。較短的鏈為支鏈,作為取代基。
(2) 從靠近支鏈的一端開始,把母體烷烴的各個碳原子依次編號,以確定取代基的位次。取代基的位次號與名稱之間用一短線相連,寫在母體名稱之前。例如:
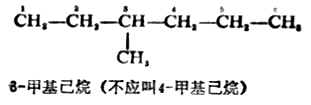
(3)主鏈上連接幾個不同的取代基時,則按「次序規則」(見本章第二節)將取代基的大小順序列出,小者在前,「較優」者在後。
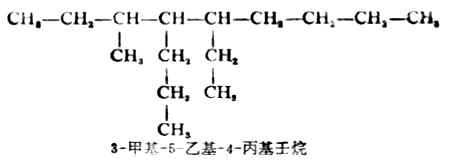
(4)若在主鏈上連有相同的取代基,則將取代基合併,用二、三……數字表示取代基的數目,寫在取代基前面,各取代基的位次號仍須標出。例如:
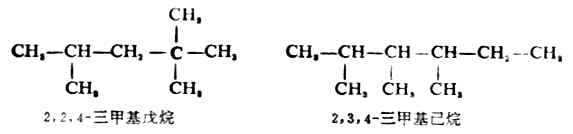
(5)若同時可能有幾個等長的主鏈時,要選擇含取代基最多的碳鏈為主鏈。例如:
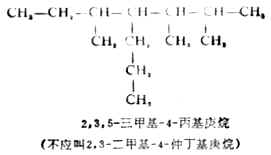
(6)若在主鏈的等距離兩端同時遇到取代基且多於兩個時,則要比較第二個取代基的位次大小,以取代基位次的代數和最小為原則。例如:
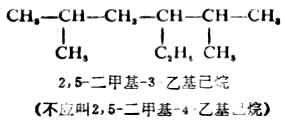
五、烷烴的物理性質
在有機化學中,物理性質通常是指化合物的聚集狀態、氣味、熔點(mp)、沸點(bp)、密度(ρ)、折射率(nΧD)、溶解度以及波譜數據等。
在室溫和常壓下,直鏈烷烴中從甲烷到丁烷都是氣體;含5-15個碳原子的烷烴是液體;16及16個碳原子以上的是固體。不僅物態隨著正烷烴同系物相對分子質量的增加而有明顯的改變,其它一些物理性質如熔點、沸點、密度、折射率也呈現出規律性的變化。
從表11-3可以看出,正烷烴的熔點(前三個除外)和沸點基本上都是隨著碳鏈的增長而變大。這是一個「量的變化會引起質的變化」的例證。
表11-3 正烷烴的物理常數
| 名稱 | 熔點 | 沸點/℃ | 相對密度 | 折射率(n20D) |
| 甲烷 | -183 | -164 | 0.4661 | - |
| 乙烷 | -183 | -89 | 0.5462 | - |
| 丙烷 | -187 | -42 | 0.5853 | - |
| 正丁烷 | -138 | -0.5 | 0.5788 | - |
| 正戊烷 | -130 | 36 | 0.6262 | 1.3575 |
| 正己烷 | -95 | 69 | 0.6603 | 1.3751 |
| 正庚烷 | -91 | 98 | 0.6838 | 1.3878 |
| 正辛烷 | -57 | 126 | 0.7025 | 1.3974 |
| 正壬烷 | -51 | 151 | 0.7179 | 1.4054 |
| 正癸烷 | -30 | 174 | 0.7300 | 1.4102 |
| 正十一烷 | -26 | 196 | 0.7402 | 1.4172 |
| 正十二烷 | -10 | 216 | 0.7487 | 1.4216 |
| 正十三烷 | -6 | 235 | 0.7564 | 1.4256 |
| 正十四烷 | 6 | 254 | 0.7628 | 1.4290 |
| 正十五烷 | 10 | 271 | 0.7685 | 1.4315 |
| 正十六烷 | 18 | 287 | 0.7733 | 1.4345 |
| 正十七烷 | 22 | 302 | 0.7780 | (1.4369) |
| 正十八烷 | 28 | 316 | 0.7768 | (1.1390) |
| 正十九烷 | 32 | 330 | 0.7855 | (1.4529) |
烷烴的熔點變化沒有沸點那樣有規律,通常是隨著分子的對稱性增大而升高。分子越對稱,它們在晶體中的排列越緊密,熔點就高。例如,正戊烷、異戊烷、新戊烷的熔點分別為-130℃、-160℃、-17℃。新戊烷的熔點最高。
烷烴的相對密度都小於1,且隨著相對分子質量的變大而有所增加,最後接近於0.80左右。這也是由於分子間的作用力隨著相對分子質量的增加而加大,使分子間的距離相對地減小,密度增大。
烷烴都不溶於水,但能溶於苯、氯仿、四氯化碳等有機溶劑。它們的溶解度隨著相對分子質量的增加而減小。
六、烷烴的化學性質
烷烴的分子中沒有官能團。除甲烷只有C-Hσ鍵外,所有烷烴分子中僅含C-C及C-Hσ鍵。
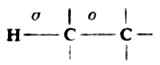
由於烷烴分子中的C-C鍵和C-H鍵都很強,需要較高的能量才能使之斷裂(如斷裂C-Cσ鍵需347.3kJ.mol-1,斷裂C-Hσ鍵需380.7-435.1kJ.mol-1),所以一般情況下,烷烴具有極大的化學穩定性,與強酸、強鹼及常用的氧化劑、還原劑都不發生化學反應。另外,碳原子和氫原子的電負性差別很小,分子中σ鍵的極性很弱,很難被極化,故烷烴的分子也不易和極性試劑發生共價鍵異裂的離子型反應。但是,在一定的條件下,例如使用高溫、高壓或催化劑,烷烴也能發生一些化學反應。
(一)鹵化反應
烷烴和氯在黑暗中幾乎不起反應。但是在日光照射、高溫或催化劑的影響下它們能發生劇烈的反應,生成氯化氫和氯代烷烴。例如甲烷和氯氣在強烈的日光或紫外光照射下反應猛烈,甚至發生爆炸。
![]()
在漫射的日光下則起一般的氯化反應,生成一氯甲烷、二氯甲烷、三氯甲烷(俗稱氯仿)和四氯化碳。

烷烴的氯化過程是逐步的。每一步被取代出來的氫原子與另一個氯原子化合成為氯化氫。
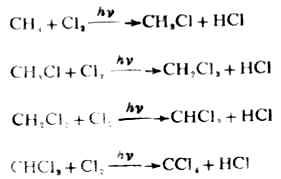
較高相對分子質量的烷烴氯化時,常生成複雜的混合物。
(二)氧化反應
烷烴在通常情況下是不被氧化的。但是它能在空氣中燃燒(劇烈氧化)生成二氧化碳和水,同時放出大量的熱能。因此烷烴可以用作燃料。
C2H6+3*1/2*O2→2CO2+3H2O △H=-1426kJ.mol-1
C6H14+9*1/2*O2→6CO2+7H2O △H=-4141kJ.mol-1
一些氣態烴或極細微粒的液態烴與空氣在一定比例範圍內混合,點燃時會發生爆炸。煤礦井的瓦斯爆炸就是甲烷與空氣混合物(體積比約為1:10左右)燃燒時造成的。
七、烷烴氯化的反應歷程
化學反應歷程是說明一個化學反應所經歷的過程,也就是對每一個化學反應的各個中間步驟的詳細描述。
已知烷烴的氯化反應是一種自由基反應。反應過程中,反應物的共價鍵發生均裂,生成自由基。一般地說自由基很不穩定,極易與其它化合物的分子發生反應,使自己變成穩定的分子,又使其它化合物的分子變為自由基,從而引起一連串反應(鏈反應)。例如,氯分子在光照下,均裂為氯自由基。
![]()
反應由此開始,所以這個步驟叫做鏈的引發。氯自由基很活潑,它奪取甲烷分子中的氫結合為氯化氫,產生甲基自由基。
Cl.+CH4→CHl+CH3.
CH3.和CL2反應,奪得一個氯原子,生成穩定的CH3CL,同時又有一個的CL.產生。
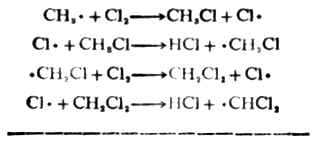
這個過程叫做鏈的增長。反應過程表明,只要在開始時有少量的氯原子(自由基),反應即會繼續傳遞下去。
最後由於自由基相互結合形成穩定的化合物,反應便終止。如:
Cl.+Cl.→Cl2
CH3.+Cl.→CH2Cl CH3.+CH3.→CH3-CH3
上述過程叫做鏈的終止。
八、幾種常用的烷烴混合物
常用的烷烴混合物,除了汽油、煤油和柴油外,還有以下幾種產品。
(一)石油醚
石油醚是低級烷烴的混合物。沸點範圍在30-60℃的是戊烷和己烷的混合物;沸點範圍在90-120℃的是庚烷和辛烷的混合物。它們主要被用作有機溶劑。石油醚極易燃燒並具有毒性,使用及貯存時要特別注意安全。
(二)液體石蠟
液體石蠟主要成分是18-24個碳原子的液體烷烴的混合物,是呈透明液體。它不溶於水和醇,能溶於醚和氯仿中。液體石蠟性質穩定。精製的液體石蠟在醫藥上常用作腸道潤滑的緩瀉劑。
(三)凡士林
凡士林是液體石蠟和固體石蠟的混合物,呈軟膏狀半固體,不溶於水,溶於醚和石油醚。因為它不能被皮膚吸收,而且化學性質穩定,不易和軟膏中的藥物起變化,所以在醫藥上常用作軟膏基質。
(四)石蠟
石蠟是C25-C34固體烴的混合物,醫藥上用作蠟療、藥丸包衣、封瓶、理療等。
| 關於「醫用化學/烷烴」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |