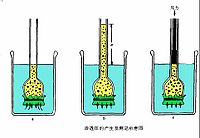
滲透壓
| A+醫學百科 >> 滲透壓 |
將溶液和水置於U型管中,在U型管中間安置一個半透膜,以隔開水和溶液,可以見到水通過半透膜往溶液一端跑,假設在溶液端施加壓強,而此壓強可剛好阻止水的滲透,則稱此壓強為滲透壓,滲透壓的大小和溶液的重量摩爾濃度、溶液溫度和溶質解離度相關,因此有時若得之滲透壓的大小和其他條件,可以反推出溶質分子的分子量。
定性理解:
溶液濃度越大,滲透壓越大
滲透壓:水分子經半透膜進入蔗糖溶液,而溶質(這是蔗糖)不會透過半透膜。單位體積清水中的水分子比單位體積蔗糖溶液中的水分子多,所以在單位時間內水分子由燒杯透過半透膜進入漏斗內的數量多於水分子由漏斗進入燒杯中的數量。水分子總是從水多的地方到水少的地方,即從濃度低的溶液到濃度高的溶液。因此產生靜水壓力,如果在溶液的上方施加一個壓力,其大小恰好阻止水分子的淨滲入,這個壓力產生的壓強數值就是該溶液在該濃度下的滲透壓(osmotic pressure),用符號π表示,單位:atm。
π的大小可用滲透計測定,或用滲透平衡時高出水面的溶液對下部產生的靜水壓力表示(h×s × 比重=體積× 比重)。也可用Vant Hoff提出的公式計算:
π = icRT或π=n/VRT
c=溶液的摩爾濃度;i = 等滲係數
π是溶液的滲透壓(kPa),V是溶液的體積(dm3),n是溶質的物質的量,R是摩爾氣體常數。
②滲透壓 osmotic pressure
隔以半透膜,一方為溶媒的水,另一方為溶液,水通過半透膜向溶液一方滲透。為阻止水的移動在溶液側所加的壓力稱為滲透壓。水的運動之所以停止,是該壓力與通過膜的水的化學勢能相等所致。重量克分子濃度Cs的溶液滲透壓П,近似於П=CsRT(R:氣體常數,T:絕對溫度)。如用容積克分子濃度,能得到比理論值更大的實測值。液胞很發達的植物細胞,與細胞體積V之間存在著ПV=定值的關係;但在動物等細胞質多的細胞,從V中減去滲透不活性部分(非水相)的細胞容積時,上式也成立。在植物細胞,細胞質和細胞液保持滲透壓平衡。細胞液的滲透壓限定細胞質的含水量,而影響細胞質粘性等物理化學性質。此外滲透壓還能使之產生膨脹壓以調節細胞的生長和膨脹運動。細胞具有調節滲透壓的作用,此稱滲透壓調節(osmoregulation)。就如動物體液那樣,浸漬組織的內環境的滲透壓,也具有很大的生理影響。滲透壓可以用氣壓、冰點下降度(△)或者滲透克分子濃度等來表示。
細胞外液的理化性質——滲透壓:
所謂溶液滲透壓,簡單的說,是指溶液中溶質微粒對水的吸引力。溶液滲透壓的大小取決於單位體積溶液中溶質微粒的數目:溶質微粒越多,即溶液濃度越高,對水的吸引力越大,溶液滲透壓越高;反過來,溶質微粒越少,即與無機鹽、蛋白質的含量有關。在組成細胞外液的各種無機鹽離子中,含量上佔有明顯優勢的是Na+和Cl-,細胞外液滲透壓的90%以上來源於Na+和Cl-。在37℃時,人的血漿滲透壓約為770kPa,相當於細胞內液的滲透壓。
|
|||||||||||||||||||||
| 關於「滲透壓」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |