臨床生物化學/固定時間法(取樣法)
| 醫學電子書 >> 《臨床生物化學》 >> 血清酶定量的檢測技術 >> 測定酶活性濃度的兩大類方法 >> 固定時間法(取樣法) |
| 臨床生物化學 |
|
|
前面已經提到,早期臨床實驗室測酶活性時常使用比色法,先讓酶與底物在一定溫度下作用一段固定的時間,然後停止酶反應,加入試劑進行化學反應呈色測出底物和產物的變化。由於比色法靈敏度較低,或由於手工操作不易控制好,常定在30分鐘左右。歷史上這類方法常被命名為「終點法」、「二點法」、「固定時間法」和「取樣法」。大多數文獻使用「固定時間法」。此命名指出了用這類方法測酶活性濃度,必須保證酶和底物在所選定的溫度下作用時間要很精確,否則將引起較大誤差。但「取樣法」的命名更具有特徵性。因它指出此類方法和下面將提到的另一類連續監測法相比較,最基本一點的是此類方法停止反應後才測底物或物的變化。很難進行連續監測,而另一類方法則不需停止酶反應,就可測定反應物的變化,很容易觀察到反應的整個過程。後一類方法開始於50年代,Warburg首先用分光光度計。在340nm處直接監測到反應物NADH的動態變化過程。由於不停止酶反應,不需添加其它呈色試劑。測定方法簡單,結果準確,逐步取代了「取樣法」成為目前測酶活性的主要方法。
由於經歷了一個發展過程,命名比較混亂而且大部分不甚確切,IFCC建議命名為「連續監測法」,不用目前廣為流行的「動態法」術語。其原因是目前測酶活性濃度方法都是基於化學反應。圖17-6是一個典型的化學反應過程。
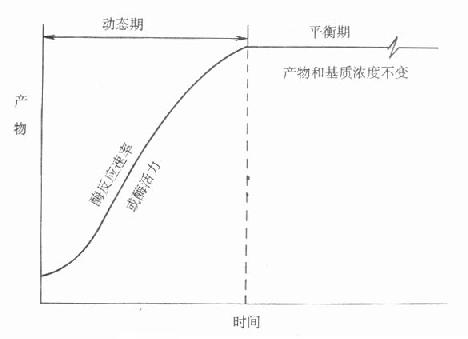
圖17-6 動態和平衡概念的示意圖
可以看出整個反應過程,可以大致分為二個時期。一開始為動態期,化學反應按一定速度進行,反應物濃度隨時間而變化,且變化程度不斷變小,到一定時間。化學反應或者達到平衡,或者反應達到終點,此時反應速度為零,反應物濃度不變。最近IFCC文件按所用方法所測定的反應是在達到平衡前還是平衡後。分別命名為動態法或平衡法。一般文獻往往將後一類方法稱為終點法。
出自A+醫學百科 「臨床生物化學/固定時間法(取樣法)」條目 http://cht.a-hospital.com/w/%E4%B8%B4%E5%BA%8A%E7%94%9F%E7%89%A9%E5%8C%96%E5%AD%A6/%E5%9B%BA%E5%AE%9A%E6%97%B6%E9%97%B4%E6%B3%95%EF%BC%88%E5%8F%96%E6%A0%B7%E6%B3%95%EF%BC%89 轉載請保留此連結
| 關於「臨床生物化學/固定時間法(取樣法)」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |