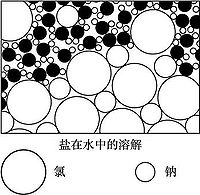
溶解
| A+醫學百科 >> 溶解 |
漢語拼音:
róng jiě
英語術語:Dissolve
廣義上說,超過兩種以上物質混合而成為一個分子狀態的均勻相的過程稱為溶解.而狹義的溶解指的是一種液體對於固體/液體/或氣體產生化學反應使其成為分子狀態的均勻相的過程稱為溶解.
一種物質(溶質)分散於另一種物質(溶劑)中成為溶液的過程。如食鹽或蔗糖溶解於水而成水溶液。溶液並不一定為液體,可以是固體、液體、氣體。比如均勻的合金和空氣都可以稱為溶液。
當兩種物質互溶時,一般把質量大的物質稱為溶劑(如有水在其中,一般習慣將水稱為溶劑)溶液中的
溶質體子小於1奈米,無丁達爾現象。
物質溶解於水,通常經過兩個過程:一種是溶質分子(或離子)的擴散過程,這種過程為物理過程,需要吸收熱量;另一種是溶質分子(或離子)和溶劑(水)分子作用,形成溶劑(水合)分子(或水合離子)的過程,這種過程是化學過程,放出熱量。當放出的熱量大於吸收的熱量時,溶液溫度就會升高,如濃硫酸、氫氧化鈉等;當放出的熱量小於吸收的熱量時,溶液溫度就會降低,如硝酸銨等;當放出的熱量等於吸收的熱量時,溶液溫度不變,如鹽、蔗糖。
一些溶質溶解後,會改變原有溶劑的性質,如氯化鈉溶解在水中,電離為自由移動的鈉離子與氯離子,故形成的溶液具有導電性(純水不導電);乙二醇溶解在水中,可降低水的凝固點。
目錄 |
物質的溶解性
定義表述
達到(化學)平衡的溶液便不能容納更多的溶質(當然,其他溶質仍能溶解),我們稱之為飽和溶液。在特殊條件下,溶液中溶解的溶質會比正常情況多,這時它便成為過飽和溶液。每份(通常是每份質量)溶劑(有時可能是溶液)所能溶解的溶質的最大值就是「溶質在這種溶劑的溶解度」。如果不指明溶劑,通常意味著溶劑為水,比如「氯化鈉的溶解度」和「氯化鈉在水中的溶解度」可以認為是具有同樣的意思。溶解度並不是一個恆定的值。一種溶質在溶劑中的溶解度由它們的分子間作用力、溫度、溶解過程中所伴隨的熵的變化以及其他物質的存在及多少所決定的,有時還與氣壓或氣體溶質的分壓有關。因此,一種物質的溶解度最好能夠表述成:「在某溫度,某氣壓下,某物質在某物質中的溶解度為xxxx。」,如無指明,則溫度及氣壓通常指的是標準狀況(STP)
分類
溶劑通常分為兩大類:極性溶劑、非極性溶劑。溶劑種類與物質溶解性的關係可以被概括為:「溶其所似」。意思是說,極性溶劑能夠溶解離子化合物以及能離解的共價化合物,而非極性溶劑則只能夠溶解非極性的共價化合物。比如,食鹽,是一種離子化合物,它能在水中溶解,卻不能在乙醇中溶解。
在有機化學中一般會用到的溶劑有丙酮、乙醇、水和苯。
水以及非極性溶劑是不能互溶的;如果你非要這麼做,它們也不會形成均一的混合物,最終會分離為兩層,又或者是形成看起來像牛奶一樣的乳濁液。
應用
溶解性
①是指物質在溶劑里溶解能力的大小。
②溶解性是物理性質,溶解是物理變化。
③溶解性是由20℃時某物質的溶解度決定的。(固體)
難溶(不溶) 微溶 可溶 易溶
(20℃) <0.01g 0.01~1g 1 g~10g >10g
④利用溶解性可有以下應用:
a、判斷氣體收集方法
可溶(易溶)於水的氣體不能用排水取氣法
如:CO2而H2,O2溶解性不好,可用排水取氣法。
b、判斷混合物分離方法
兩種物質在水中溶解性明顯不同時,可用過濾法分離。
如:KNO3(易溶)與CaCO3(難溶)可用過濾法分離;
而C與MnO2二者均不溶NaClKNO3均易溶,都不能用過濾法分離。
溶解度演算法:溶質質量/溶劑質量(通常為水)
單位: g/100g水
溶解度
1、固體物質的溶解度是指在一定的溫度下,某物質在100克溶劑里達到飽和狀態時所溶解的克數,用字母s表示,其單位是「g/100g水」。在未註明的情況下,通常溶解度指的是物質在水裡的溶解度。
2、氣體的溶解度通常指的是該氣體(其壓強為1標準大氣壓)在一定溫度時溶解在1體積水裡的體積數。也常用「g/100g水」作單位(自然也可用體積)。
3、溶解度是指在一定的溫度下,某物質在100克溶劑(通常是水)里達到飽和狀態時所溶解的克數.
4、特別注意:溶解度的單位是克(或者是克/100克水)而不是沒有單位
常見沉澱
白色:BaSO4 BaCO3 CaCO3 AgCl Ag2CO3 Mg(OH)2
黃色:AgI
淺黃色:AgBr
藍色:Cu(OH)2
紅褐色:Fe(OH)3
相關詞條:溶解度、熔解熱、溶液、溶解氧
| 關於「溶解」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |