醫用化學/溶膠的性質
| 醫學電子書 >> 《醫用化學》 >> 膠體溶液 >> 溶膠 >> 溶膠的性質 |
| 醫用化學 |
|
|
當光波投射到粒子上時,如果粒子大于波長,則光波以一定的角度從粒子表面反射出來。如果粒子遠小於光波的波長,則光波繞過粒子前進不受阻礙。當粒子的大小和光波波長接近或稍小時,光波產生散射。溶膠粒子的大小在1-100nm之間,與普通光波波長接近,因此有一定強度的散射現象,稱為丁鐸爾(Tyndall)現象。即當一束強光投射到溶膠上,在暗室或黑暗背景下,從光束的垂直方向觀察,可以清楚地觀察到一條光帶(圖9-5),這是膠體溶液的特點。
溶膠中膠體粒子和溶液中溶質的粒子相似,也處於不停的運動狀態,這種不停的無規則的運動稱為布朗(Brown)運動(圖9-6)。由此表現出與膠體粒子運動有關的性質,稱為膠體的分子動力學性質,如擴散、滲透、沉降等。它們和膠體粒子的大小和形狀有密切的關係。所以從分子動力學性質出發,可以研究膠體粒子的大小和形狀。其次,溶膠由於分子動力學性質,可以保持膠體粒子不因重力作用而沉集在容器底部。這種保持分散相不從分散介質中分離出來的性質,稱為動力學穩定性。
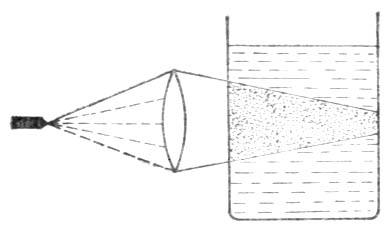
圖9-6 丁鐸爾現象

圖9-6 布朗運動
(一)電泳
1.電泳
在一U形管中,加入棕色的氫氧化鐵溶膠(圖9-7左),然後插上電極並通直流電,陰極附近顏色逐漸變深,表示氫氧化鐵膠體粒子向陰極移動(圖9-7右)。如果在U形管中換上硫化砷溶膠並通電,膠體粒子向陽極移動。這種膠體粒子在電場作用下向陽極或陰極移動的現象叫電泳。
2.膠粒帶電的原因
(1)選擇吸附由於溶膠膠核常常選擇性地吸附作為穩定劑的某種離子,而使其表面帶有電荷。溶膠膠核總是選擇吸附與其組成相類似的離子。例如Fe(OH)3溶膠,其膠核吸附穩定劑FeO+CL-中的FeO+而帶正電荷。
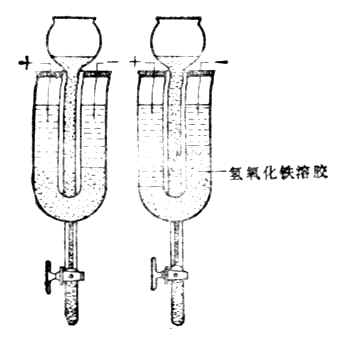
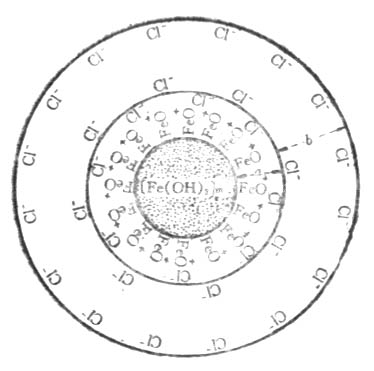
圖9-7 氫氧化鐵溶膠電泳向負極 圖9-8 氫氧化鐵膠團結構示意
圖α-吸附層,b-擴散層
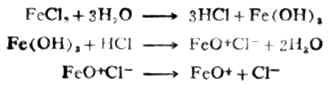
cl-則留在介質中。
在硫化砷溶膠中,其溶膠膠核吸附HS-而帶負電荷。
As2O3+3H2S →As2S3+3H2O
H2S![]()
H++HS-
H+留在介質中。
(2)表面分子離解 膠體粒子與分散介質接觸後,表面上的分子與介質作用而離解,某種離子將擴散到介質中去,因此膠體粒子帶有和擴散離子符號相反的電荷。例如,矽膠的膠粒是由很多SiO2分子組成的。粒子表面上的SiO2分子和水接觸形成矽酸H2SiO3,隨後離解生成了SiO32-和H+,H+擴散到介質中成為反離子,膠體粒子則因保留有SiO32-而帶負電荷。
3.膠團結構
現以Fe(OH)3溶膠為例來說明膠團的結構(圖9-8)。
氫氧化鐵溶膠是由許多Fe(OH)3分子構成的,其中心部分叫膠核。膠核的外邊是由FeO+和一部分CL-所形成的吸附層,膠核和吸附層統稱為膠粒。另一部分CL-借擴散作用而分布於離膠核較遠處,形成擴散層。帶有相反電荷的吸附層和擴散層電荷符號相反,電量相等,所以膠團是電中性的。膠團的結構可用下式表示。
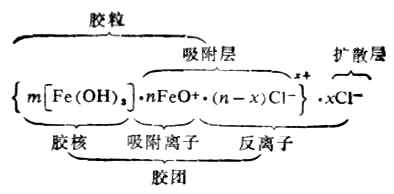
Fe(OH)3膠粒包括膠核(設為m個Fe(OH)3分子組成)和吸附層。膠粒和擴散層合稱為膠團,膠團分散在介質中乃是膠體體系。
(二)溶膠的穩定性和聚沉
由於溶膠是高度分散的多相體系,膠粒有自動聚結的趨勢,是一個聚結不穩定體系。但在某種條件下,它又具有聚結的穩定性,膠粒並不合併變大。決定聚結穩定性的主要因素是溶膠膠粒表面的雙電層結構,它使膠粒在碰撞時不致相互接觸,同時雙電層有水化離子,好像膠粒外麵包上一層水化膜或溶劑化膜,這層膜就起到阻礙膠粒合併的作用。
凡是使溶膠的分散度降低,分散相顆粒變大,最後從介質中沉澱析出的現象叫聚沉。促使溶膠聚沉的因素有電解質,反電荷的膠體,溫度等。溶膠對電解質的影響非常敏感,這是由於電解質中反離子的加入促使膠粒周圍的擴散層被「壓縮」,擴散層厚度迅速變薄,當電解質的量達到一定程度後,擴散層消失,膠粒變成電中性,同時水化膜也隨之消失,這樣膠粒就能迅速凝集而聚沉。例如,在氫氧化鐵中加入少量K2SO4溶液,溶膠內立即發生聚沉作用,析出氫氧化鐵沉澱。
不同的電解質,對溶膠的聚沉能力是不同的,通常用聚沉值來衡量電解質對溶膠聚沉能力的大小。聚沉值是指一定溶膠,在一定時間內完全聚沉所需電解質的最低濃度(mmol.L-1)。聚沉值越小,表示聚沉能力越大。
可以使溶膠聚沉的電解質的有效部分是與膠粒帶有相反電荷的離子,這些離子稱為反離子。根據叔爾采-哈迪(Schulze-Hardy)規則,反離子的價數越高,聚沉能力也越大。一般說來,一價反離子的聚沉值在25-150之間,二價的約在0.5-2之間,三價的約在0.01-0.1之間。
對於給定的溶膠,反離子為1,2,3價的電解質,其聚沉值的比約為(1/1)6:(1/2)6:(1/3)6。
帶有相反電荷的不同溶膠,可以相互聚沉。例如,將帶有正電荷的氫氧化鐵溶膠和帶負電荷的As2S3溶膠混合,可以相互聚沉。
明礬的淨水作用,是利用明礬的水解生成AL(OH)3正溶膠,而與帶負電荷的膠體污物發生相互聚沉。
溫度對溶膠的穩定性影響不大。溫度升高時,由於溶膠的布朗運動增強,溶膠粒子之間的碰撞加劇,使溶膠的穩定性下降。
| 關於「醫用化學/溶膠的性質」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |