醫用化學/界面現象
| 醫學電子書 >> 《醫用化學》 >> 膠體溶液 >> 溶膠 >> 界面現象 |
| 醫用化學 |
|
|
物體的表面是指它與空氣或與本身的蒸氣接觸的面,而物體的表面與另一相接觸的面則稱為界面。凡是界面上發生的一切物理化學現象統稱為界面現象。
(一)界面張力和界面能
由於物質分子與分子間存在相互吸引力的作用,位於表面層的分子和它的內部分子所處的情況是不同的。以液體為例來說明。圖9-1中A為處於液體內部的分子,它從各方向所受到相鄰分子的引力是均衡的,即作用於該分子上的吸引力的合力等於零。B處於液體表面層的分子,它所受到相鄰分子吸引力的合力等於零,而且其合力是指向液體內部並與液面相垂直的。液體表面層的其它分子也都受到同樣力的作用,其結果是這種合力企圖把表面層的分子拉入液體內部,因面液體表面有自動縮小的傾向。如果想使表面增大,就必須使分子從液體內部反抗引力將其拉到表面,這一過程需要消耗一定量的功,這種功成為表面層分子多餘的能量貯藏在表面上。這種液體表面層的分子比內部分子所多餘的能量叫界面能(液體——空氣),單位是J.m-2。
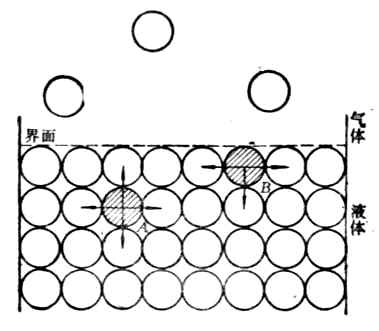
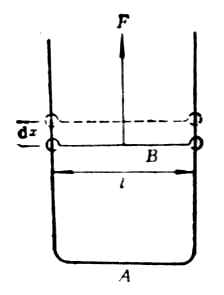
圖9-1 表面張力來源 圖9-2 表面張力的測量
在圖9-2中,線圈A上面有一個無磨擦的滑動線B,將它們浸在(具有一定界面張力的)液體中,在線圈A和滑動線B圍繞的平面上形成一層薄膜。因為液體表面有縮小的趨勢,滑動線B將自動地向下移動。現在,我們從相反方向施以外拉力F以阻止其移動。這個力F將作用於薄膜的整個邊緣l,力的大小隨著長度l而改變。從實驗中可以看到,作用於這個薄膜整個邊緣的是每單位長度的力,這個力稱界面張力,單位是N.m-1。也可用單位面積的能表示,稱比表面能,單位是J.m-2。故界面張力又稱比表面能。
(∵1J=1N.m ∴1J.m-2=1N.m.m-2=1N.m-1)
界面能等於界面張力(σ)與界面積(S)的乘積:
E=σ.S
物體的界面能有自動降低的趨勢。界面能愈大,降低的趨勢也愈大。液體界面能的減小可以通過一種自動過程來實現,即自動減小S或自動減小σ,或者S和σ兩者同時減小。
恆溫下,液體的σ是一個常數,因此界面能的減小只能通過減小S的辦法進行。如水滴常呈球形——界面能最小。在溶液中界面積不變的情況下,界面能的減小只能用減小σ的辦法進行,即液體界面從周圍介質中自動吸引其它物質分子、原子或離子填入表面層來降低它的σ,即吸附作用。
(二)吸附
溶膠屬多相分散系,分散相和分散介質之間有界面存在,對於一定體積的物質,分散粒子愈小,個數愈多,其總面積就愈大,比表面積(即單位體積物質的表面積)也就愈大。例如,當1cm3的物質分割到每邊長10-5-10-7cm大小的立方體時,其比表面積達到60-600m2,因此大大改變了界面性質。
1.固體界面上的吸附
固體的表面不能自動縮小,它只能依賴於吸附其它物質以降低界面能。具有吸附作用的物質叫吸附劑,被吸附的物質叫吸附質。疏鬆多孔的固體,如活性炭、矽膠、活性氧化鋁、鉑黑等都是良好的吸附劑。1g良好活性炭的微孔界面積可達1000m2,常用於防毒面具中,也可用作蔗糖脫色。矽膠和活性氧化鋁都可用作色層分析中的層析中的層析柱或薄層的吸附劑。鉑黑用於氫電極以吸附氫。
2.固體-氣體界面上的吸附
氣體在固體界面上的吸附作用是可逆的。氣體分子可被吸附到吸附劑的界面上,但由於分子的熱運動,氣體又可能掙脫界面進入氣相,這種過程叫解吸。當吸附與解吸達到平衡時,單位質量吸附劑所能吸附氣體的量叫做吸附量。吸附是放熱過程,解吸是吸熱過程。
當溫度不變時,增加氣體壓力,吸附量增加。當氣體的壓力增加到一定程度時,吸附量達到一極限值,這時吸附劑界面的吸附已達到飽和,這種在給定溫度下,以吸附量為縱坐標,以氣體壓力為橫坐標作圖所得的曲線,叫等溫吸附線(圖9-3)。
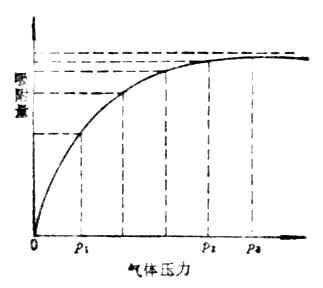
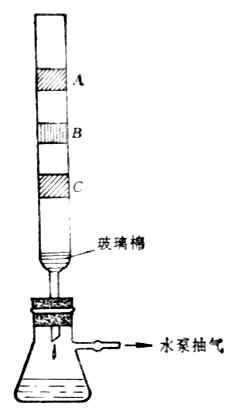
圖9-3 吸附等溫曲線 圖9-4 柱層析法簡單裝置圖
3.固體-液體界面上的吸附
固體-液體界面上的吸附,可能是溶質吸附,也可能是溶劑吸附,通常兩者兼有只是程度不同。例如,活性炭從色素水溶液中吸附的色素就遠比吸附的水多,因此可以用活性炭使溶液脫色。但是如果把活性炭放入色素的酒精溶液中,由於活性炭對酒精的吸附大於對色素的吸附,故不能用於在酒精溶液中對色素的脫色。
在固體-液體界面上的吸附中,吸附的溶質可以是電解質,也可以是非電解質。
分子吸附指吸附物質的整個分子被吸附在固-液界面上。被吸附物質是非電解質或弱電解質的分子型物質。利用各物質吸附能力的不同,選用適當的吸附劑,可將溶液中的各種溶質的混合物加以分離。利用各種溶質與吸附劑之間吸附能力的不同,使溶質得到分離的方法叫色譜法或層析法。如在一玻璃管(柱型)中,裝入某種吸附劑(如氧化鋁或矽膠)作為吸附柱。當把含各種溶質的溶液流經管中的吸附柱時,由於不同物質在吸附柱上的吸附能力不同,因而被吸附在柱的不同高度的位置上,最容易吸附的物質在柱的上部,其餘依次向下。隨後取出吸附柱,分層切開,再用溶劑分別提取,即被分離。或者用溶劑把被吸附物質由吸附柱上洗脫下來。在洗脫過程中,吸附力弱的先被洗出,吸附力強的後被洗出,將洗出液分段收集,同樣達到分離的目的。。
例如,用石油醚提取綠葉中的成分:將石油醚加到綠葉中,使其作用後,把渣子濾去,將溶液倒入吸附柱,在柱上依次顯出葉綠素、葉紅素、胡蘿卜素等色層(圖9-4中的A,B,C)。然後分別提取即可得各種成分。
| 關於「醫用化學/界面現象」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |