疏水物
| A+醫學百科 >> 疏水物 |

在化學里,疏水性指的是一個分子(疏水物)與水互相排斥的物理性質。[1]
疏水性分子偏向於非極性,並因此較會溶解在中性和非極性溶液(如有機溶劑)。疏水性分子在水裡通常會聚成一團,而水在疏水性溶液的表面時則會形成一個很大的接觸角而成水滴狀。
舉例來說,疏水性分子包含有烷烴、油、脂肪和多數含有油脂的物質。
疏水性通常也可以稱為親脂性,但這兩個詞並不全然是同義的。即使大多數的疏水物通常也是親脂性的,但還是有例外,如矽橡膠和碳氟化合物(Fluorocarbon)。
目錄 |
性質理論
根據熱力學的理論,物質會尋求存在於最低能量的狀態,而關鍵便是個可以減少化學能的辦法。水是極性物質,並因此可以在內部形成氫鍵,這使得它有許多獨別的性質。但是,因為疏水物不是電子極化性的,它們無法形成氫鍵,所以水會對疏水物產生排斥,而使水本身可以互相形成氫鍵。這即是導致疏水作用(這名稱並不正確,因為能量作用是來自親水性的分子[2])的疏水效應,因此兩個不相溶的相態(親水性對疏水性)將會變化成使其界面的面積最小時的狀態。此一效應可以在相分離的現象中被觀察到。
超疏水性
超疏水性物質,如荷葉,具有極難被水沾溼的表面,其水在其表面的接觸角超過150°,滑動角小於20°。
理論
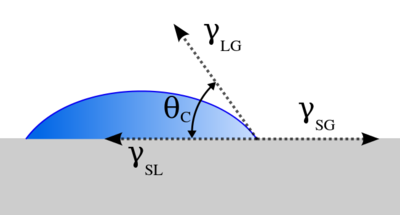
1805年,托馬斯·楊通過分析作用在由氣體環繞的固體表面的液滴的力而確定了接觸角θ。[3]
-
- 其中
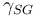 = 固體和氣體之間的表面張力
= 固體和氣體之間的表面張力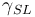 = 固體和液體之間的表面張力
= 固體和液體之間的表面張力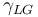 = 液體和氣體之間的表面張力
= 液體和氣體之間的表面張力
θ可以用接觸角測量計來測量。
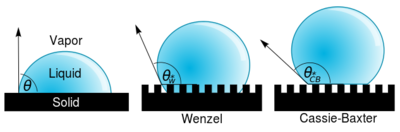
Wenzel確定了當液體直接接觸微結構化的表面時,θ角會轉變為θW *
-
- cosθW * = rcosθ
其中,r為實際面積與投影面積的比率。[4]Wenzel的方程顯示了微結構化一個表面將會放大表面張力。疏水性表面(具有大於90°的接觸角)在微結構化之後會變得更加疏水,其新的接觸角將比原來增大。然而,一個親水性表面(具有小於90°的接觸角)在微結構化之後卻會變得更加親水,其新的接觸角將比原來減小。[5]
Cassie和Baxter發現如果液體懸浮在微結構表面,θ角將會變為θCB *
-
- cosθCB * = φ(cos θ + 1) – 1
其中,φ為固體與液體接觸面積的比例。[6]在Cassie-Baxter狀態下的液體比Wenzel狀態下更具有運動性。
通過用以上兩個方程計算出的新接觸角,我們可以預測Wenzel狀態或Cassie-Baxter狀態是否應該存在。由於有自由能最小化的限制,預測出具有更小的新接觸角的狀態就會更可能存在。從數學上來說,要使Cassie-Baxter狀態存在,以下的不等式必須成立。[7]
-
- cos θ < (φ-1)/(r - φ)
最近提出的一個判斷Cassie-Baxter狀態是否存在的替代標準是:1)接觸線力克服液滴未被支撐部分的重力;2)微結構足夠高從而阻止液滴接觸微結構的基底(即凹面)。[8]
接觸角是靜態測量疏水性的方法,接觸角滯後和滑動角則對疏水性的動態測量法。接觸角滯後是一種鑒定表面異質性的現象。[9]當移液器將液體注到固體表面時,液體就會形成一定的接觸角。隨著注入液體的增加,液滴的體積會隨之增加,接觸角也會變大,但三相邊界會保持固定直到液體突然溢出。在液體溢出前瞬間的接觸角被稱為前進接觸角。回退接觸角可以通過將液體從液滴中吸出來測量。隨著液體被吸出,液滴的體積減小,接觸角也減小,但三相邊界同樣保持固定直到被完全吸回。在液體被吸回瞬間的接觸角被稱為回退接觸角。而前進接觸角和回退接觸角之間的差異就是接觸角滯後,它被用來鑒定表面的異質性、粗糙性和運動性。非同質的表面會有能夠阻礙接觸線的區域。滑動角是另一種動態測量疏水性的方法:在固體表面放置一個液點,傾斜表面知道液滴開始滑動,此時的傾斜角即為滑動角。處於Cassie-Baxter狀態的液滴通常會表現出比Wenzel狀態更小的滑動角和接觸角滯後。
研究和應用
許多在自然界中找到的超疏水性物質都遵循Cassie定律,而它在次微米尺度下可以和空氣組成雙相物質。蓮花效應便是基於此一原理而形成的。仿生學上,超疏水性物質的例子有利用奈米科技製作的nanopin膜(nanopin film)。
另見
參考
- ↑ Aryeh Ben-Na'im Hydrophobic Interaction Plenum Press, New York (ISBN 0-306-40222-X)
- ↑ Goss, K. U. and R. P. Schwarzenbach (2003): "Rules of Thumb for Assessing Equilibrium Partitioning of Organic Compounds: Successes and Pitfalls." JOURNAL OF CHEMICAL EDUCATION 80(4): 450-455. Link to abstract
- ↑ Young, T.. An Essay on the Cohesion of Fluids. Phil. Trans. R. Soc. Lond.. 1805, 95: 65–87. doi:10.1098/rstl.1805.0005.
- ↑ Wenzel, RN. Resistance of Solid Surfaces to Wetting by Water. Ind. Eng. Chem.. 1936, 28: 988-994.
- ↑ de Gennes, Pierre-Gilles. Capillarity and Wetting Phenomena. 2004.
- ↑ Cassie, ABD. Wettability of Porous Surfaces. Trans. Faraday Soc.. 1944, 40: 546-551.
- ↑ Quere, D. Non-sticking Drops. Reports on Progress in Physics. 2005, 68: 2495-2532.
- ↑ Extrand, C. Criteria for Ultralyophobic Surfaces. Langmuir. 2004, 20: 5013-5018.
- ↑ Johnson, RE. Contact Angle Hysteresis. J. Phys. Chem.. 1964, 68: 1744-1750.
外部連結
|
||||||||||||||
參考來源
| 關於「疏水物」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |