醫用化學/酸鹼反應
| 醫學電子書 >> 《醫用化學》 >> 電解質溶液 >> 酸鹼質子理論 >> 酸鹼反應 |
| 醫用化學 |
|
|
酸鹼質子理論中的酸鹼反應是酸鹼之間的質子傳遞。例如:
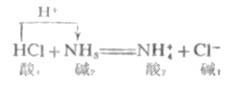
這個反應無論在水溶液中、苯或氣相中,它的實質都是一樣的。HCL是酸,放出質子給NH3,然後轉變成共軛鹼CL-,NH3是鹼,接受質子後轉變成共軛酸NH4+。強鹼奪取了強酸放出的質子,轉化為較弱的共軛酸和共軛鹼。
酸鹼質子理論不僅擴大了酸鹼的範圍,還可以把酸鹼離解作用、中和反應、水解反應等,都看作是質子傳遞的酸鹼反應。
由此可見,酸鹼質子理論更好地解釋了酸鹼反應,擺脫了酸鹼必須在水中才能發生反應的局限性,解決了一些非水溶劑或氣體間的酸鹼反應,並把水溶液中進行的某些離子反應系統地歸納為質子傳遞的酸鹼反應,加深了人們對酸鹼和酸鹼反應的認識。但是酸鹼質子理論不能解釋那些不交換質子而又具有酸鹼性的物質,因此它還存在著一定的局限性。
路易斯提出的酸鹼電子理論是目前概括最廣的酸鹼理論。該理論認為,凡是能給出電子對的物質叫做鹼;凡是能接受電子對的物質叫做酸。即酸是電子對的接受體,鹼是電子對的給予體。因此,鹼中給出電子的原子至少有一對孤對電子(未成鍵的電子對),而酸中接受電子的原子至少有一個空軌道(外層未填充電子的軌道),以便接受鹼給予的電子對,這種由路易斯定義的酸和鹼叫做路易斯酸和路易斯鹼。例如,三氟化硼(BF3)是路易斯酸,因為BF3中的B原子有一個空軌道是電子的接受體。NH3中N原子有一對孤對電子,是電子對的給予體,為路易斯鹼。但是,由於酸鹼電子理論概括的酸鹼範圍太寬,使其實用價值受到一定的限制。
出自A+醫學百科 「醫用化學/酸鹼反應」條目 http://cht.a-hospital.com/w/%E5%8C%BB%E7%94%A8%E5%8C%96%E5%AD%A6/%E9%85%B8%E7%A2%B1%E5%8F%8D%E5%BA%94 轉載請保留此連結
| 關於「醫用化學/酸鹼反應」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |