醫用化學/多元酸鹼在溶液中的離解
| 醫學電子書 >> 《醫用化學》 >> 電解質溶液 >> 電解質在溶液中的離解 >> 多元酸鹼在溶液中的離解 |
| 醫用化學 |
|
|
|
多元酸鹼在溶液中的離解是分步進行的,叫做分步離解。表2-2列出了一些常見的多元酸的分步離解常數。表中pKa為Ka的負對數值。
表2-2 一些常見的多元酸的分步離解常數
| 名稱 | 分子式 | Ka1 | PKa1 | Ka2 | PKa2 | Ka3 | PKa3 | |
| 酸性強度增加 | 草酸 | H2C2O4 | 5.4×10-2 | 1.27 | 5.4×10-5 | 4.27 |
2.2×10-13 |
12.67 |
| 亞硫酸 | H2SO3 | 1.54×10-2 | 1.81 | 1.02×10-7 | 6.91 | |||
| 磷酸 | H3PO4 | 7.52×10-3 | 2.12 | 6.23×10-8 | 7.21 | |||
| 丙二酸 | CH2(COOH)2 | 1.38×10-3 | 2.86 | 2×10-6 | 5.70 | |||
| 鄰苯二甲酸 | C6H4(COOH)2 | 1.12×10-3 | 2.95 | 3.9×10-5 | 5.41 | |||
| 酒石酸 | (CHOHCOOH)2 | 9.1×10-4 | 3.04 | 4.3×10-5 | 4.37 | |||
| 碳酸 | H2CO3 | 4.30×10-7 | 6.37 | 5.61×10-11 | 10.25 | |||
| 氫硫酸 | H2S | 9.1×10-8 | 7.04 | 1.1×10-12 | 11.96 |
例如草酸(H2C2O4)的離解分兩步進行。
一級離解
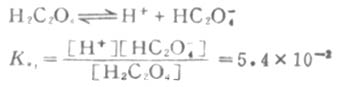
二級離解
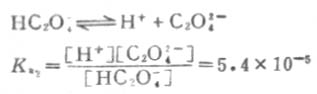
二級離解總比一級離解困難,因為H+要克服帶有兩個電荷的C2O2-4對它的吸引。從Ka1和Ka2可以反映這一點。草酸溶液中的HC2O-4濃度要比C2O2-4濃度大得多。
磷酸的離解要分步,有Ka1、Ka2、和Ka3三個離解常數,且Ka1》Ka2》Ka3。這說明多元酸分級離解是依次變難。
根據多元酸的濃度和各級離解常數,可以算出溶液中各種離子的濃度。
例2 計算0.1mol.L-1H2S溶液中的H+和S2-的濃度。
解:由於H2S的 Ka1》Ka2 ,所以H2S溶液中的H+主要來自第一步離解,而第一步離解所產生的H+,又抑制第二步離解。這樣計算H2S溶液中H+的總濃度時,可以忽略第二步離解的H+,近似地等於第一步離解平衡時H+濃度。
設第一步離解平衡時[H+]=x,則[H+]≈[HS-],平衡時則有下列關係:
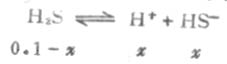
由表2-2知H2S的Ka為9.1×10-8,則
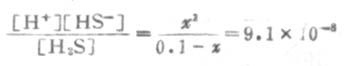
因Ka1很小,x必然很小,所以0.1-x≈0.1,則
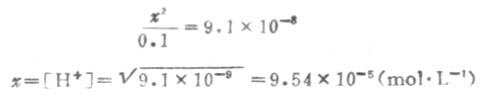
溶液中的S2-是第二步離解的產生,因此,計算溶液中的S2-濃度時,應根據第二步離解平衡進行計算.
設第二步離解時,[S2-]=y,平衡時有下列關係:
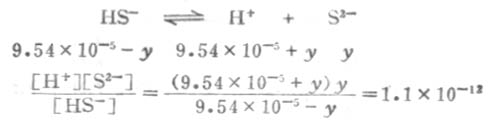
因為Ka1極小,y必然極小,所以9.54×10-5±y≈9.54×10-5,則
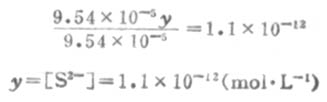
所以,[S2-]≈Ka2。
出自A+醫學百科 「醫用化學/多元酸鹼在溶液中的離解」條目 http://cht.a-hospital.com/w/%E5%8C%BB%E7%94%A8%E5%8C%96%E5%AD%A6/%E5%A4%9A%E5%85%83%E9%85%B8%E7%A2%B1%E5%9C%A8%E6%BA%B6%E6%B6%B2%E4%B8%AD%E7%9A%84%E7%A6%BB%E8%A7%A3 轉載請保留此連結
| 關於「醫用化學/多元酸鹼在溶液中的離解」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |