乙酸
| A+醫學百科 >> 乙酸 |
乙酸又稱醋酸,廣泛存在於自然界,它是一種有機化合物,是典型的脂肪酸。被公認為食醋內酸味及刺激性氣味的來源。在家庭中,乙酸稀溶液常被用作除垢劑。食品工業方面,在食品添加劑列表E260中,乙酸是規定的一種酸度調節劑。
目錄 |
簡介
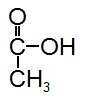
乙酸(acetic acid)分子中含有兩個碳原子的飽和羧酸。分子式C2H4O2,結構簡式CH3COOH。因是醋的主要成分,又稱醋酸。例如在水果或植物油中主要以其化合物酯的形式存在;在動物的組織內、排泄物和血液中以游離酸的形式存在 。無色液體 ,有刺激性氣味。熔點16 .6℃,沸點117 .9℃, 相對密度1.0492(20/4℃),折光率1.3716。純乙酸在16.6℃以下時能結成冰狀的固體,所以常稱為冰醋酸。易溶於水、乙醇、乙醚和四氯化碳。當水加到乙酸中,混合後的總體積變小,密度增加,直至分子比為1∶1 ,相當於形成一元酸的原乙酸CH3C(OH)3,進一步稀釋,體積不再變化。
分子量:60.05
分子結構:
純的無水乙酸(冰醋酸)是無色的吸濕性液體,凝固點為16.6 °C (62 °F) ,凝固後為無色晶體。儘管根據乙酸在水溶液中的離解能力它是一個弱酸,但是乙酸是具有腐蝕性的,其蒸汽對眼和鼻有刺激性作用。乙酸是一種簡單的羧酸,是一個重要的化學試劑。乙酸也被用來製造電影膠片所需要的醋酸纖維素和木材用膠粘劑中的聚乙酸乙烯酯,以及很多合成纖維和織物。
命名
乙酸既是常用的名稱,也是國際純粹與應用化學聯合會(IUPAC)規定的官方名稱。俗稱醋酸(acetic acid),該名稱來自於拉丁文中的表示醋的詞「acetum」。無水的乙酸在略低於室溫的溫度下(16.7℃),能夠轉化為一種具有腐蝕性的冰狀晶體,故常稱無水醋酸為冰醋酸,冰乙酸,冰形醋酸,乙酸冰。
乙酸的實驗式(即最簡式)為CH2O,化學式(即分子式)為C2H4O2。常被寫為CH3-COOH、CH3COOH或CH3CO2H來突出其中的羧基,表明更加準確的結構。失去H後形成的離子為乙酸根陰離子。乙酸最常用的正式縮寫是AcOH 或 HOAc,其中Ac代表了乙酸中的乙醯基(CH3CO)。酸鹼中和反應中也可以用HAc表示乙酸,其中Ac代表了乙酸根陰離子(CH3COO),但很多人認為這樣容易造成誤解。上述兩種情況中,Ac都不應與化學元素中錒的縮寫混淆。
易錯點
乙酸與「蟻酸」「己酸」不同
① 蟻酸(formic acid) = 甲酸(methanoic acid)
化學式:HCOOH(HCO2H)
② 羊油酸(caproic acid) = 己酸(hexanoic acid)
(百度小詞典中譯「乙酸」為「caproic acid」有誤)
化學式CH3(CH2)4COOH
物理性質
乙酸在常溫下是一種有強烈刺激性酸味的無色液體。 乙酸的熔點為16.5℃(289.6 K)。沸點118.1℃(391.2 K)。相對密度1.05,閃點39℃,爆炸極限4%~17%(體積)。純的乙酸在低於熔點時會凍結成冰狀晶體,所以無水乙酸又稱為冰醋酸。 乙酸易溶於水和乙醇,其水溶液呈弱酸性。乙酸鹽也易溶於水。 下為中華人民共和國關於工業乙酸的國家標準
| 指標名稱 | 指標 | ||
| 優等品 | 一等品 | 合格品 | |
| 色度, Hazen 單位(鉑 - 鈷色號)≤ | 10 | 20 | 30 |
| 乙酸含量, % ≥ | 99.8 | 99.0 | 98.0 |
| 水分, % ≤ | 0.15 | - | - |
| 甲酸含量, % ≤ | 0.06 | 0.15 | 0.35 |
| 乙醛含量, % ≤ | 0.05 | 0.05 | 0.10 |
| 蒸發殘渣, % ≤ | 0.01 | 0.02 | 0.03 |
| 鐵含量(以 Fe 計), % ≤ | 0.00004 | 0.0002 | 0.0004 |
| 還原高錳酸鉀物質, min ≥ | 30 | 5 | - |
化學性質
酸性
羧酸中,例如乙酸,的羧基氫原子能夠部分電離變為氫離子(質子)而釋放出來,導致羧酸的酸性。乙酸在水溶液中是一元弱酸,酸度係數為4.8,pKa=4.75(25℃),濃度為1mol/L的醋酸溶液(類似於家用醋的濃度)的pH為2.4,也就是說僅有0.4%的醋酸分子是解離的。
乙酸的酸性促使它還可以與碳酸鈉、氫氧化銅、苯酚鈉等物質反應。
2CH3COOH + Na2CO3 =2NaCH3COO + CO2 ↑+ H2O
2CH3COOH + Cu(OH)2 =Cu(CH3COO)2 + 2H2O
CH3COOH + C6H5ONa =C6H5OH (苯酚)+ CH3COONa
二聚物
乙酸的二聚體,虛線表示氫鍵
乙酸的晶體結構顯示 ,分子間通過氫鍵結合為二聚體(亦稱二締結物),二聚體也存在於120℃的蒸汽狀態。二聚體有較高的穩定性,現在已經通過冰點降低測定分子量法以及X光衍射證明了分子量較小的羧酸如甲酸、乙酸在固態及液態,甚至氣態以二聚體形式存在。當乙酸與水溶和的時候,二聚體間的氫鍵會很快的斷裂。其它的羧酸也有類似的二聚現象。
(兩端連接H)
溶劑
液態乙酸是一個親水(極性)質子化溶劑,與乙醇和水類似。因為介電常數為6.2,它不僅能溶解極性化合物,比如無機鹽和糖,也能夠溶解非極性化合物,比如油類或一些元素的分子,比如硫和碘。它也能與許多極性或非極性溶劑混合,比如水,氯仿,己烷。乙酸的溶解性和可混合性使其成為了化工中廣泛運用的化學品。
化學反應
對於許多金屬,乙酸是有腐蝕性的,例如鐵、鎂和鋅,反應生成氫氣和金屬乙酸鹽。因為鋁在空氣中表面會形成氧化鋁保護層,所以鋁製容器能用來運輸乙酸。金屬的乙酸鹽也可以用乙酸和相應的鹼性物質反應,比如最著名的例子:小蘇打與醋的反應。除了醋酸鉻(II),幾乎所有的醋酸鹽能溶於水。
Mg(s)+ 2 CH3COOH(aq) → (CH3COO)2Mg(aq) + H2(g) NaHCO3(s) + CH3COOH(aq) → CH3COONa(aq) + CO2(g) + H2O(l)
乙酸能發生普通羧酸的典型化學反應,特別注意的是,可以還原生成乙醇,通過親核取代機理生成乙醯氯,也可以雙分子脫水生成酸酐。
同樣,乙酸也可以成酯或氨基化合物。如乙酸可以與乙醇在濃硫酸存在並加熱的條件下生成乙酸乙酯(本反應為可逆反應,反應類型屬於取代反應中的酯化反應)。
CH3COOH + CH3CH2OH<==> CH3COOCH2CH3 + H2O
鑒別
乙酸可以通過其氣味進行鑒別。若加入氯化鐵(III),生成產物為深紅色並且會在酸化後消失,通過此顏色反應也能鑒別乙酸。乙酸與三氧化砷反應生成氧化二甲砷,通過產物的惡臭可以鑒別乙酸。
生物化學
乙酸中的乙醯基,是生物化學中所有生命的基礎。當它與輔酶A結合後,就成為了碳水化合物和脂肪新陳代謝的中心。然而,乙酸在細胞中的濃度是被嚴格控制在一個很低的範圍內,避免使得細胞質的pH發生破壞性的改變。與其它長鏈羧酸不同,乙酸並不存在於甘油三酸脂中。但是,人造含乙酸的甘油三酸脂,又叫甘油醋酸酯(甘油三乙酸酯),則是一種重要的食品添加劑,也被用來製造化妝品和局部性藥物。
乙酸由一些特定的細菌生產或分泌。值得注意的是醋菌類梭菌屬的丙酮丁醇梭桿菌,這個細菌廣泛存在於全世界的食物、水和土壤之中。在水果或其他食物腐敗時,醋酸也會自然生成。乙酸也是包括人類在內的所有靈長類生物的陰道潤滑液的一個組成部分,被當作一個溫和的抗菌劑
製取方式
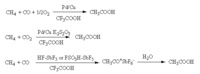
主要製法有:
① 乙醛催化氧化法: 2CH3CHO+O2→2CH3COOH
CH3OH+CO→CH3COOH
③ 低碳烷或烯液相氧化法:
2C4H10+5O2→4CH3COOH+2H2O
以上各反應皆需催化劑與適宜的溫度、壓力。除合成法還有發酵法,我國用米或酒釀造醋酸。
乙酸最初由發酵法及木材乾餾法製得,現一般由乙醇或乙醛氧化製得,近年來利用丁烷為原料通過催化、氧化製得(醋酸鈷為催化劑,空氣氧化後,得到的乙酸是含有酮、醛、醇等的混合物)。
對環境的影響:
一、健康危害
侵入途徑:吸入、食入、經皮吸收。
健康危害:吸入後對鼻、喉和呼吸道有刺激性。對眼有強烈刺激作用。皮膚接觸,輕者出現紅斑,重者引起化學灼傷。誤服濃乙酸,口腔和消化道可產生糜爛,重者可因休克而致死。
慢性影響:眼瞼水腫、結膜充血、慢性咽炎和支氣管炎。長期反覆接觸,可致皮膚乾燥、脫脂和皮炎。
二、毒理學資料及環境行為
毒性:屬低毒類。
急性毒性:LD503530mg/kg(大鼠經口);1060mg/kg(兔經皮);LC505620ppm,1小時(小鼠吸入);人經口1.47mg/kg,最低中毒量,出現消化道症状;人經口20~50g,致死劑量。
亞急性和慢性毒性:人吸入200~490mg/m3×7~12年,有眼瞼水腫,結膜充血,慢性咽炎,支氣管炎。
致突變性:微生物致突變:大腸桿菌300ppm(3小時)。姊妹染色單體交換:人淋巴細胞5mmlo/L。
生殖毒性:大鼠經口最低中毒劑量(TDL0):700mg/kg(18天,產後),對新生鼠行為有影響。大鼠睾丸內最低中毒劑量(TDL0):400mg/kg(1天,雄性),對雄性生育指數有影響。
危險特性:其蒸氣與空氣形成爆炸性混合物,遇明火、高熱能引起燃燒爆炸。與強氧化劑可發生反應。
燃燒(分解)產物:一氧化碳、二氧化碳。
醋酸是一種極為重要的化工產品,它在有機化工中的地位與無機化工中的硫酸相當。醋酸的主要用途有:
(1)醋酸乙烯。醋酸的最大消費領域是製取醋酸乙烯,約佔醋酸消費的44%以上,它廣泛用於生產維綸、聚乙烯醇、乙烯基共聚樹脂、黏合劑、塗料等。
(2)溶劑。醋酸在許多工業化學反應中用作溶劑。
(3)醋酸纖維素。醋酸可用於制醋酐,醋酐的80%用於製造醋酸纖維,其餘用於醫藥、香料、染料等。
(4)醋酸酯。醋酸乙酯、醋酸丁酯是醋酸的兩個重要下游產品。醋酸乙酯用於清漆、稀釋料、人造革、硝酸纖維、塑料、染料、藥物和香料等;醋酸丁酯是一種很好的有機溶劑,用於硝化纖維、塗料、油墨、人造革、醫藥、塑料和香料等領域。
其他補充,滿足國際運輸操作人員需要
中文名稱:醋酸
別 名:醋酸、冰醋酸
英文名稱:ACETIC ACID,Ethanic acid,Vinegar acid
英文縮寫:A C 聯合國編號(UNNO):2789
化學式:CH3COOH
理化性質
相對密度(水為1):1.050 凝固點(℃):16.7
沸點(℃):118.3 粘度(Pa.s):1.22
20℃時蒸氣壓(KPa):1.5
外觀及氣味:無色液體,有刺鼻的醋味。
溶解性:能溶於水、乙醇、乙醚、四氯化碳及甘油等有機溶劑。
相容性:材料:稀釋後對金屬有強烈腐蝕性,316#和318#不鏽鋼及鋁可作良好的結構材料。
燃燒爆炸危險性
閃點(℃):39 爆炸極限(%):4.0-17
靜電作用:可能有 聚合危害:
燃燒性: 自燃溫度:
危險特性:能與氧化劑發生強烈反應,與氫氧化鈉與氫氧化鉀等反應劇烈。稀釋後對金屬有腐蝕性。
消防方法:用霧狀水、乾粉、抗醇泡沫、二氧化碳、滅火。用水保持火場中容器冷卻。用霧狀水驅散蒸氣,趕走泄漏液體,使稀釋成為不燃性混合物。並用水噴淋去堵漏的人員。
泄漏處理
污染排放類別:Z
泄漏處理:切斷火源,穿戴好防護眼鏡、防毒面具和耐酸工作服,用大量水沖洗溢漏物,使之流入航道,被很快稀釋,從而減少對人體的危害。
健康危害性
健康危害性評價:2, 3, 2 閾限值(TLV):50
大鼠經口LD50:3530(mg/kg)
健康危害:吸入後對鼻、喉、和呼吸道強烈的刺激作用。皮膚接觸,輕者出現紅斑,重者引起化學灼傷。誤服農醋酸,口腔和消化道可因休克致死。
急救
皮膚接觸:皮膚接觸先用水沖洗,再用肥皂徹底洗滌。
眼睛接觸:眼睛受刺激用水沖洗,嚴重的須送醫院診治。
吸 入:若吸入蒸氣得使患者脫離污染區,安置休息並保暖。
食 入:誤服立即漱口,給予催吐劑催吐,急送醫院診治。
防護措施
呼吸系統防護:空氣中深度濃度超標時,應佩戴防毒面具。
眼睛防護:戴化學安全防護眼鏡。
手防護:戴橡皮手套。
其它:工作後,淋浴更衣,不要將工作服帶入生活區。
儲運
適裝船型:3 適裝艙型:不鏽鋼艙
儲運注意事項:注意貨物溫度保持在20-35℃,即貨物溫度要大於其凝固點16.7℃防止凍結。裝卸貨完畢時要盡量排儘管系中的殘液。
冰醋酸用途
冰醋酸是最重要的有機酸之一.主要用於醋酸乙烯、醋酐、醋酸纖維、醋酸酯和金屬醋酸鹽等,也用作農藥、醫藥和染料等工業的溶劑和原料,在照相藥品製造、織物印染和橡膠工業中都有廣泛用途. 冰醋酸是重要的有機化工原料之一,它在有機化學工業中處於重要地位.醋酸廣泛用於合成纖維、塗料、醫藥、農藥、食品添加劑、染織等工業,是國民經濟的一個重要組成部分.冰醋酸按用途又分為工業和食用兩種,食用冰醋酸可作酸味劑、增香劑.可生產合成食用醋.用水將乙酸稀釋至4-5%濃度,添加各種調味劑而得食用醋.其風味與釀造醋相似.常用於番茄調味醬、蛋黃醬、醉米糖醬、泡菜、乾酪、糖食製品等.使用時適當稀釋,還可用於製作蕃茄、蘆筍、嬰兒食品、沙丁魚、魷魚等罐頭,還有酸黃瓜、肉湯羹、冷飲、酸法乾酪用於食品香料時,需稀釋,可製作軟飲料,冷飲、糖果、焙烤食品、布丁類、膠媒糖、調味品等.作為酸味劑,可用於調飲料、罐頭等. 洗滌通常使用的冰醋酸,濃度分別為28%,56%,99%的.如果買的是冰醋酸,把28CC的冰醋酸加到72CC的水裡,就可得到28%的醋酸.更常見的是它以56%的濃度出售,這是因為這種濃度的醋酸只要加同量的水,即可得到28%的醋酸. 濃度大幹28%的醋酸會損壞醋酸纖維和代納爾纖雛. 草酸是有機酸中的強酸之一,在高錳酸鉀的酸性溶液中,草酸易被氧化生成二氧化碳和水.草酸能與鹼類起中和反應,生成草酸鹽. 醋酸也一樣,28%的醋酸具有揮發性,揮發後使織物是中性;就象氨水可以中和酸一樣,28%的醋酸也可以中和鹼. 鹼也會導致變色.用酸(如28%的醋酸)即可把變色恢復過來. 這種酸也常用來減少由丹寧複合物、茶、咖啡、果計、軟飲料以及啤酒造成的黃漬.在去除這些污漬時,28%的醋酸用在水和中性潤滑劑之後,可用到最大程度.
乙酸反應化學方程式
乙酸與碳酸鈉:2CH3COOH+Na2CO3==2CH3COONa+CO2↑+H2O
乙酸與碳酸氫鈉:NaHCO3+CH3COOH=NaCH3COO+H2O+CO2↑
醋酸與鹼反應:CH3COOH+OH-=CH3COO- +H2O
醋酸與弱酸鹽反應:2CH3COOH+CO32-=2CH3COO- +H2O+CO2↑
醋酸與活潑金屬單質反應:Fe+2CH3COOH=Fe(CH3COO)2+H2↑
醋酸與金屬氧化物反應:2CH3COOH+ZnO=Zn(CH3COO)2+H2O
醋酸與醇反應:CH3COOH+C2H5OH=CH3COOC2H5+H2O(條件是加熱,濃硫酸催化,可逆反應)
|
||||||||
|
||||||||||||||||||||||||||
| 關於「乙酸」的留言: | |
|
目前暫無留言 | |
| 添加留言 | |